Clear Sky Science · pl
Obrazowanie śródoperacyjne biopsji ryzyka raka płuca
Widzieć ukryte ślady raka
Chirurdzy zajmujący się rakiem płuca stają przed zadaniem o wysokiej stawce: w trakcie operacji muszą szybko zlokalizować maleńkie guzy i ich dokładne brzegi, a dostępne dziś narzędzia mogą przeoczyć niebezpieczne miejsca lub zajmować zbyt dużo czasu. W tym badaniu przedstawiono nowe podejście do „zobaczenia” raka, polegające nie na analizie samych komórek nowotworowych, lecz na obserwacji mikroskopowej rusztowania, które je otacza. Łącząc zaawansowane obrazowanie laserowe z metodami sztucznej inteligencji, autorzy pokazują, że można szybko i z zadziwiającą precyzją wykrywać raka płuca i jego granice.
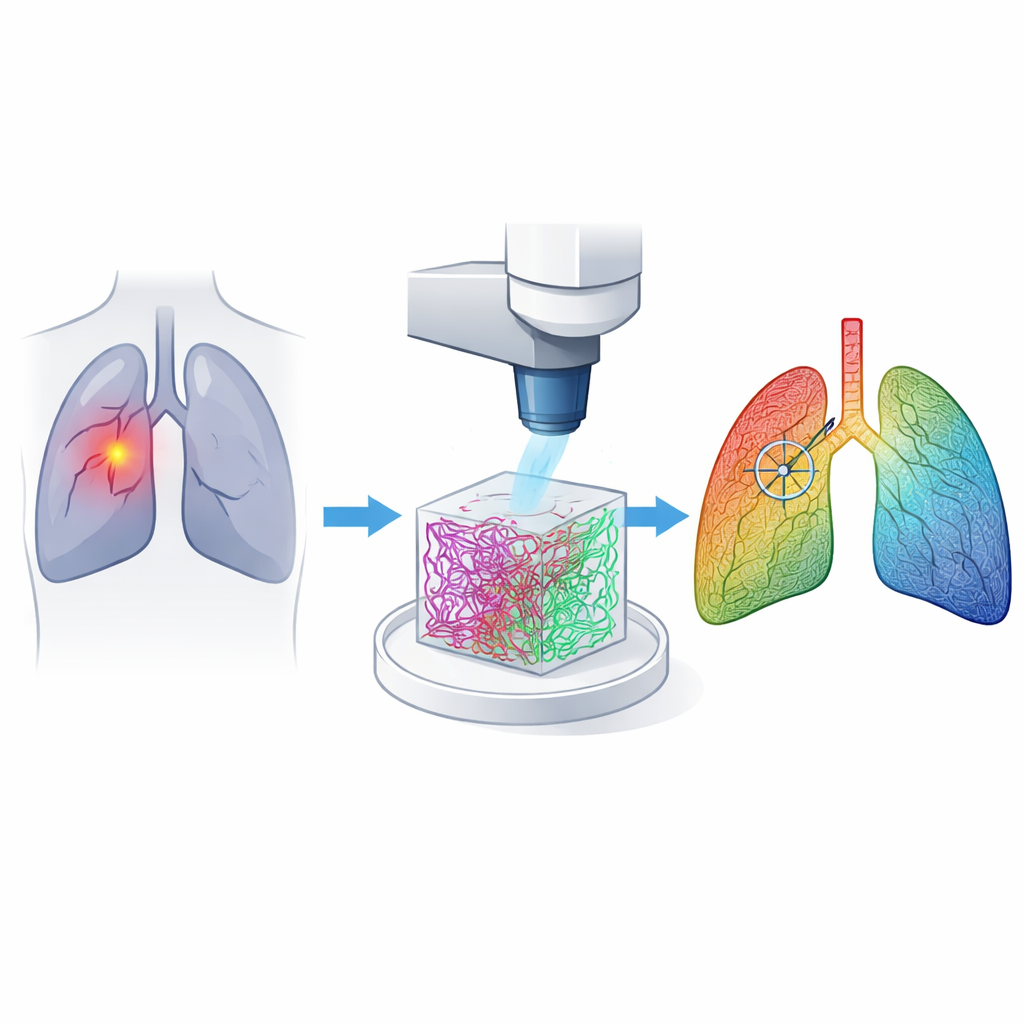
Tkanka podporowa, która opowiada historię
Nasze płuca utrzymywane są przez sieć włókien białkowych zwaną macierzą zewnątrzkomórkową. Dwa kluczowe składniki, kolagen i elastyna, zapewniają tkance płucnej wytrzymałość i sprężystość. Gdy rozwija się rak, te włókna są przebudowywane: zmienia się ich układ, gęstość i wzajemne interakcje. Badacze wysunęli hipotezę, że te subtelne zmiany strukturalne mogą służyć jako wiarygodne odciski palców raka, nawet gdy guzy trudno dostrzec zwykłą kamerą chirurgiczną.
Delikatny mikroskop laserowy na sali operacyjnej
Zespół zbudował niestandardowy mikroskop multiphotonowy, rodzaj systemu laserowego, który może penetrować setki mikrometrów w świeżej tkance bez konieczności stosowania barwników. Przy jednym ustawieniu lasera w bliskiej podczerwieni rejestruje jednocześnie dwa sygnały: jeden uwidacznia kolagen, drugi — elastynę. To podwójne obrazowanie daje ostre widoki 3D sieci włókien płuca w ciągu kilku minut na miejsce, co jest wystarczająco szybkie, by być praktycznym podczas zabiegu. Metodę przetestowano na tkankach pobranych od 222 pacjentów z gruczolakorakiem płuca, rejestrując setki małych stosów obrazów 3D zarówno z obszarów guzowych, jak i prawidłowych.
Nauczanie SI odczytywania kodu włókien
Zamiast oceniać te obrazy wzrokowo, naukowcy zmierzyli każdy mały element objętości, czyli woksel, w szeregu cech: jak bardzo włókna są zorientowane, jak faliste się wydają, jak gęsto wypełniają przestrzeń, jak grube są pasma elastyny oraz jak podobne w położeniu i kierunku są pobliskie włókna kolagenu i elastyny. Wprowadzili nowy „współczynnik podobieństwa”, który rośnie, gdy kolagen i elastyna leżą blisko siebie i ukierunkowane są w podobny sposób. Przy użyciu uczenia bez nadzoru pogrupowali miliony wokseli w powtarzające się „słownictwa” włókien oddające typowe wzorce strukturalne. Standardowy klasyfikator uczenia maszynowego nauczył się następnie, jak mieszanka tych słownictw różni się między tkanką prawidłową a nowotworową.
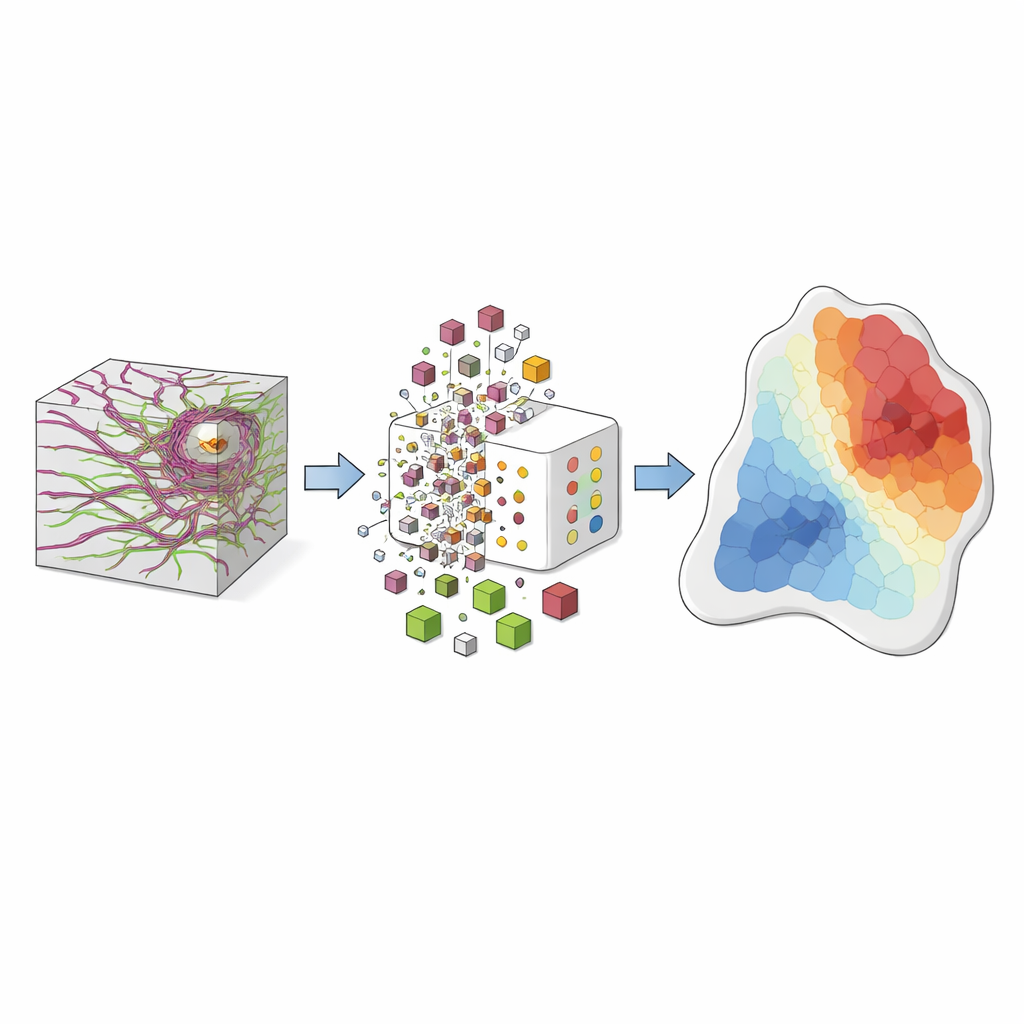
Od niewidocznych wzorców do map ryzyka
Gdy ten system przetestowano na niezależnym zestawie próbek płuc, zidentyfikował raka z czułością około 99%, co oznacza, że niemal nigdy nie przeoczył guza. Badacze poszli dalej i stworzyli „wskaźnik ryzyka raka” dla każdego słownictwa włókien, wskazujący, czy ma ono tendencję do występowania w tkance zdrowej czy chorobowej. Kolorując każdy woksel zgodnie z tym wskaźnikiem, wygenerowali intuicyjne mapy ryzyka: obszary guzowe świecą ciepłymi barwami, zdrowe — chłodnymi, a strefy graniczne pokazują mieszankę. Mapy te skutecznie wyznaczały granicę między guzem a tkanką normalną w ludzkich preparatach i ukazywały te same trendy przebudowy w modelu myszy obrazowanym in vivo, co sugeruje, że podejście to mogłoby zostać przetłumaczone na wskazówki w czasie rzeczywistym na sali operacyjnej.
Co to może znaczyć dla pacjentów
Zamiast czekać na wyniki patologii z mrożonych przekrojów, chirurgowie mogliby pewnego dnia zeskanować podejrzane obszary płuca małą sondą laserową i od razu zobaczyć, gdzie rak najprawdopodobniej się ukrywa, ujawniony przez zreorganizowany kolagen i elastynę wokół niego. Badanie pokazuje, że wspierające rusztowanie guza niesie silny, czytelny sygnał ryzyka i że SI może przekształcić ten sygnał w czytelne wskazówki wizualne. Jeśli zostanie rozwinięte do narzędzi klinicznych, takie obrazowanie mogłoby zwiększyć dokładność biopsji, zmniejszyć liczbę reoperacji i pomóc zapewnić usunięcie niebezpiecznej tkanki przy jednoczesnym zachowaniu jak największej ilości zdrowego płuca.
Cytowanie: Qian, S., Yang, L., Meng, J. et al. Intraoperative biopsy imaging of lung cancer risk. Commun Med 6, 143 (2026). https://doi.org/10.1038/s43856-026-01406-y
Słowa kluczowe: chirurgia raka płuca, obrazowanie śródoperacyjne, macierz zewnątrzkomórkowa, mikroskopia multiphotonowa, diagnostyka sztucznej inteligencji