Clear Sky Science · pl
Charakterystyka genomowa i podklastrowanie kompleksu klonalnego Escherichia coli 38 ujawniają markery genetyczne związane z gospodarzem
Dlaczego to ma znaczenie w codziennym życiu
Infekcje odporne na antybiotyki przestały być jedynie problemem szpitalnym — coraz częściej dotyczą żywności, zwierząt, podróży i życia społecznego. W tym badaniu skupiono się na konkretnej grupie bakterii Escherichia coli, zwanej kompleksem klonalnym 38 (CC38), która może powodować ciężkie zakażenia krwi i dróg moczowych i często wykazuje oporność na najważniejsze antybiotyki. Śledząc pochodzenie tych bakterii oraz ich przemieszczanie się między ludźmi, zwierzętami i środowiskiem, badacze ujawniają wskazówki, które mogą pomóc władzom zdrowia publicznego zatrzymać niebezpieczne szczepy, zanim rozprzestrzenią się szeroko.
Bliższe spojrzenie na kłopotliwą rodzinę bakterii
Nie wszystkie szczepy E. coli są szkodliwe, ale niektóre linie wielokrotnie powodują poważne choroby. CC38 w ostatnim czasie wyłonił się jako jedna z takich problematycznych grup, ustępując pod względem częstości tylko dobrze znanej, wysokiego ryzyka linii (ST131) w duńskich zakażeniach krwi. Zespół przebadał 242 oporne szczepy E. coli CC38 od duńskich pacjentów, 83 pochodzące z żywności i zwierząt gospodarskich oraz ponad 2 300 powiązanych genomów zebranych na całym świecie. Wykorzystali sekwencjonowanie całych genomów — zasadniczo odczytanie DNA każdej bakterii — aby odwzorować, jak powiązane są różne gałęzie tej rodziny, jakie geny oporności noszą i w jakich gospodarzy się przeważnie pojawiają.
Śledząc szlak od szpitali po farmy i żywność
Porównując E. coli CC38 z duńskich próbek pacjentów z tymi z drobiu, bydła i żywności, badacze wyróżnili dwie główne duńskie grupy. Jedna grupa składała się głównie z izolatów ludzkich, podczas gdy druga obejmowała bakterie z drobiu, innych zwierząt gospodarskich i produktów spożywczych. Co ważne, nie znaleziono niemal identycznych dopasowań DNA między izolatami ludzkimi a zwierzęcymi, co sugeruje brak wyraźnych ognisk zakażeń przenoszonych drogą żywnościową w Danii w badanym okresie. Jednak modele statystyczne analizujące segmenty DNA dodatkowego (akcesoryjnego) wskazały, że niektóre podgrupy związane z ludźmi prawdopodobnie mają pochodzenie drobiowe, co sugeruje przeszłe lub pośrednie przejście ze zwierząt (kur) na ludzi.
Globalne drzewo rodowe z dwiema dużymi gałęziami
Rozszerzając analizę do światowego zbioru 2 638 genomów, zespół zbudował globalne „drzewo rodowe” dla CC38. Wyraźnie wyodrębniły się dwie główne gałęzie. Jedna była silnie powiązana z drobiem i wykazywała umiarkowane poziomy oporności oraz wiele cech związanych z ciężkimi chorobami. Druga była zdominowana przez podgrupy związane z ludźmi, różniące się opornością, potencjałem chorobotwórczym i preferencjami gospodarzy. Niektóre podgrupy były wyraźnie ukierunkowane na ludzi i silnie oporne, podczas gdy inne miały mieszane wzorce — pojawiały się u ludzi, drobiu, dzikich zwierząt, w wodzie i u zwierząt towarzyszących. Ten mozaikowy obraz odzwierciedla zdolność CC38 do adaptacji do różnych środowisk i gatunków gospodarzy, co komplikuje wysiłki kontrolne.
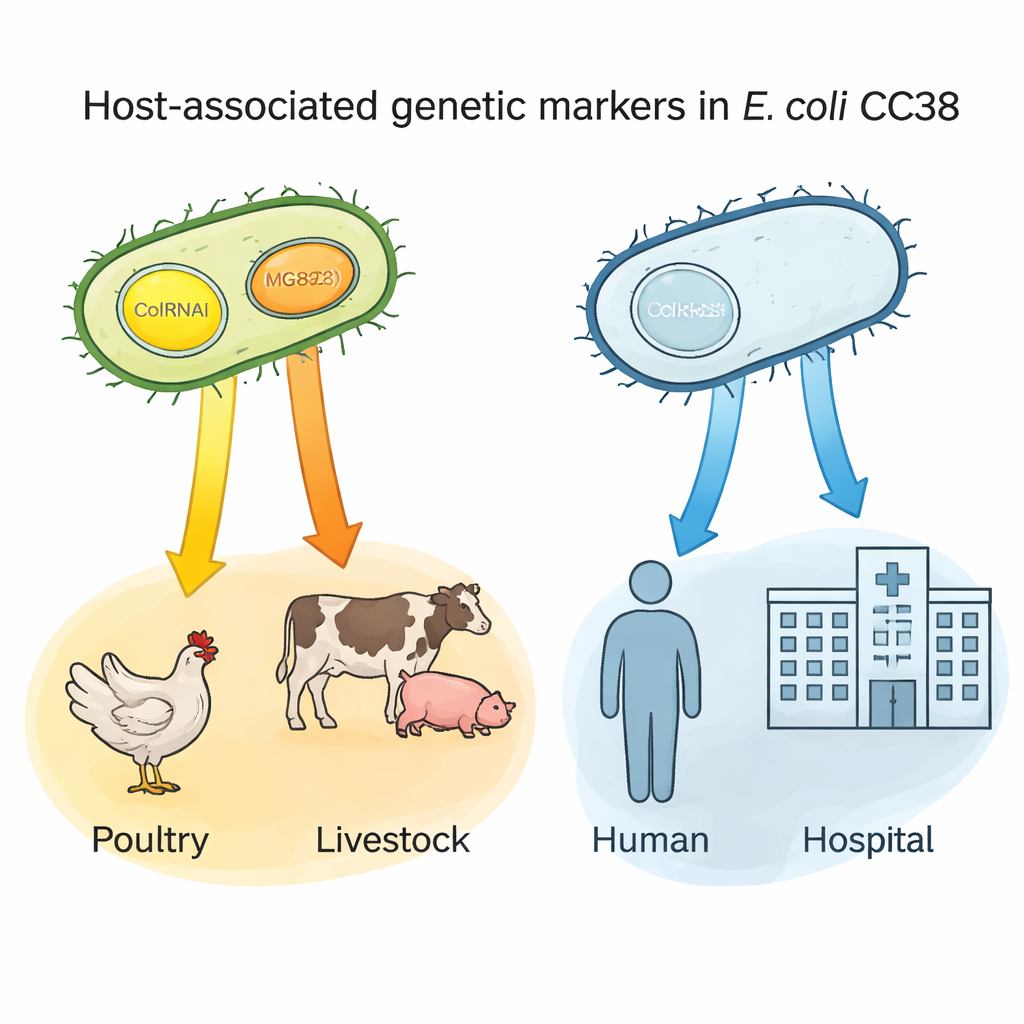
Małe kółka DNA jako „identyfikatory” gospodarza
Kluczowe odkrycie dotyczyło dwóch maleńkich elementów DNA — plazmidów nazwanych ColRNAI i Col(MG828) — które mogą przenosić się między bakteriami. Plazmidy te były powszechne w CC38 pochodzącym z drobiu i innych zwierząt gospodarskich, ale rzadkie w podgrupach skoncentrowanych na ludziach. Analiza statystyczna wykazała, że posiadanie któregokolwiek z tych plazmidów silnie predykowało pochodzenie drobiowe; noszenie obu jednocześnie było szczególnie charakterystyczne dla linii powiązanych z hodowlą i niektórymi źródłami żywności. Ponieważ plazmidy te często niosą również cechy oporności, mogą działać jak genetyczne „identyfikatory”, wskazujące bakterie prawdopodobnie pochodzące z rezerwuarów zwierzęcych i pomagające śledzić, jak oporne szczepy dostają się do łańcucha żywnościowego i trafiają do ludzi.
Co to oznacza dla ochrony zdrowia
Dla osoby niebędącej specjalistą najważniejsze przesłanie jest takie, że szkodliwe, lekooporne E. coli nie ograniczają się do szpitali czy pacjentów: tworzą powiązane populacje obejmujące ludzi, drób, zwierzęta gospodarskie, dziką faunę, żywność i środowisko. To badanie pokazuje, że w obrębie jednej ważnej linii — CC38 — niektóre gałęzie są silnie związane ze zwierzętami, inne z ludźmi, a konkretne ruchome elementy DNA mogą pomóc ustalić, skąd dany szczep prawdopodobnie pochodzi. Wykorzystanie tych markerów genetycznych w rutynowym nadzorze mogłoby dawać wczesne ostrzeżenia, gdy związane ze zwierzętami szczepy oporne zaczynają pojawiać się u ludzi. W konsekwencji wspiera to podejście „Jedno Zdrowie” — traktujące zdrowie ludzi, zwierząt i środowiska jako część jednego systemu — w celu projektowania bardziej inteligentnych, ukierunkowanych strategii zapobiegania infekcjom i spowalniania rozprzestrzeniania się oporności na antybiotyki.
Cytowanie: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Słowa kluczowe: oporność na środki przeciwdrobnoustrojowe, Escherichia coli, transmisja zoonotyczna, drób i bydło, nadzór genomowy