Clear Sky Science · pl
Wysokorozdzielczy zintegrowany atlas pojedynczych komórek raka głowy i szyi niezwiązanego z HPV
Dlaczego ta mapa nowotworu ma znaczenie
Raki głowy i szyi niezwiązane z wirusem brodawczaka ludzkiego (HPV) są częste, często agresywne i notorycznie nieprzewidywalne: dwaj pacjenci z wyglądającymi podobnie guzami mogą reagować bardzo różnie na to samo leczenie. W tym badaniu postanowiono zrozumieć przyczyny, przyglądając się poziomowi pojedynczych komórek. Autorzy połączyli dane z ponad 230 000 komórek od 54 pacjentów, tworząc szczegółowy „atlas” raka głowy i szyi niezwiązanego z HPV. Atlas ujawnia, jakie komórki występują w guzach, jak ze sobą współdziałają i jak mogą kształtować odpowiedź na leczenie oraz rokowanie pacjentów.
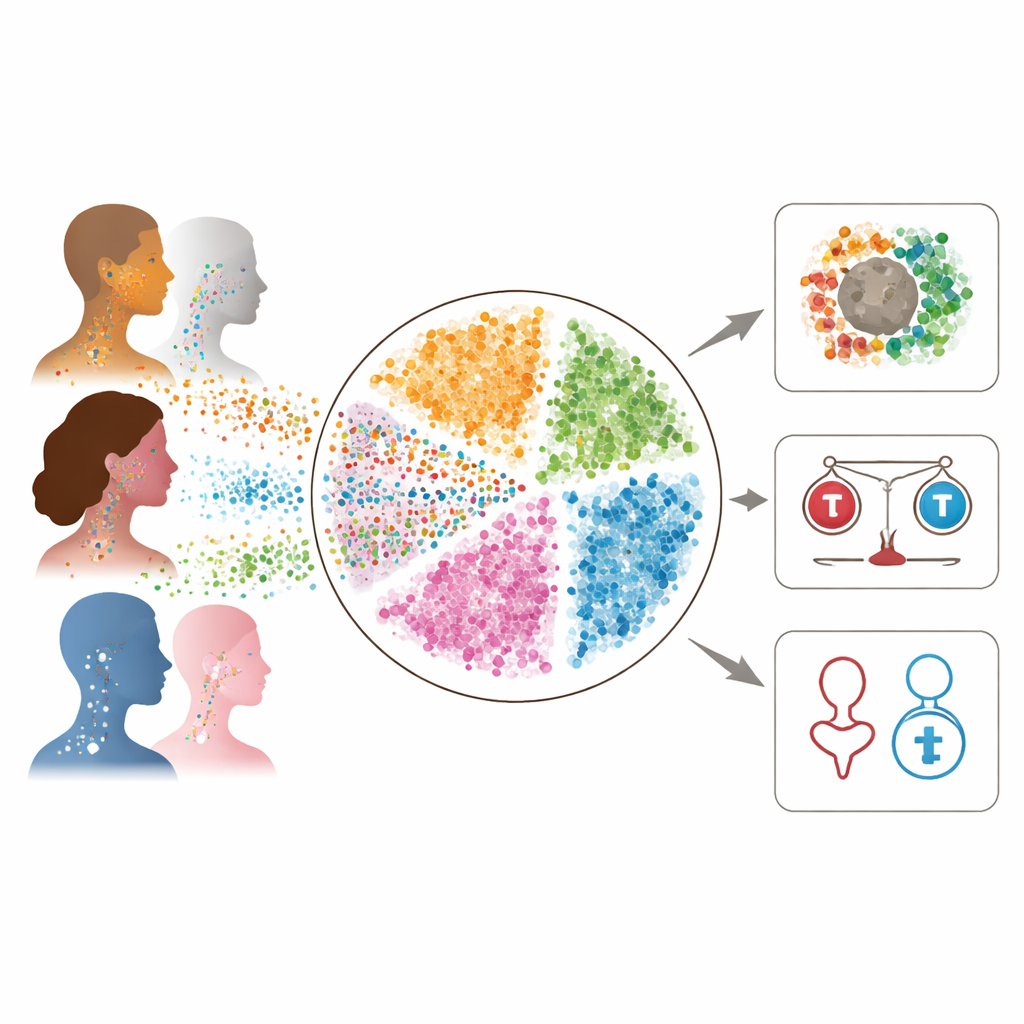
Budowa wysoko rozdzielczego atlasu nowotworu
Naukowcy połączyli sześć wcześniej opublikowanych zestawów danych sekwencjonowania RNA pojedynczych komórek od pacjentów, których nowotwory powstawały głównie w jamie ustnej i krtani i były powiązane z paleniem lub używaniem alkoholu, a nie z zakażeniem HPV. Każdy zestaw danych został wygenerowany nieco innymi metodami, więc zespół zastosował staranne kroki obliczeniowe, aby oczyścić dane, usunąć komórki niskiej jakości i ujednolicić etykiety komórkowe. Następnie wykorzystano zaawansowane algorytmy do zintegrowania zestawów w jedną spójną mapę, w której komórki grupowały się według typów biologicznych (takich jak komórki nowotworowe, komórki odpornościowe czy komórki naczyń krwionośnych), a nie według pochodzenia ze studium. Ta integracja stworzyła potężne narzędzie: wspólny punkt odniesienia, który odzwierciedla zarówno różnorodność, jak i wspólne wzorce w guzach niezwiązanych z HPV.
Kto mieszka wewnątrz tych guzów?
W „sąsiedztwie” immunologicznym guzów atlas wyróżnił wiele podtypów limfocytów T, limfocytów B, komórek plazmatycznych, makrofagów, monocytów, komórek dendrytycznych i neutrofili. Poprzez ocenę komórek za pomocą znanych programów genowych autorzy odtworzyli, jak cytotoksyczne limfocyty CD8 i komórki NK mogą przesuwać się wzdłuż kontinuum od wysoko cytotoksycznych do dysfunkcjonalnych, wyczerpanych stanów. Stwierdzili, że nowotwory we wczesnym stadium (T1) są wzbogacone w bardziej efektywne, cytotoksyczne limfocyty CD8, gdy rozważa się cały atlas — zależność zbyt subtelna, by ujawnić ją w pojedynczym badaniu. Zespół również uporządkował klastry immunologiczne w coś w rodzaju „drzewa rodzinnego”, pokazując, jak pokrewne podtypy grupują się razem i które kombinacje typów komórek mają tendencję do wspólnego wzrostu i spadku u pacjentów, wzorce odzwierciedlające dobre lub złe rokowanie opisane wcześniej.
Ukryci gracze: specjalne komórki mieloidalne i fibroblasty
Główną korzyścią z większego zbioru danych była zdolność rozróżnienia drobnych subpopulacji w mikrośrodowisku guza. Wśród komórek mieloidalnych atlas odtworzył dwa stany makrofagów wcześniej powiązane z wynikiem choroby, ale także wyróżnił odrębną populację bogatą w IL1B, która była niekonsekwentnie oznaczana w wcześniejszych badaniach. Komórki te produkują molekuły zapalne i immunosupresyjne oraz wykazują unikatowe wzory sygnalizacji obejmujące czynnik martwicy nowotworu, interleukinę‑1β i białko macierzy zwane trombospondyną — wszystkie związane z wzrostem guza, opornością na leki lub zmianami naczyń krwionośnych. W compartmentum stromalnym autorzy rozdzielili fibroblasty związane z rakiem na kilka grup, w tym dwa odrębne typy fibroblastów zapalnych: jeden zorientowany wokół chemokiny CXCL8, drugi wokół CXCL12. Pokazali, że fibroblasty bogate w CXCL8 preferencyjnie sygnalizują do komórek naczyń krwionośnych przez receptor ACKR1, droga która, jak sugerują inne badania, może sprzyjać powstawaniu nowych naczyń i gorszemu rokowaniu.
Komórki krawędzi guza i różnice związane z płcią
Komora nabłonkowa — główne ciało nowotworu — również wykazała wyraźną strukturę. Na podstawie wzorców kopii liczby DNA zespół oddzielił komórki nabłonkowe normalne od złośliwych, a następnie uporządkował je wzdłuż skali różnicowania i „plastyczności”. Jeden klaster, oznaczony Epi1, łączył cechy podobne do komórek macierzystych, częściową przemianę nabłonkowo‑mezenchymalną (program powiązany z inwazją i opornością na terapię) oraz wysokie potencjały rozwojowe. Porównanie z danymi przestrzennymi od innych pacjentów wykazało, że komórki Epi1 odpowiadają regionom „wiodącej krawędzi” guza na froncie inwazji, gdzie komórki nowotworowe spotykają się i wchodzą w interakcje z komórkami stromalnymi wspierającymi wzrost. Analizy komunikacji ujawniły, że te komórki krawędzi zarówno wysyłają, jak i odbierają intensywne sygnały związane z macierzą zewnątrzkomórkową i czynnikami wzrostu — szczególnie TGF‑β — od fibroblastów i komórek naczyń krwionośnych. Wreszcie, dzięki dużej kohorcie, badanie odkryło zmiany w składzie komórkowym związane z płcią: pacjenci płci męskiej mieli wyższy odsetek niektórych makrofagów oraz komórek proliferujących i CD8 T, a także więcej agresywnych komórek Epi1 i innego klastra nabłonkowego, podczas gdy pacjentki miały stosunkowo więcej komórek plazmatycznych, monocytów i komórek NK.
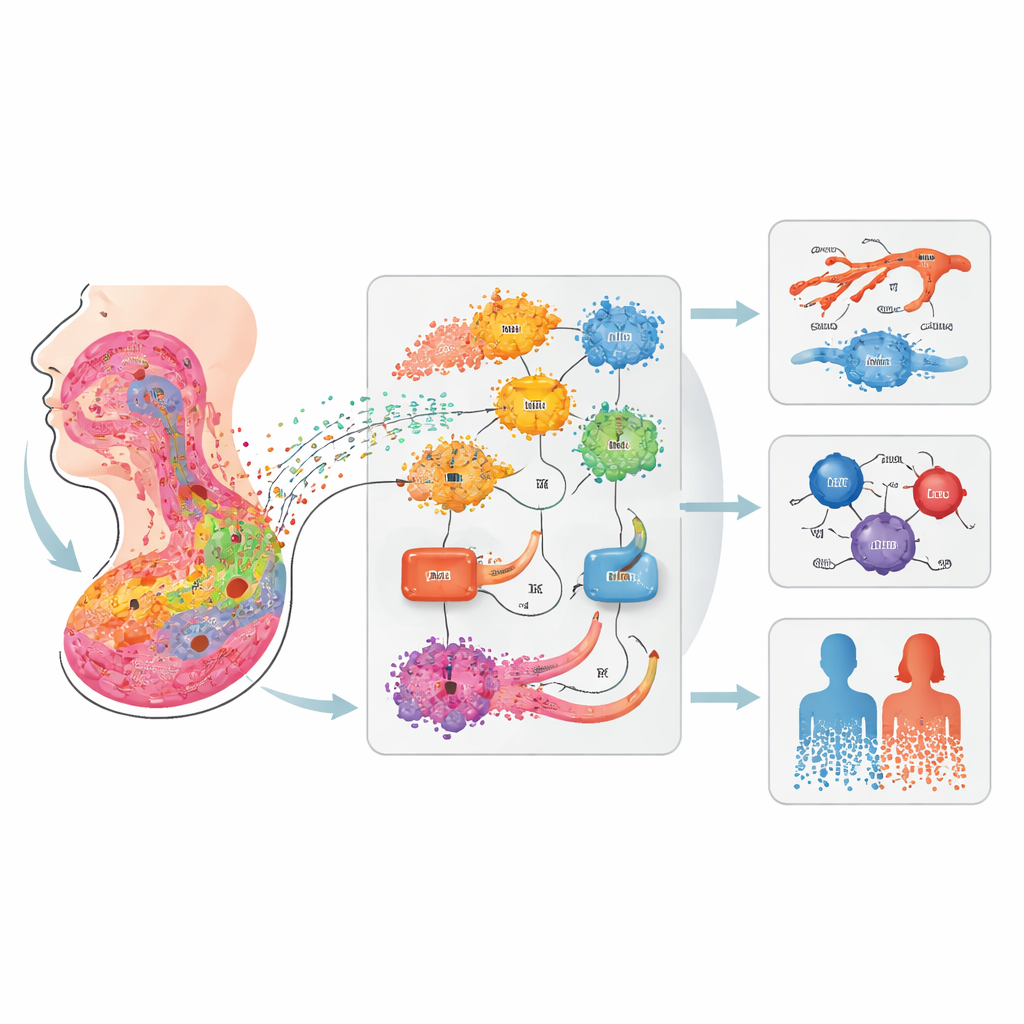
Co to oznacza dla pacjentów i przyszłych badań
Podsumowując, praca ta przekształca rozproszone zbiory danych od pojedynczych pacjentów w zjednoczony, publiczny atlas raka głowy i szyi niezwiązanego z HPV w rozdzielczości pojedynczych komórek. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że guz to nie tylko masa identycznych komórek nowotworowych: to ekosystem, w którym określone komórki odpornościowe, fibroblasty i inwazyjne komórki krawędziowe mogą hamować chorobę lub ją napędzać oraz wpływać na to, kto skorzysta z immunoterapii lub innych metod leczenia. Wyjaśniając tożsamość i interakcje populacji komórkowych, takich jak komórki mieloidalne pozytywne dla IL1B, fibroblasty produkujące CXCL8 oraz komórki nabłonkowe o cechach podobnych do komórek macierzystych na krawędzi guza, atlas wskazuje konkretne cele komórkowe i szlaki sygnałowe, które mogą być przetestowane w kontekście nowych leków lub terapii skojarzonych. Równie ważne, dostarcza wspólnego języka i mapy odniesienia, dzięki którym przyszłe badania będą mogły łatwiej porównywać wyniki, badać różnice związane z płcią i łączyć wzorce molekularne z wynikami klinicznymi w sposób bardziej precyzyjny i spersonalizowany.
Cytowanie: Kroehling, L., Chen, A., Spinella, A. et al. A highly resolved integrated single-cell atlas of HPV-negative head and neck cancer. Commun Med 6, 138 (2026). https://doi.org/10.1038/s43856-026-01401-3
Słowa kluczowe: płaskonabłonkowy rak głowy i szyi, sekwencjonowanie RNA pojedynczych komórek, mikrośrodowisko guza, fibroblasty związane z nowotworem, krajobraz immunologiczny guza