Clear Sky Science · pl
Predykcja wyniku na podstawie przestrzennego profilowania białek w rakach piersi potrójnie ujemnych
Dlaczego układ komórek nowotworowych ma znaczenie
Kiedy lekarze oglądają pod mikroskopem agresywny rak piersi, widzą zatłoczony krajobraz komórek nowotworowych, komórek układu odpornościowego i tkanki wspierającej. Ale do niedawna większość testów skupiała się na tym, ile danej cząsteczki jest obecne, a nie na tym, gdzie się znajduje. Badanie to pokazuje, że fizyczne rozmieszczenie białek i komórek w rakach piersi potrójnie ujemnych może przewidywać losy pacjentów i przedstawia nowy sposób odczytywania tych przestrzennych wzorców bezpośrednio z obrazów o wysokiej rozdzielczości.
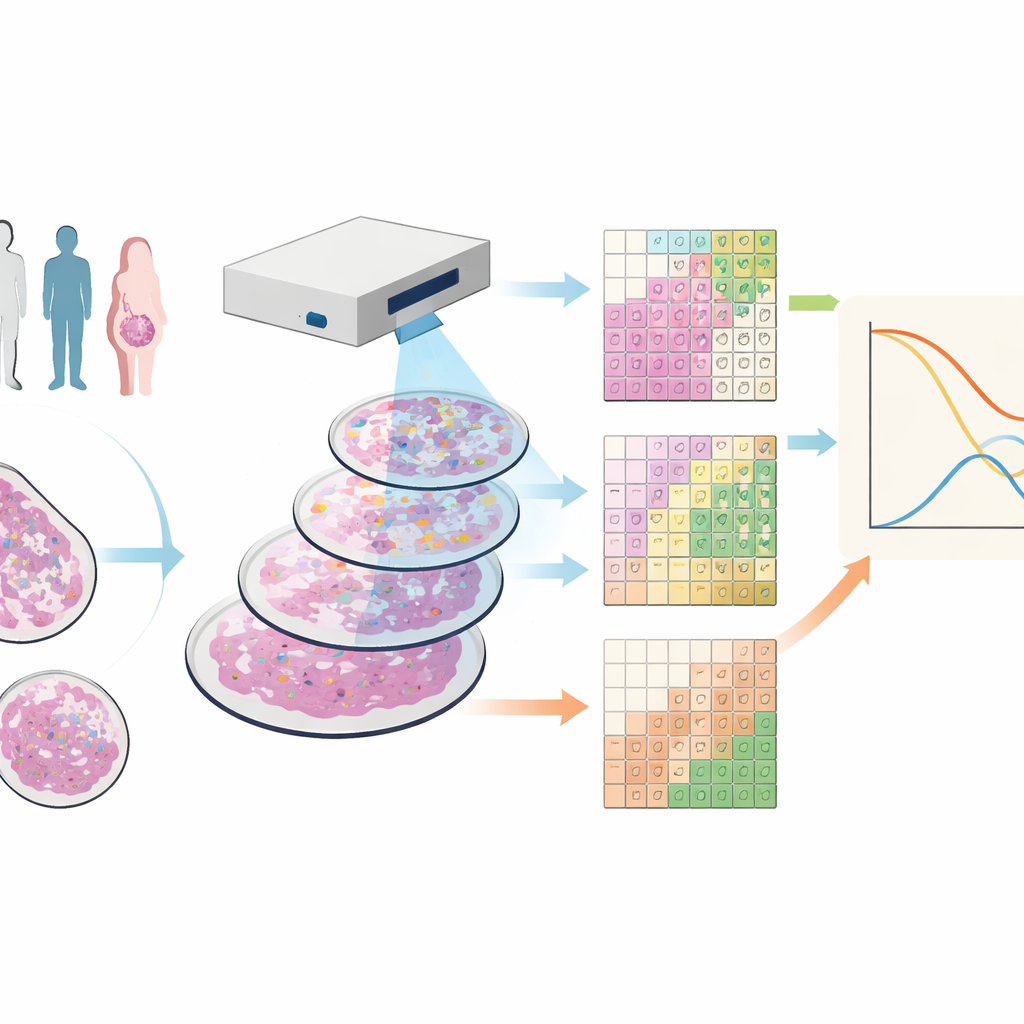
Widzenie tkanki nowotworowej wieloma kolorami
Naukowcy pracowali na próbkach tkankowych od 88 osób z rakiem piersi potrójnie ujemnym — formą choroby pozbawioną powszechnych celów terapeutycznych i często o złym rokowaniu. Zastosowali technikę zwaną obrazowaniem przy użyciu cytometrii mas, która barwi każdą próbkę dziesiątkami przeciwciał znakowanych metalami. Pod specjalnym skanerem powstają obrazy, na których każdy punkt tkanki ma szczegółowy „odcisk palca” wielu różnych białek, ujawniając jednocześnie komórki nowotworowe, różne komórki odpornościowe, naczynia krwionośne i włókna strukturalne.
Dzielenie obrazu na kafelki zamiast na komórki
Większość obecnych narzędzi próbuje odrysować granice każdej komórki i potem klasyfikować je według typu — proces, który może być podatny na błędy i powolny, zwłaszcza w cienkich wycinkach tkanki, gdzie komórki są częściowo utrwalone. Zespół opracował zamiast tego SparTile, metodę, która pomija rysowanie konturów pojedynczych komórek. SparTile dzieli każdy obraz na wiele małych nachodzących na siebie kwadratów, czyli kafelków, i wykorzystuje techniki matematyczne do wykrywania powtarzających się wzorców kombinacji białek w tych kafelkach. Najpierw grupuje kafelki w szerokie regiony — guz, tkankę wspierającą (szkliwiak/stroma) lub obszary bogate w komórki odpornościowe — a następnie dzieli każdy region na bardziej specyficzne „mikrośrodowiska”, z własnymi mieszaninami białek i typami sąsiadujących komórek.
Ukryte sąsiedztwa powiązane z wynikiem pacjenta
Po zmapowaniu tych mikrośrodowisk naukowcy zmierzyli, jak często każdy wzorzec pojawiał się w próbce każdego pacjenta i porównali to z długoterminowym przeżyciem. Pojawiło się kilka uderzających powiązań. Jedno mikrośrodowisko zlokalizowane w obrębie guza, bogate w białko o nazwie MX1 oraz markery komórek mieloidalnych, wiązało się ze znacznie wyższym ryzykiem zgonu. Inny wzorzec guza, oznaczony wimentyną — sygnałem, że komórki nowotworowe przeszły w stan bardziej ruchliwy i inwazyjny — również silnie korelował ze złym przeżyciem. Natomiast obszary zdominowane przez określone komórki T wiązały się z lepszymi wynikami, podczas gdy rejony bogate w komórki B wykazywały słabsze efekty, prawdopodobnie dlatego, że były rzadkie w małych rdzeniach tkankowych analizowanych w badaniu.
Odległość między komórkami nowotworowymi a odpornościowymi jako sygnał ostrzegawczy
Poza samą obecnością określonych sąsiedztw istotne były też ich relacje przestrzenne. Zespół zmierzył, jak blisko siebie leżały regiony guza i regiony bogate w komórki mieloidalne, obliczając statystyczną miarę nakładania się ich sygnałów białkowych w przestrzeni. Pacjenci, u których obszary bogate w komórki mieloidalne były ściśle wplecione w masy nowotworowe, mieli tendencję do gorszych wyników niż ci, u których te dwie populacje były bardziej rozdzielone. Miara tej „odległości” pozostała silnym predyktorem ryzyka nawet po uwzględnieniu standardowych czynników klinicznych, a jej znaczenie potwierdziło się przy testowaniu na dwóch niezależnych zbiorach obrazów raka piersi od innych grup badawczych.
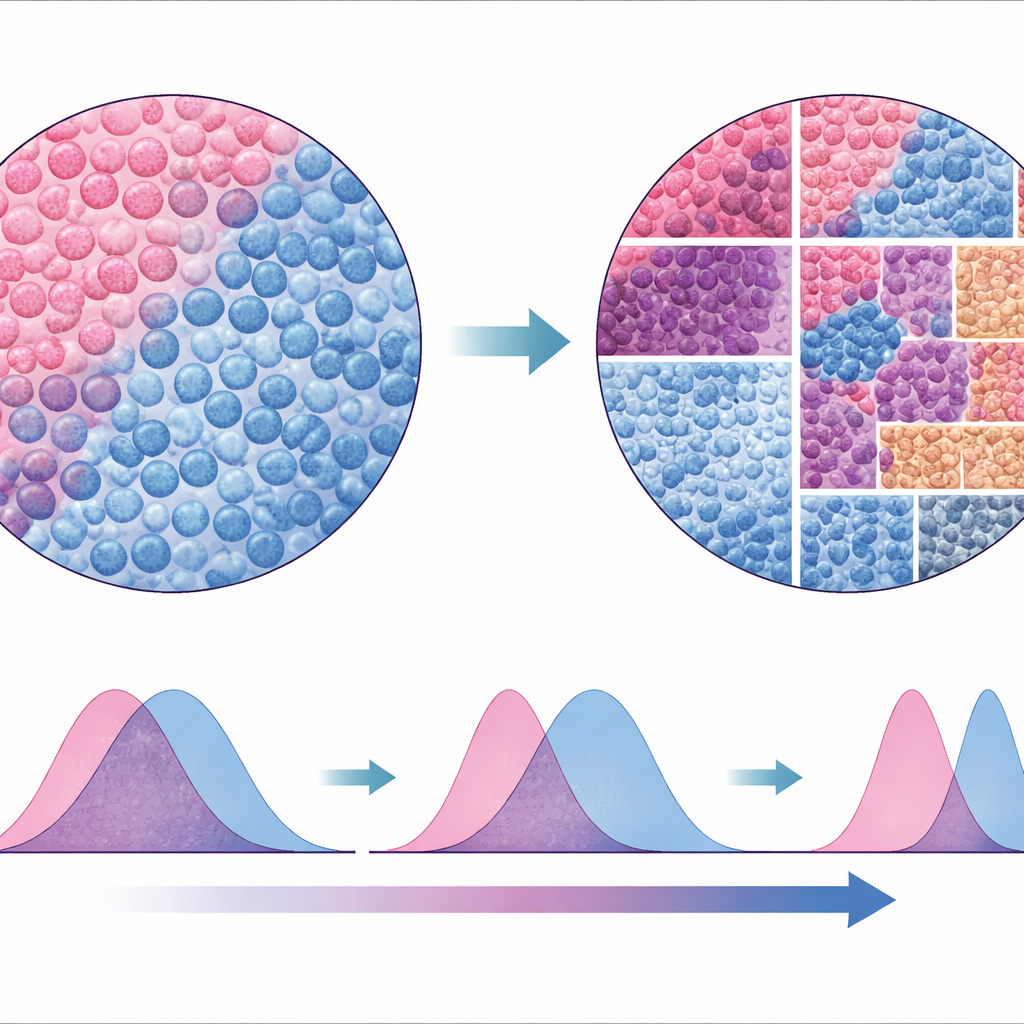
Nowy sposób odczytywania krajobrazu guza
Aby sprawdzić, jak odporne jest ich podejście, autorzy porównali SparTile z tradycyjnymi metodami opartymi na segmentacji i klasyfikacji pojedynczych komórek, a następnie budowaniu wokół nich sąsiedztw. Analizy oparte na komórkach odtworzyły niektóre z tych samych wzorców, ale były mniej spójne między zestawami danych i mniej wiarygodne przy wskazywaniu pewnych ryzykownych mikrośrodowisk, takich jak te związane z MX1 i komórkami mieloidalnymi. Ponieważ SparTile działa bezpośrednio na surowych obrazach białkowych, omija wiele założeń i technicznych pułapek metod komórka po komórce, a jednocześnie można je później łączyć z analizami komórkowymi, gdy potrzebne są szczegółowe typy komórek do planowania eksperymentów lub terapii.
Co to oznacza dla pacjentów i przyszłej opieki
Praca ta pokazuje, że nie tylko składniki, ale i układ guza mają znaczenie przy przewidywaniu losu pacjenta z rakiem piersi potrójnie ujemnym. Przekształcając złożone, wielobiałkowe obrazy w interpretowalne wzorce przestrzenne i proste miary odległości, SparTile oferuje sposób wykrywania pacjentów wysokiego ryzyka na podstawie małych próbek tkanki oraz odkrywania biologicznych układów, które mogłyby być celami przyszłych terapii. Choć potrzeba dalszej walidacji, zanim metoda będzie mogła kierować rutynową opieką, podejście wskazuje na przyszłość, w której „mapa” guza stanie się równie ważna jak jego lista molekularnych składników.
Cytowanie: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Słowa kluczowe: rak piersi potrójnie ujemny, mikrośrodowisko guza, przestrzenna proteomika, obrazowanie z użyciem cytometrii mas, biomarkery prognostyczne