Clear Sky Science · pl
IdentifiHR przewiduje niedobór homologicznej rekombinacji w wysokogatunkowym surowiczym raku jajnika na podstawie ekspresji genów
Dlaczego te badania mają znaczenie dla pacjentek z rakiem jajnika
Dla osób z wysokogatunkowym surowiczym rakiem jajnika — jedną z najgroźniejszych postaci tego nowotworu — wybór terapii może decydować o życiu lub śmierci. Około połowa tych guzów ma defekt w mechanizmach naprawy DNA, co czyni je szczególnie wrażliwymi na leki z grupy inhibitorów PARP. Wyzwanie polega na ustaleniu, u której pacjentki guz rzeczywiście ma taką podatność. W tym badaniu przedstawiono IdentifiHR, nowe narzędzie, które analizuje wzorce aktywności genów, zamiast polegać wyłącznie na mutacjach DNA, aby przewidzieć, które guzy mają uszkodzoną naprawę DNA i mogą najbardziej skorzystać z tych ukierunkowanych terapii.
Od śladów w DNA do wzorców aktywności genów
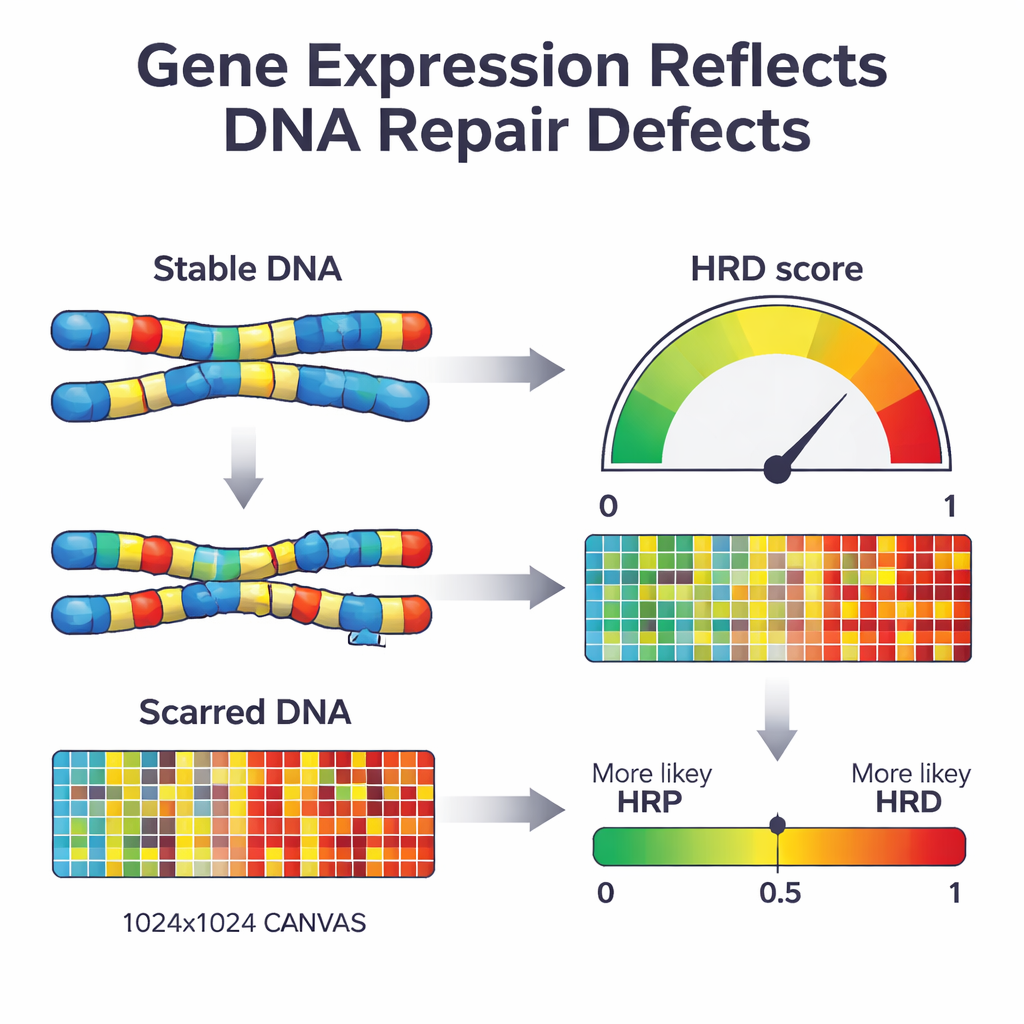
Gdy komórka traci główną ścieżkę naprawczą zwaną homologiczna rekombinacją, zaczyna naprawiać DNA przy użyciu bardziej niedokładnych mechanizmów. Z czasem pozostawia to charakterystyczne „blizny” w genomie — brakujące fragmenty, dodatkowe kopie i złamane segmenty chromosomów. Istniejące testy kliniczne szukają tych śladów bezpośrednio w DNA lub konkretnych mutacji w kluczowych genach, takich jak BRCA1 i BRCA2. Choć są one skuteczne, wymagają rozległego sekwencjonowania DNA i nie zawsze odzwierciedlają aktualny stan naprawy w guzie. Autorzy zastanawiali się, czy inna warstwa biologii — wzorzec genów włączonych i wyłączonych w guzie — mogłaby służyć jako bieżący wskaźnik tych uszkodzeń i być użyta do klasyfikacji guzów jako naprawa-niewydolna lub naprawa-sprawna.
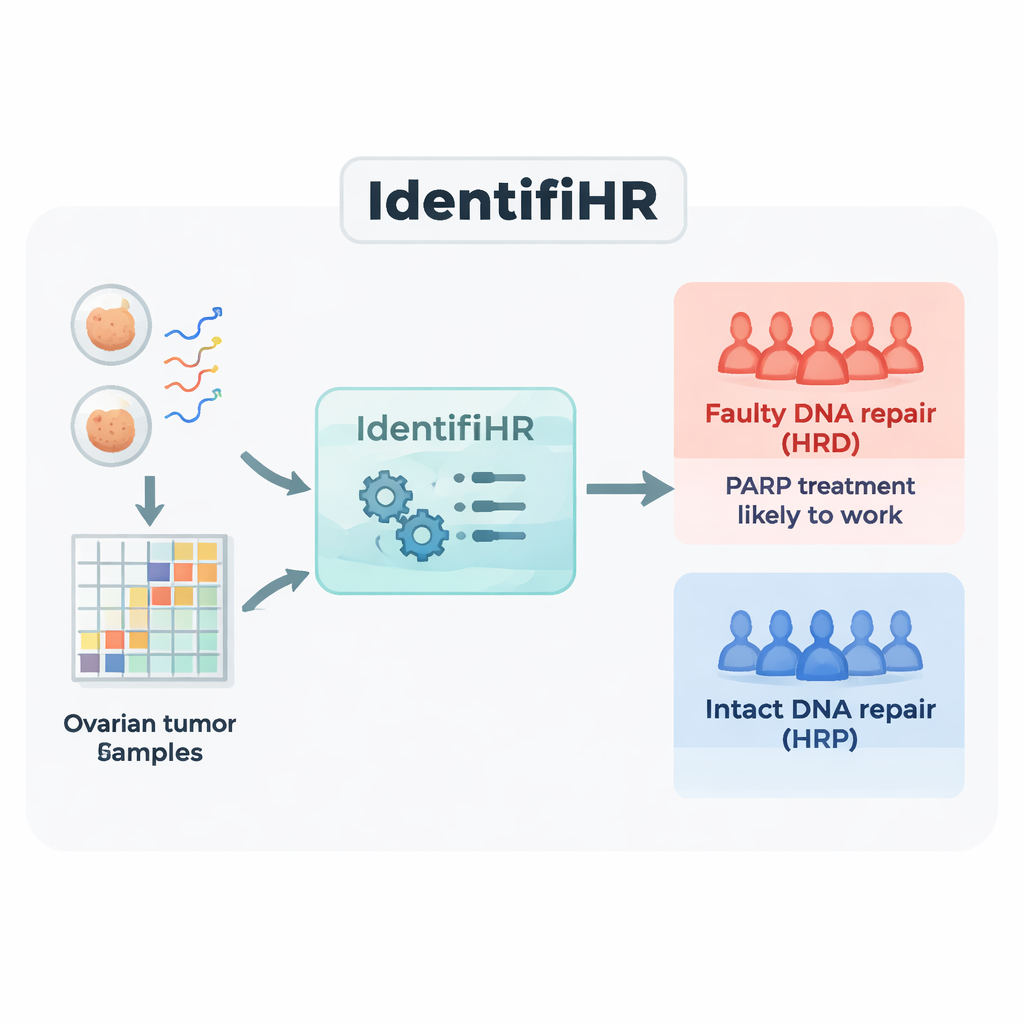
Budowa predyktora opartego na genach, IdentifiHR
Zespół rozpoczął analizę od danych z sekwencjonowania RNA pochodzących z 361 guzów jajnika z dużego publicznego zasobu, The Cancer Genome Atlas. Sekwencjonowanie RNA mierzy, które geny są aktywne i w jakim stopniu w każdej próbce. Guzy podzielono na grupę treningową i testową, oznaczając każdy przypadek jako defekt naprawy (HRD) lub prawidłową naprawę (HRP) według obecnego standardu opartego na DNA, który łączy kilka miar blizn genomowych. W guzach z grupy treningowej zidentyfikowano 2 604 geny, których aktywność konsekwentnie różniła się między nowotworami HRD i HRP. Wiele z tych genów znajdowało się w regionach genomu już wcześniej znanych z częstych zysków lub strat w guzach z defektem naprawy, co sugeruje, że sygnał ekspresji genów odzwierciedla leżące u podstaw uszkodzenia DNA.
Sygnatura 209 genów śledząca stan naprawy
Następnie badacze zastosowali podejście uczenia maszynowego znane jako karana regresja logistyczna, aby skompresować listę 2 604 genów do najbardziej informatywnego zbioru. Otrzymany model, nazwany IdentifiHR, opiera się na aktywności zaledwie 209 genów, aby oszacować, jak prawdopodobne jest, że guz ma defekt naprawy. Co ciekawe, tylko jeden z tych genów jest klasycznym genem naprawy DNA; większość stanowią zwykłe geny, których aktywność zmienia się w wyniku szerszych zmian w strukturze chromosomów. IdentifiHR nie zwraca jedynie etykiety tak/nie — generuje wynik w postaci prawdopodobieństwa, który gładko koreluje z opartym na DNA wynikiem uszkodzeń, odzwierciedlając ideę, że niedobór naprawy występuje na kontinuum, a nie jako stan zero-jedynkowy.
Testowanie narzędzia w wielu kohortach pacjentek
Autorzy rygorystycznie przetestowali IdentifiHR w trzech niezależnych zbiorach danych, które nie były używane podczas treningu. W wyodrębnionej części The Cancer Genome Atlas model poprawnie rozróżniał guzy HRD od HRP w około 85% przypadków. Uzyskał podobną skuteczność — około 86% dokładności — w odrębnym australijskim badaniu, które obejmowało nie tylko guzy pierwotne, lecz także próbki pobrane podczas autopsji, z płynu w jamie brzusznej (ascites) oraz z normalnych jajowodów, będących prawdopodobnym miejscem powstawania wielu tych nowotworów. We wszystkich próbkach zdrowego jajowodu IdentifiHR poprawnie przewidział nienaruszoną naprawę DNA. Narzędzie działało także na tzw. pseudobulkowanych danych pojedynczych komórek, gdzie tysiące pojedynczych komórek nowotworowych zostało łączonych obliczeniowo, aby naśladować próbkę zbiorczą, osiągając ponownie około 84% dokładności. We wszystkich tych testach IdentifiHR dorównywał lub przewyższał wyniki kilku istniejących metod opartych na ekspresji genów, pierwotnie opracowanych dla innych nowotworów lub do przewidywania powiązanych wskaźników uszkodzeń.
Jak to może zmienić badania i opiekę
Ponieważ IdentifiHR działa na danych RNA, które są często tańsze i łatwiejsze do pozyskania niż profile całego genomu DNA, oferuje praktyczny sposób dla badaczy — a potencjalnie w przyszłości także klinicystów — na oszacowanie stanu naprawy DNA, gdy dostępne są jedynie dane o ekspresji genów. Model udostępniono jako otwartoźródłowy pakiet w R, więc każda grupa dysponująca odpowiednimi danymi sekwencyjnymi może go zastosować. Choć nie zastępuje jeszcze testów DNA uznawanych za złoty standard, a jego zdolność do wykrywania subtelniejszych zmian, takich jak przywrócenie naprawy, wymaga dalszych badań, IdentifiHR dostarcza potężnej, nowej perspektywy na to, które guzy jajnika najprawdopodobniej zareagują na inhibitory PARP i podobne leki. Dla pacjentek ta linia badań przybliża medycynę do bardziej precyzyjnych, opartych na biologii decyzji terapeutycznych, dopasowanych do rzeczywistego zachowania komórek nowotworowych.
Cytowanie: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Słowa kluczowe: rak jajnika, naprawa DNA, niedobór homologicznej rekombinacji, ekspresja genów, uczenie maszynowe