Clear Sky Science · pl
Niedobór homologicznej rekombinacji w pierwotnym raku piersi z receptorem estrogenowym dodatnim i HER2-ujemnym
Dlaczego to ma znaczenie dla pacjentek z rakiem piersi
Większość raków piersi należy do dużej grupy określanej jako receptor estrogenowy dodatni i HER2-ujemny. Guzy te zwykle leczy się lekami blokującymi hormony, czasem w połączeniu z chemioterapią. Mimo to wiele pacjentek i tak doświadcza nawrotu choroby, a lekarzom brakuje precyzyjnych narzędzi, by zdecydować, kto rzeczywiście potrzebuje intensywnego leczenia lub mógłby skorzystać z nowych leków celowanych. Badanie to analizuje specyficzną słabość niektórych guzów — zwaną niedoborem homologicznej rekombinacji (HRD) — która utrudnia komórkom nowotworowym naprawę uszkodzonego DNA, co potencjalnie otwiera drogę do bardziej spersonalizowanego leczenia.
Ukryta słabość występująca tylko w części guzów
Homologiczna rekombinacja jest jednym z głównych systemów komórkowych naprawiających niebezpieczne przerwania DNA. Gdy ten system zawodzi — często z powodu wad w dobrze znanych genach, takich jak BRCA1, BRCA2, PALB2 czy RAD51C — komórki gromadzą mutacje i mogą stać się szczególnie wrażliwe na pewne leki, w tym chemioterapeutyki z platyny oraz inhibitory PARP. HRD jest powszechny w agresywnej postaci raka piersi zwanej potrójnie ujemną, ale jego rola w częstszej grupie receptor estrogenowy dodatni, HER2-ujemny była niepewna. Aby to wyjaśnić, naukowcy przeanalizowali 502 takie guzy z badania SCAN-B w Szwecji, używając sekwencjonowania całego genomu oraz dopasowanych danych o aktywności genów, metylacji DNA, zastosowanych terapiach i długoterminowych wynikach klinicznych.
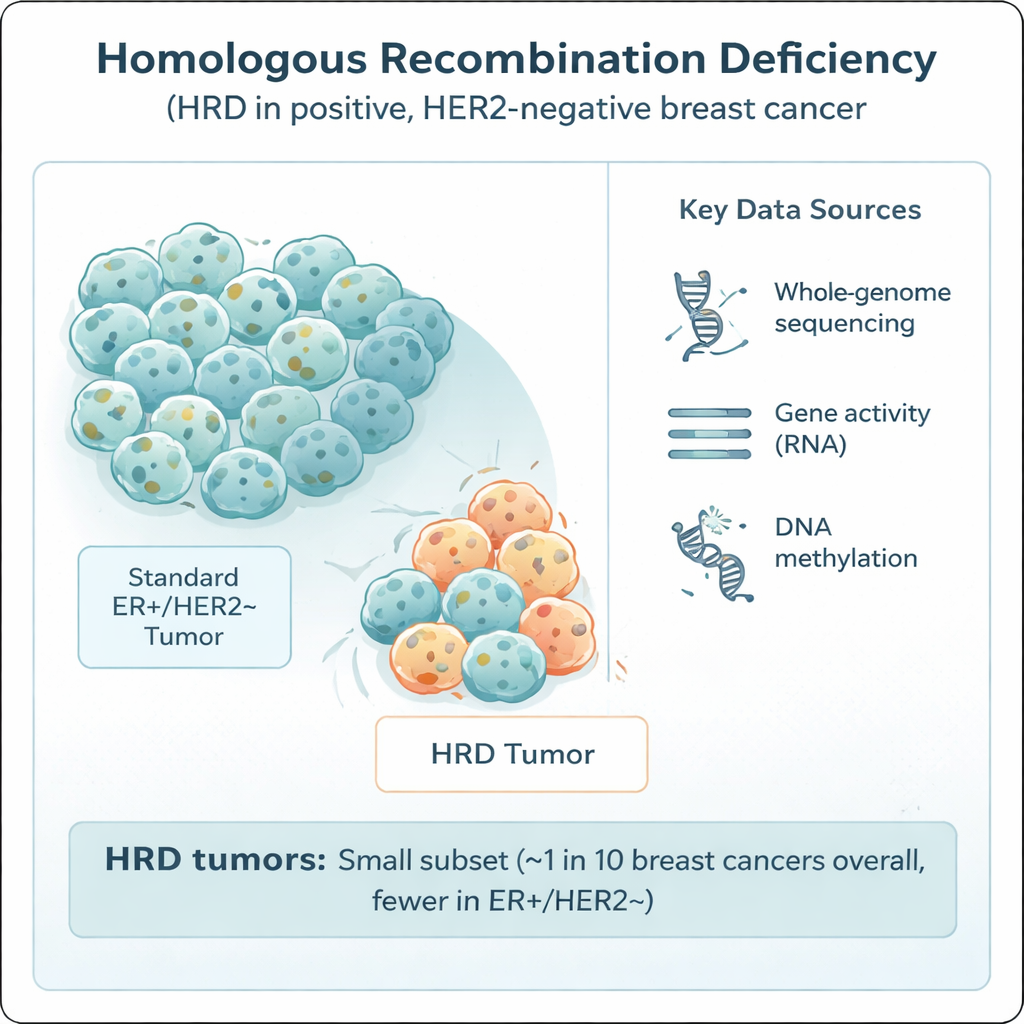
Jak przeprowadzono badanie
Wszystkie guzy pobrano podczas operacji, przed jakimkolwiek leczeniem farmakologicznym, co dało wyraźny obraz ich pierwotnej biologii. Zespół zastosował zaawansowane narzędzie do rozpoznawania wzorców, HRDetect, aby odczytać „sygnatury mutacyjne” pozostawione w DNA nowotworu, gdy homologiczna rekombinacja zawodzi. Guzy oznaczono jako HRD, jeśli przekroczyły rygorystyczny próg prawdopodobieństwa. Naukowcy porównali też różne metody wykrywania HRD — od innych wskaźników opartych na DNA po test ekspresji genów oparty na RNA — aby sprawdzić, jak wiarygodnie różne podejścia się zgadzają. Dodatkowo zbadali szersze cechy, takie jak całkowite obciążenie mutacjami, wzorce zysków i strat chromosomalnych, aktywność genów związanych z układem odpornościowym oraz chemiczne oznaczenia na DNA (metylacja), które mogą wyłączać geny.
Jak często występuje HRD i co je powoduje?
Naukowcy stwierdzili, że tylko 8,4% guzów receptor estrogenowy dodatnich i HER2-ujemnych w sekwencjonowanej grupie wykazywało silne dowody HRD — znacznie mniej niż około 60% obserwowanych w chorobie potrójnie ujemnej. Łącząc te dane z rejestrami krajowymi i innymi badaniami, oszacowali, że około 1 na 20 guzów w tej podgrupie klinicznej, a około 1 na 9 raków piersi ogółem w populacjach Europy Zachodniej/Skandynawii, wykazuje HRD. W guzach HRD często udawało się wskazać prawdopodobną przyczynę: około 70% miało wyraźne uszkodzenia BRCA1, BRCA2, RAD51C lub PALB2 — poprzez mutacje dziedziczne, zmiany specyficzne dla guza lub delecje, albo epigenetyczne wyciszenie promotorów genów. Uderzająco, około jedna trzecia przypadków HRD wynikała z hipermetylacji promotorów — dodatkowej chemicznej powłoki wyłączającej geny naprawy DNA bez zmiany ich sekwencji. Jednak około 30% guzów HRD nie wykazywało oczywistej pojedynczej przyczyny, co sugeruje istnienie dodatkowych, jeszcze nieodkrytych dróg prowadzących do tej awarii naprawy.
Jak guzy HRD wyglądają w mikroskopie i w praktyce klinicznej
Guzy HRD w tej powszechnej grupie raka piersi wykazywały cechy bardziej agresywnej choroby: często miały wyższe tempo podziałów komórkowych, niższe poziomy barwienia receptorów hormonalnych oraz bardziej złożone, bogate w mutacje genomy niż guzy z funkcjonalną naprawą homologicznej rekombinacji. Występowały w niemal wszystkich głównych podtypach molekularnych, ale były rzadkie w bardziej łagodnej klasie Luminal A i stosunkowo wzbogacone w mniejszym podzbiorze o cechach podobnych do typu basalnego. Jednak gdy badacze przyjrzeli się całkowitej aktywności genów i wzorcom metylacji DNA, guzy HRD nie tworzyły jednorodnego, łatwo rozpoznawalnego profilu. Ich wzorce ekspresji były zróżnicowane, a różnice w obrębie konkretnych podtypów były skromne. Niektóre guzy HRD, zwłaszcza w grupach Luminal B i typu basalnego, wykazywały wyższe sygnały aktywności immunologicznej i zwiększoną ekspresję PD-L1, co sugeruje, że mogą być bardziej widoczne dla układu odpornościowego i potencjalnie bardziej podatne na immunoterapię.
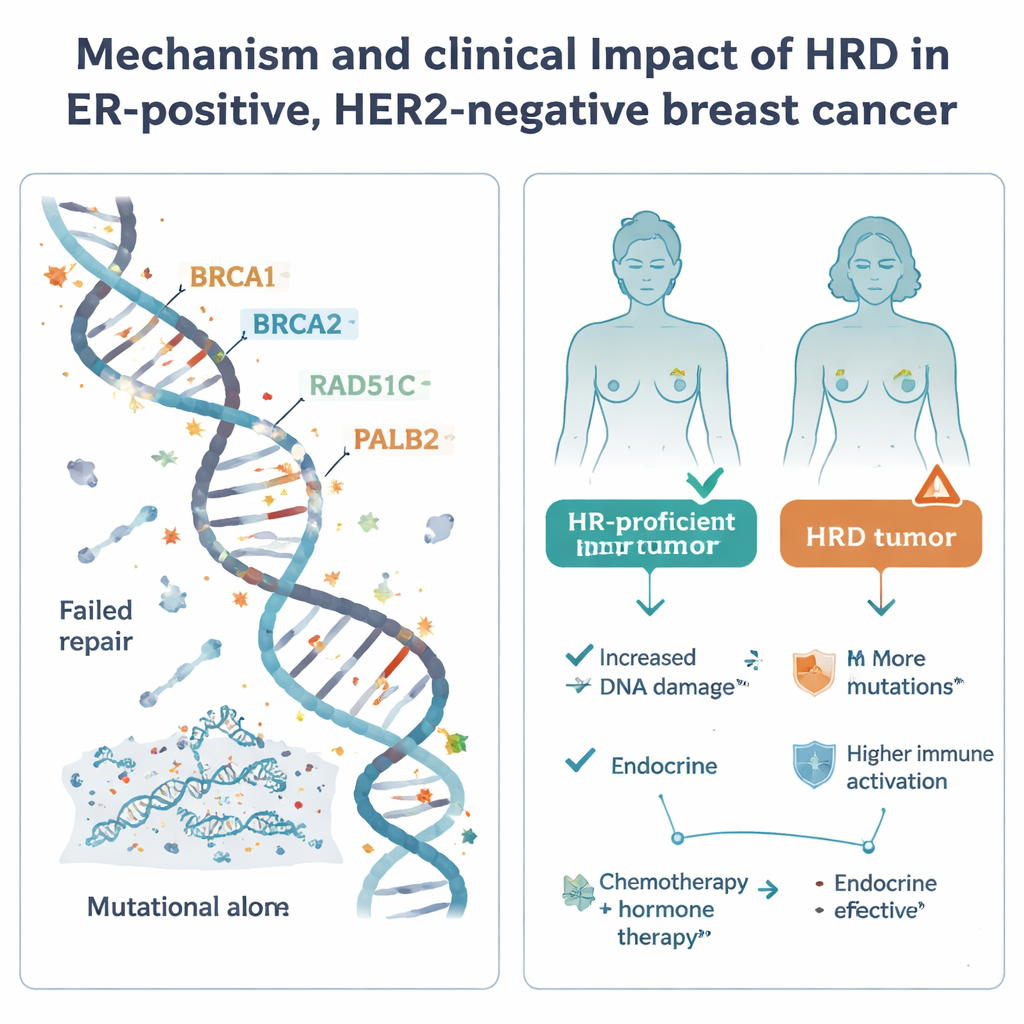
Czy HRD wpływa na wyniki leczenia pacjentek?
Następnie badanie przeanalizowało, jak status HRD wiązał się z rzeczywistymi wynikami przy standardowej opiece. U pacjentek leczonych wyłącznie terapią hormonalną po operacji guzy HRD wykazywały tendencję do gorszego przeżycia wolnego od odległych nawrotów, chociaż liczba przypadków HRD była mała i wynik nie osiągnął formalnej istotności statystycznej. Ten wzorzec, wraz z ich agresywnymi cechami molekularnymi, sugeruje, że poleganie jedynie na terapii hormonalnej może być ryzykowne dla pacjentek z guzami HRD. W przeciwieństwie do tego, wśród pacjentek otrzymujących chemioterapię i terapię hormonalną, status HRD nie był wyraźnie związany z lepszym ani gorszym wynikiem; wszystkie grupy miały w przybliżeniu podobne wskaźniki nawrotów, a chemioterapia może łagodzić część zwiększonego ryzyka w guzach HRD.
Co to oznacza dla przyszłych wyborów terapeutycznych
Dla czytelnika ogólnego kluczowe przesłanie jest takie, że tylko mniejszość raków piersi receptor estrogenowy dodatni, HER2-ujemnych ma tę specyficzną słabość w naprawie DNA, ale jeśli jest obecna, zwykle wskazuje na bardziej agresywną chorobę, która może nie być dobrze kontrolowana samą terapią hormonalną. Praca wspiera pogląd, że sekwencjonowanie całego genomu może wiarygodnie wskazać HRD i wyjaśnić jego przyczyny, wykraczając poza samo badanie mutacji dziedzicznych BRCA1 lub BRCA2. Chociaż badanie nie dowodzi jeszcze, że zmiana leczenia na podstawie statusu HRD poprawia przeżycie, dostarcza wczesnych dowodów, że pacjentki z guzami HRD mogą odnieść korzyść z chemioterapii, a w przyszłych badaniach klinicznych — z inhibitorów PARP lub immunoterapii. Krótko mówiąc, testowanie HRD mogłoby stać się jednym z elementów bardziej wysublimowanego zestawu narzędzi do dopasowywania intensywności terapii — i nowych opcji celowanych — do biologii guza każdej pacjentki z rakiem piersi.
Cytowanie: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Słowa kluczowe: rak piersi, naprawa DNA, geny BRCA, sekwencjonowanie genomu, terapia celowana