Clear Sky Science · pl
Powierzchniowo modyfikowane, dwuskładnikowe liposomowe nanocząstki ukierunkowane na guz w celu przezwyciężenia oporności terapeutycznej w glejakach wielopostaciowych
Dlaczego to badanie nad rakiem mózgu ma znaczenie
Glejak to jedna z najbardziej śmiertelnych postaci nowotworu mózgu. Nawet przy zastosowaniu operacji, radioterapii i chemioterapii większość pacjentów przeżywa zaledwie nieco ponad rok od rozpoznania. Głównym problemem jest to, że standardowe leki często nie docierają do guza w mózgu, a jeśli już dotrą, guz szybko adaptuje się i rozwija oporność. W pracy tej badano nową metodę przemycania wielu leków przez naturalne bariery mózgu i ich koncentracji wewnątrz guza, z celem istotnego zwiększenia skuteczności istniejących terapii, takich jak radioterapia.
Maleńka ciężarówka dostarczająca leki przeciwnowotworowe
Naukowcy skonstruowali ultramałe nośniki leków zwane liposomami ukierunkowanymi na guz. To miękkie, lipidowe pęcherzyki w skali miliardowych części metra, które mogą pomieścić leki wewnątrz. Zespół zmodyfikował powierzchnię tych pęcherzyków specjalnym peptydem, który rozpoznaje i przyczepia się do komórek glejaka, pomagając cząstkom lokalizować guzy zamiast zdrowej tkanki. Każdy pęcherzyk zaprojektowano tak, aby jednocześnie przenosił parę leków przeciwnowotworowych: albo everolimus i winorelbina, albo rapamycynę i winorelbina. Pomysł polega na tym, że dwa leki atakują komórki guza komplementarnie, podczas gdy ochronna powłoka pomaga lekom przetrwać w krwiobiegu i przeniknąć do mózgu.
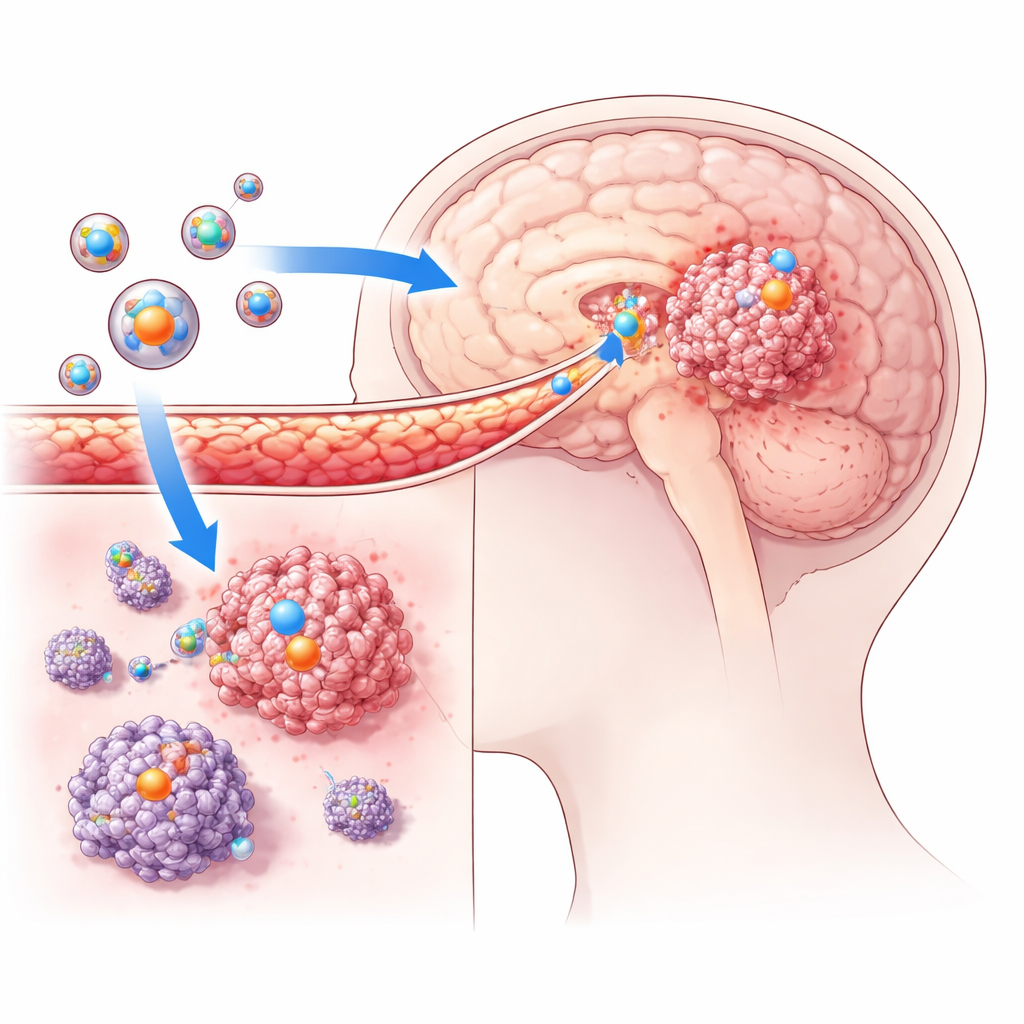
Przechodząc przez ochronną ścianę mózgu
Wykorzystując modele mysie z wszczepionymi ludzkimi komórkami glejaka, zespół sprawdził, czy te liposomy rzeczywiście mogą dotrzeć do guzów w mózgu. Oznakowali cząstki barwnikami fluorescencyjnymi i śledzili ich drogę za pomocą zaawansowanych narzędzi obrazowania. W porównaniu z liposomami bez ukierunkowania, wersje ukierunkowane na guz wykazywały znacznie silniejszy sygnał w obrębie guzów mózgu i niewielki sygnał w prawidłowych obszarach mózgu. Potwierdziło to, że zaprojektowane cząstki potrafiły przekroczyć barierę krew–mózg i kumulować się specyficznie tam, gdzie rosły komórki nowotworowe. W eksperymentach z hodowlami komórkowymi komórki glejaka również pobierały znacznie więcej liposomów ukierunkowanych niż kontrolnych, co wzmacniało przekonanie, że peptyd powierzchniowy znacząco poprawia celowanie i wnikanie do guza.
Silniejsze uderzenie w guz przy jednoczesnym oszczędzaniu reszty ciała
Naukowcy najpierw porównali, jak dobrze liposomy zawierające pojedynczy lek i liposomy zawierające dwa leki zabijają komórki nowotworowe na szalkach. Wersje z dwoma lekami, szczególnie kombinacja everolimus–winorelbina, były bardziej skuteczne niż każdy z leków osobno i działały lepiej niż te same leki podane bez nośnika liposomalnego. Po połączeniu z radioterapią efekt był jeszcze silniejszy: komórki nowotworowe tworzyły znacznie mniej kolonii, poruszały się mniej i wykazywały oznaki nasilonych uszkodzeń. W mysich guzach mózgu zwierzęta leczone liposomami z dwoma lekami plus radioterapią miały wolniejszy wzrost guza i dłuższe przeżycie niż te otrzymujące samą radioterapię, same liposomy lub standardową chemioterapię temozolomidem. Co ważne, badacze nie zaobserwowali wyraźnych uszkodzeń w innych narządach, co sugeruje, że ukierunkowanie leczenia do guza może zmniejszać skutki uboczne.
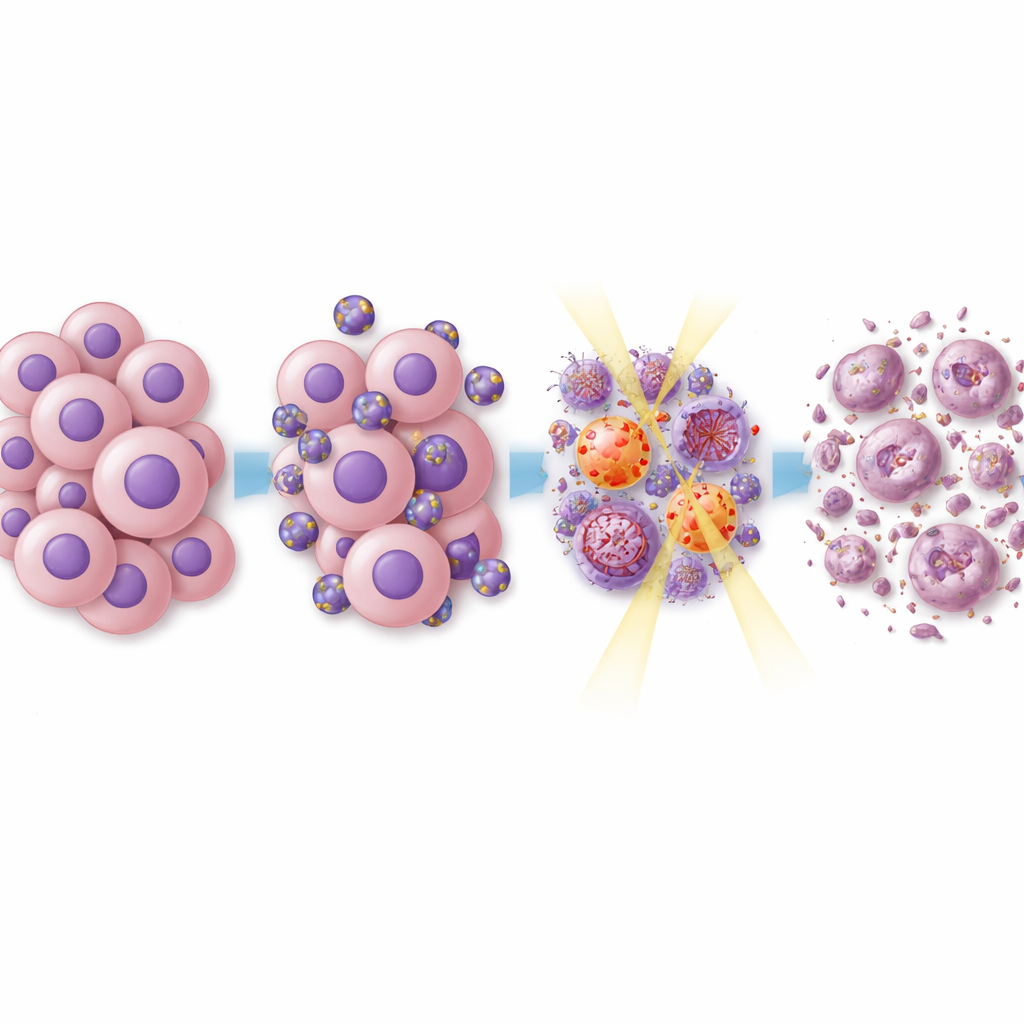
Co dzieje się wewnątrz komórek nowotworowych
Aby zrozumieć, dlaczego to podejście zwiększało wrażliwość guzów na leczenie, zespół przeanalizował kluczowe układy sygnalizacyjne w komórkach nowotworowych. Everolimus i rapamycyna są znane z blokowania szlaku mTOR, który wspiera wzrost komórek i odporność na stres. Liposomy z dwoma lekami tłumiły sygnały związane z mTOR, jak również inne szlaki wzrostu napędzające podział i migrację komórek glejaka. Po dodaniu radioterapii białka zaangażowane w naprawę uszkodzeń DNA były również osłabione. Oznacza to, że komórki guza miały mniejszą zdolność do naprawy uszkodzeń genetycznych wywołanych przez promieniowanie, co skłaniało je ku śmierci zamiast do regeneracji. Szczegółowe analizy aktywności genów w leczonych guzach wykazały szerokie zmiany w sieciach powiązanych z kontrolą cyklu komórkowego, naprawą DNA i interakcją guza z układem odpornościowym, a wiele genów związanych z opornością na leczenie zostało wyciszonych.
Co to może oznaczać dla przyszłych pacjentów
Praca ta pokazuje, że starannie zaprojektowane, celujące w guz nanopreparaty mogą przetransportować dwa współpracujące leki przez barierę ochronną mózgu, skoncentrować je wewnątrz glejaka i zwiększyć skuteczność radioterapii. U myszy ta strategia spowolniła wzrost guza i wydłużyła przeżycie bez wyraźnego wzrostu toksyczności. Chociaż wyniki te są nadal przedkliniczne i zanim metoda zostanie zastosowana u ludzi potrzebne są dalsze testy, badanie wskazuje praktyczny sposób łączenia ukierunkowanego dostarczania leków z istniejącymi terapiami, by przechytrzyć wysoce oporny nowotwór. Jeśli podobne korzyści wystąpią u ludzi, takie dwuskładnikowe liposomy mogłyby kiedyś zaoferować pacjentom z glejakiem dłuższe i lepsze życie.
Cytowanie: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
Słowa kluczowe: glejak, nanocząstki, liposomy, leczenie nowotworów mózgu, uwrażliwianie na radioterapię