Clear Sky Science · pl
Badanie 201: kontrolowane placebo, randomizowane badanie fazy 2 bezpieczeństwa i tolerancji inhibitora kinazy c‑Abl — risvodetinibu — u nieleczonej choroby Parkinsona
Dlaczego to badanie ma znaczenie dla rodzin dotkniętych chorobą Parkinsona
Choroba Parkinsona stopniowo pozbawia ludzi sprawności ruchowej i niezależności, a dostępne dziś leki głównie łagodzą objawy, nie zmieniając przebiegu choroby. W tym badaniu przetestowano nową tabletkę, risvodetinib, u osób z wczesną, nieleczoną chorobą Parkinsona, aby sprawdzić, czy jest bezpieczna i czy może zacząć oddziaływać na chorobę u jej źródeł. Zamiast jedynie maskować drżenie czy sztywność, lek ma zakłócać sygnał stresowy w komórkach nerwowych, który uważa się za czynnik prowadzący do obumierania neuronów i gromadzenia szkodliwych białek.
Nowy cel wewnątrz wrażliwych komórek mózgu
Naukowcy od dawna wiedzą, że choroba Parkinsona wiąże się z grudkami białka zwanego alfa‑synukleiną, które gromadzą się w komórkach nerwowych i rozprzestrzeniają się po układzie nerwowym. Te skupiska mogą aktywować czujnik stresu komórkowego zwany c‑Abl, który uruchamia łańcuch reakcji popychających komórki w kierunku śmierci. Risvodetinib to tabletka zaprojektowana tak, by przenikać do mózgu i selektywnie blokować c‑Abl. W modelach zwierzęcych choroby Parkinsona codzienne podawanie chroniło neurony, zmniejszało szkodliwe nagromadzenie białka i poprawiało ruch. Te obiecujące wyniki skłoniły badaczy do rozpoczęcia tzw. „Badania 201”, pierwszego dłuższego badania dawkowania risvodetinibu u ludzi.
Jak zaprojektowano Badanie 201
Do badania zrekrutowano 137 dorosłych w Stanach Zjednoczonych, u których niedawno rozpoznano chorobę Parkinsona i którzy nie rozpoczęli jeszcze standardowego leczenia przeciwparkinsonowskiego. Uczestnicy zostali losowo przydzieleni do otrzymywania jednej z trzech dziennych dawek risvodetinibu (50, 100 lub 200 miligramów) albo placebo przez 12 tygodni, a następnie wykonano dwutygodniowy okres obserwacji pod kątem bezpieczeństwa. Ani uczestnicy, ani lekarze nie wiedzieli, kto otrzymywał lek aktywny. Głównym celem nie było udowodnienie korzyści w zakresie objawów, lecz uważne monitorowanie działań niepożądanych, poważnych zdarzeń medycznych oraz liczby osób, które były w stanie przyjmować lek przez pełen okres.
Bezpieczeństwo, skutki uboczne i funkcjonowanie dnia codziennego
Risvodetinib przeszedł tę pierwszą próbę bezpieczeństwa. Około 95% osób, które przystąpiły po krótkiej przerwie regulacyjnej, ukończyło 12‑tygodniowy okres leczenia, z niemal doskonałą zgodnością w przyjmowaniu tabletek. Liczba osób zgłaszających co najmniej jeden nowy problem medyczny była podobna w grupach risvodetinibu i placebo, i nie odnotowano zgonów. Poważne zdarzenia, takie jak infekcje czy urazy wymagające hospitalizacji, były rzadkie i ocenione jako niezwiązane z lekiem badanym. Skutki uboczne często obserwowane przy innych lekach z tej szerokiej grupy, takie jak obciążenie serca, znaczne obrzęki czy uszkodzenia oczu, były minimalne lub nie występowały. Ogólnie rzecz biorąc, risvodetinib okazał się zaskakująco łagodny jak na lek oddziałujący na silny enzym sygnałowy.
Ponieważ badanie było krótkie i stosunkowo niewielkie, nie oczekiwano, że wykaże wyraźną poprawę kliniczną. Rzeczywiście, standardowe skale oceniające ruch i codzienne czynności zmieniły się nieznacznie w ciągu 12 tygodni, a główny łączony wynik ruchowy nie różnił się istotnie między risvodetinibem a placebo. Kilka miar wykazało niewielkie, „nominalne” poprawy przy niektórych dawkach, na przykład skromne polepszenia w samoocenie codziennych czynności, ale sygnały te są zbyt słabe i krótkotrwałe, by uznać je za dowód, że lek łagodzi objawy. Co ważne, risvodetinib nie wydawał się ogólnie pogarszać cech ruchowych ani niemotorycznych.
Wgląd w proces chorobowy przez skórę
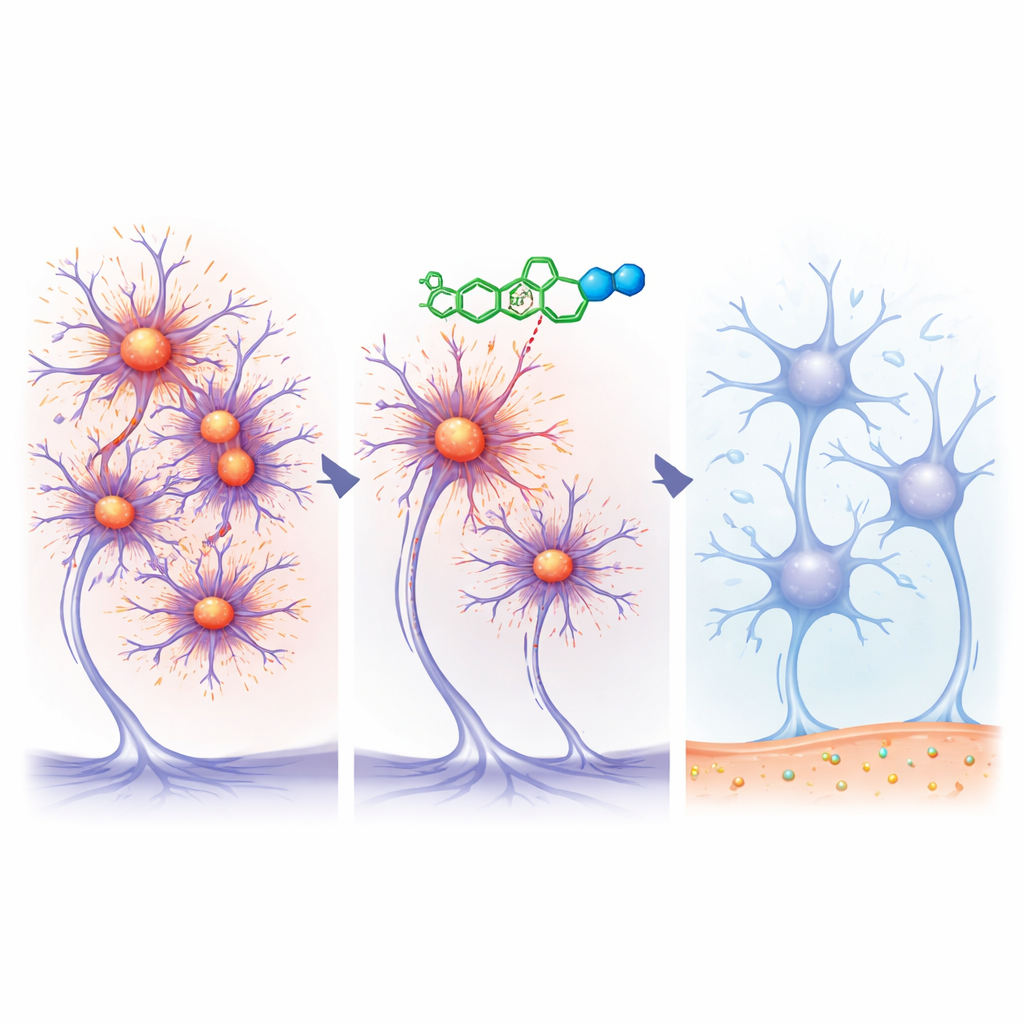
Aby zajrzeć poza objawy, zespół wykorzystał nietypowe okno na chorobę: drobne biopsje skóry. Włókna nerwowe w skórze osób z chorobą Parkinsona także mogą gromadzić nieprawidłową alfa‑synukleinę, którą można uwidocznić mikroskopią fluorescencyjną. Około 40% uczestników zgodziło się na powtarzane pobrania skóry, a 36 osób miało użyteczne tkanki zarówno przed, jak i po leczeniu. W grupie placebo wielu uczestników wykazywało niezmienione lub rosnące poziomy złogów białkowych w ciągu 12 tygodni, choć u nielicznych obserwowano spontaniczne spadki. Wśród przyjmujących risvodetinib przyrosty złogów występowały rzadziej, a odsetek osób z zmniejszonymi złogami rósł wraz z wyższymi dawkami, osiągając około dwóch trzecich w grupie o najwyższej dawce. Jednak grupy były małe, a różnice nie osiągnęły standardowych progów statystycznych, więc wyniki są raczej sugestywne niż rozstrzygające.
Co to oznacza dla przyszłości leczenia
Badanie 201 pokazuje, że hamowanie c‑Abl za pomocą risvodetinibu można przeprowadzić bezpiecznie przez co najmniej trzy miesiące u osób z wczesną chorobą Parkinsona, przy stężeniach leku znacznie wyższych niż stosowane w niektórych istniejących lekach przeciwnowotworowych oddziałujących na tę samą ścieżkę. Wstępne wyniki z biopsji skóry sugerują, że lek może wpływać na podstawowy proces chorobowy, pomagając komórkom nerwowym usuwać szkodliwe nagromadzenia białka, ale potrzebne są silniejsze, dłuższe badania, aby to potwierdzić i ustalić, czy takie zmiany przekładają się na spowolnienie postępu objawów. Na razie badanie nie twierdzi, że risvodetinib poprawia samopoczucie czy funkcjonowanie ludzi — jedynie że wydaje się na tyle bezpieczny, by uzasadniać kolejny krok: większe, dłuższe badania sprawdzające, czy rzeczywiście może zmienić bieg choroby Parkinsona.
Cytowanie: Werner, M.H., McGarry, A., Meyer, C. et al. The 201 Trial: a placebo-controlled randomized phase 2 study of safety and tolerance of the c-Abl kinase inhibitor risvodetinib in untreated Parkinson’s disease. Nat Aging 6, 626–635 (2026). https://doi.org/10.1038/s43587-026-01084-4
Słowa kluczowe: choroba Parkinsona, neuroprotekcja, badanie kliniczne, agregacja białek, inhibitor kinazy tyrozynowej