Clear Sky Science · pl
Strukturalny znak białek surowicy klasyfikuje stadium choroby Alzheimera
Dlaczego test krwi na utratę pamięci ma znaczenie
Choroba Alzheimera często jest już zaawansowana daleko zanim problemy z pamięcią staną się oczywiste, ale obecne testy pozwalające wykryć ją wcześnie mogą być inwazyjne, kosztowne lub trudno dostępne. W tym badaniu badacze rozważają inną koncepcję: czy drobne zmiany w trójwymiarowych kształtach białek krążących we krwi mogą ujawniać, na jakim etapie znajdują się osoby — od zdrowego starzenia przez łagodne zaburzenia pamięci do pełnoobjawowej choroby Alzheimera. Jeśli pomysł się sprawdzi, taki test krwi mógłby uprościć przesiew, wspierać wcześniejsze leczenie i pomagać naukowcom śledzić, kto odnosi korzyść z nowych terapii.
Badanie kształtu białek, a nie tylko ich ilości
Większość badań krwi ocenia, ile danej cząsteczki jest obecne. Tutaj naukowcy skoncentrowali się zamiast tego na kształcie białek. W naszych komórkach system kontroli jakości dba o prawidłowe fałdowanie białek; gdy ten mechanizm słabnie z wiekiem, niesprawne białka mogą się gromadzić i uszkadzać komórki mózgu. Zespół zastanawiał się, czy ten rozpad „porządku białkowego” pozostawia strukturalny odcisk w białkach we krwi. Od 520 ochotników — będących albo poznawczo zdrowymi, albo z łagodnymi zaburzeniami poznawczymi (MCI), albo z chorobą Alzheimera — pobrano krew i zastosowano technikę chemiczną zwaną kowalencyjnym profilowaniem białek, aby znakować odsłonięte fragmenty białek. Im bardziej odsłonięte jest miejsce, tym łatwiej je znakować, co daje numeryczny pomiar kształtu białka, w dużej mierze niezależny od ilości danego białka.
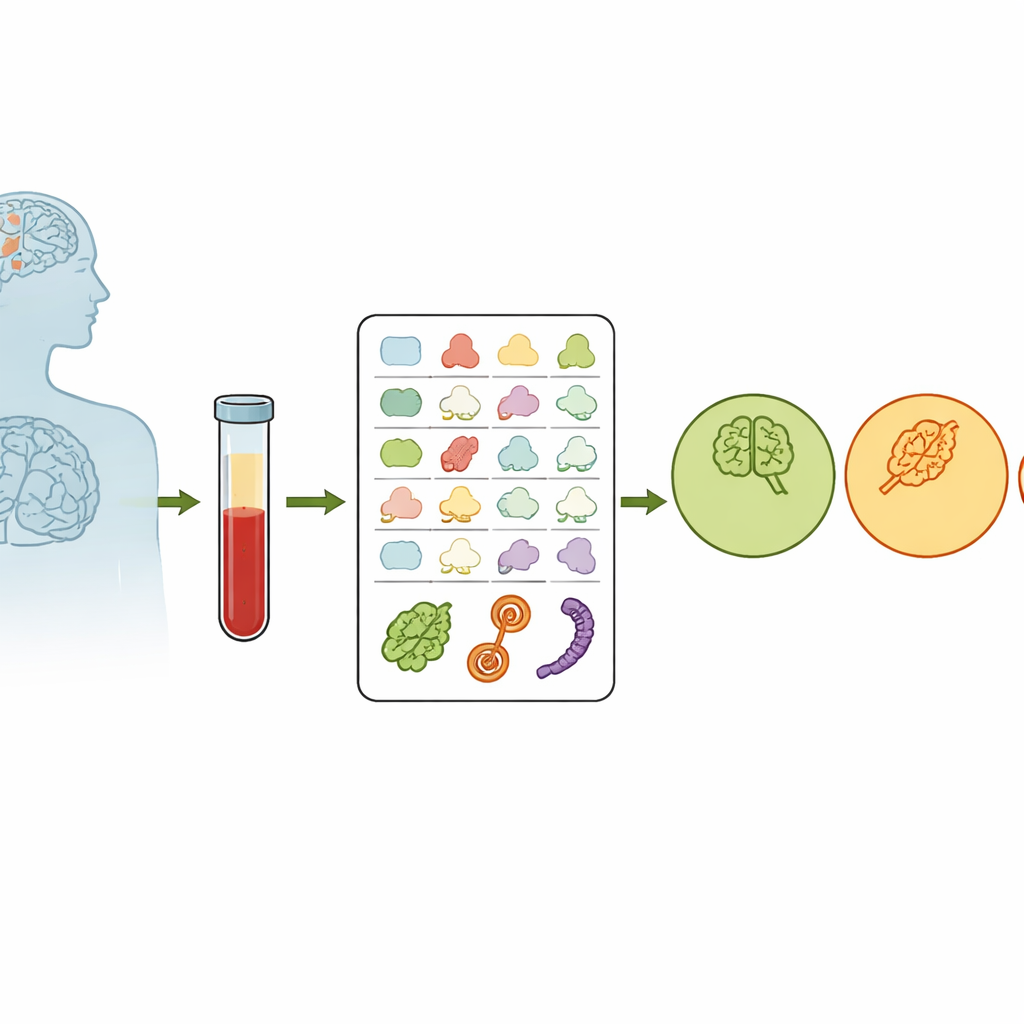
Odnajdywanie strukturalnych odcisków we krwi
Wśród prawie 900 znakowanych fragmentów białek badacze zaobserwowali subtelny, lecz spójny trend: wraz z przejściem osób od zdrowia do MCI, a następnie do Alzheimera, powierzchnie niektórych białek stawały się mniej odsłonięte i wykazywały większą zmienność między osobami. Wzorzec ten zgadza się z hipotezą, że kontrola fałdowania białek pogarsza się w miarę postępu choroby. Zespół przyjrzał się też, jak istotny genetyczny czynnik ryzyka Alzheimera, wariant APOE ε4, wpływa na kształt białek. Stwierdzili, że osoby noszące dwie kopie ε4 wykazywały charakterystyczne przesunięcia strukturalne w kilku białkach wchodzących w interakcje z białkiem APOE, co sugeruje, że ten ryzykowny wariant zmienia nie tylko to, które białka są obecne, ale także jak są złożone i ułożone.
Powiązanie białek krwi z nastrojem i zachowaniem
Choroba Alzheimera dotyka znacznie więcej niż pamięć; objawy takie jak pobudzenie, depresja i halucynacje są częste i często różnią się między kobietami i mężczyznami. Badacze połączyli kliniczne oceny 12 typów objawów neuropsychiatrycznych z pomiarami kształtu białek. U obu płci gorsze objawy zwykle współwystępowały z tym, że białka stawały się strukturalnie bardziej „zamknięte”. Niektóre białka, w tym clusterin i kilka innych powiązanych z odkładaniem amyloidu, śledziły nasilenie objawów podobnie u mężczyzn i kobiet, podczas gdy inne wykazywały wzorce specyficzne dla płci. Te obserwacje sugerują, że struktura białek we krwi może odzwierciedlać nie tylko obecność choroby, lecz także sposób, w jaki przejawia się ona w zachowaniu i nastroju.
Panel trzech białek do klasyfikacji stadium choroby
Aby przekształcić te złożone pomiary w coś użytecznego klinicznie, zespół wprowadził dane strukturalne do 18 różnych metod uczenia maszynowego. Najlepiej działający model, oparty na głębokim uczeniu, korzystał tylko z trzech fragmentów białkowych pochodzących z C1QA, clusterinu (również nazywanego CLUS) i apolipoproteiny B (ApoB). Wykorzystując tylko odczyty strukturalne z tych trzech fragmentów, model poprawnie przyporządkował osoby do grup zdrowych, MCI lub chorych na Alzheimera w około 83% przypadków w niezależnym zestawie testowym. Przy prostszych pytaniach dwuetapowych — na przykład rozróżnieniu zdrowych od MCI albo MCI od Alzheimera — wydajność panelu była jeszcze lepsza, z miarami dokładności porównywalnymi lub lepszymi niż wiele obecnych podejść opartych na ilości białek zamiast ich struktury.
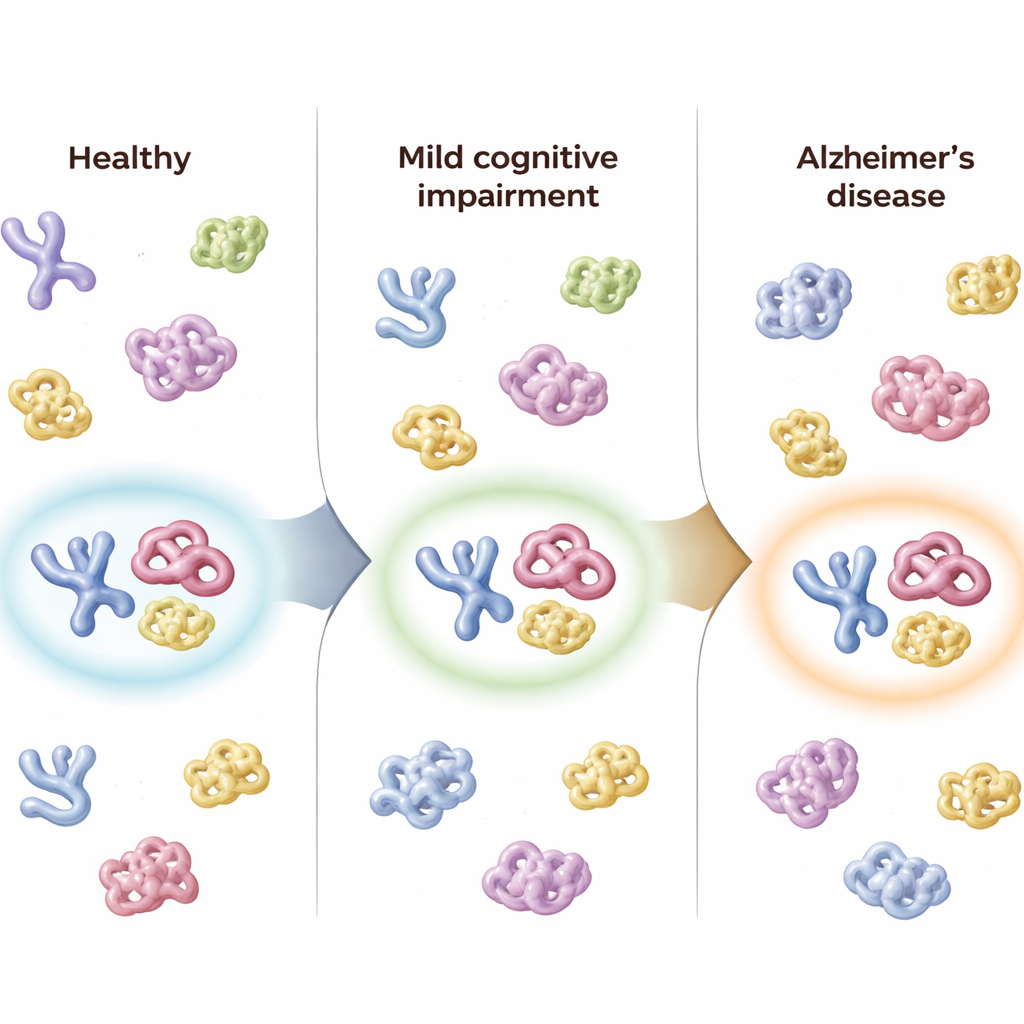
Śledzenie osób w czasie
Badacze mieli też próbki kontrolne od 50 uczestników pobrane do około ośmiu miesięcy później. U osób, których diagnoza pogorszyła się — na przykład ze stanu zdrowia do MCI lub z MCI do Alzheimera — skumulowany wynik z panelu trzech białek zmieniał się w tym samym kierunku, odzwierciedlając postęp choroby. Natomiast u osób, których stan kliniczny pozostał bez zmian, wyniki panelu wykazywały niewielkie zmiany. Ogólny wskaźnik „pewności Alzheimera” panelu dobrze korelował z standardowymi testami poznawczymi, ocenami funkcjonowania w codziennym życiu, z kurczeniem się mózgu widocznym w obrazach MRI oraz z ustalonymi markerami amyloidu i tau w płynie mózgowo-rdzeniowym, co sugeruje, że strukturalny sygnał krwi odzwierciedla leżące u podstaw zmiany mózgowe.
Co to może oznaczać dla pacjentów
Podsumowując, praca pokazuje, że niewielkie, skoordynowane zmiany w kształtach zaledwie kilku obfitych białek krwi mogą wiarygodnie sygnalizować, czy ktoś jest poznawczo zdrowy, ma łagodne upośledzenie czy choruje na Alzheimera. Ponieważ test wykorzystuje krew zamiast płynu mózgowo-rdzeniowego lub obrazowania mózgu, mógłby — w zasadzie — zostać wdrożony do rutynowego przesiewu albo do wyboru i monitorowania uczestników badań klinicznych. Autorzy zaznaczają, że potrzebne są większe i dłuższe badania, a stosowana chemia jest wciąż wyspecjalizowana. Niemniej jednak ich wyniki wskazują, że struktura białek — nie tylko ich poziomy — stanowi obiecujące nowe źródło informacji do wcześniejszego i dokładniejszego wykrywania oraz śledzenia choroby Alzheimera.
Cytowanie: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Słowa kluczowe: markery choroby Alzheimera, test krwi na demencję, zmiany w fałdowaniu białek, diagnostyka z użyciem uczenia maszynowego, clusterin i C1QA