Clear Sky Science · pl
Oporność na chemioterapię opartą na platynie w raku płuca i jajnika jest napędzana przez celowany sekretom senescentny zależny od TGFβ
Kiedy leczenie raka działa na niekorzyść
Chemioterapia oparta na platynie jest jednym z fundamentów współczesnego leczenia nowotworów, szczególnie w raku płuca i jajnika. Ma ona uszkadzać DNA guza tak silnie, żeby komórki nowotworowe nie mogły się dalej dzielić. Jednak u wielu pacjentów guzy początkowo się cofną, by potem powrócić w postaci trudniejszej do leczenia. W tym badaniu postawiono proste, lecz niepokojące pytanie: czy te same leki, które ratują życie, mogą też pomagać ocalałym komórkom nowotworowym w odbudowie? Odpowiedź, jak ustalili autorzy, kryje się w grupie uszkodzonych komórek przypominających komórki starzejące się oraz w silnych sygnałach chemicznych, które one wysyłają.
Podwójne życie starzejących się komórek nowotworowych
Chemioterapia nie działa tak samo na wszystkie komórki guza. Niektóre są natychmiast zabijane, inne zaś wchodzą w stan zwany senescencją komórkową — trwale zatrzymane w podziale, lecz nadal żywe. Komórki senescentne powiększają się i zaczynają wydzielać koktajl białek i sygnałów znany jako fenotyp wydzielniczy związany z senescencją (SASP). Na komórkach ludzkiego raka płuca i jajnika w warunkach laboratoryjnych oraz w modelach mysich badacze wykazali, że leki na bazie platyny, takie jak cisplatyna i karboplatyna, wywołują szczególnie silne komórki senescentne. Gdy świeże komórki nowotworowe były inkubowane w płynie pobranym z kultur senescentnych, rosły szybciej, migrowały chętniej i tworzyły większe, bardziej agresywne skupiska i kule niż komórki kontrolne.
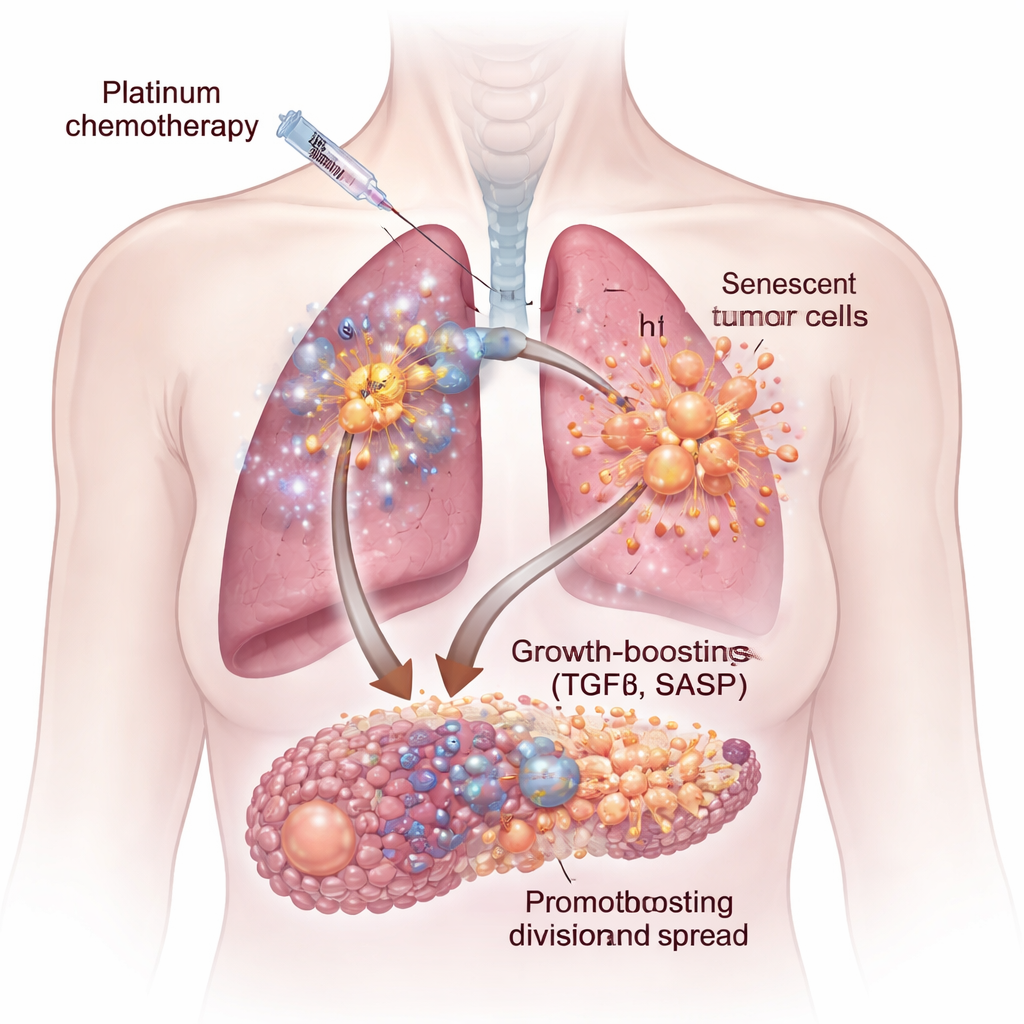
Ukryty sygnał wzrostu: TGFβ
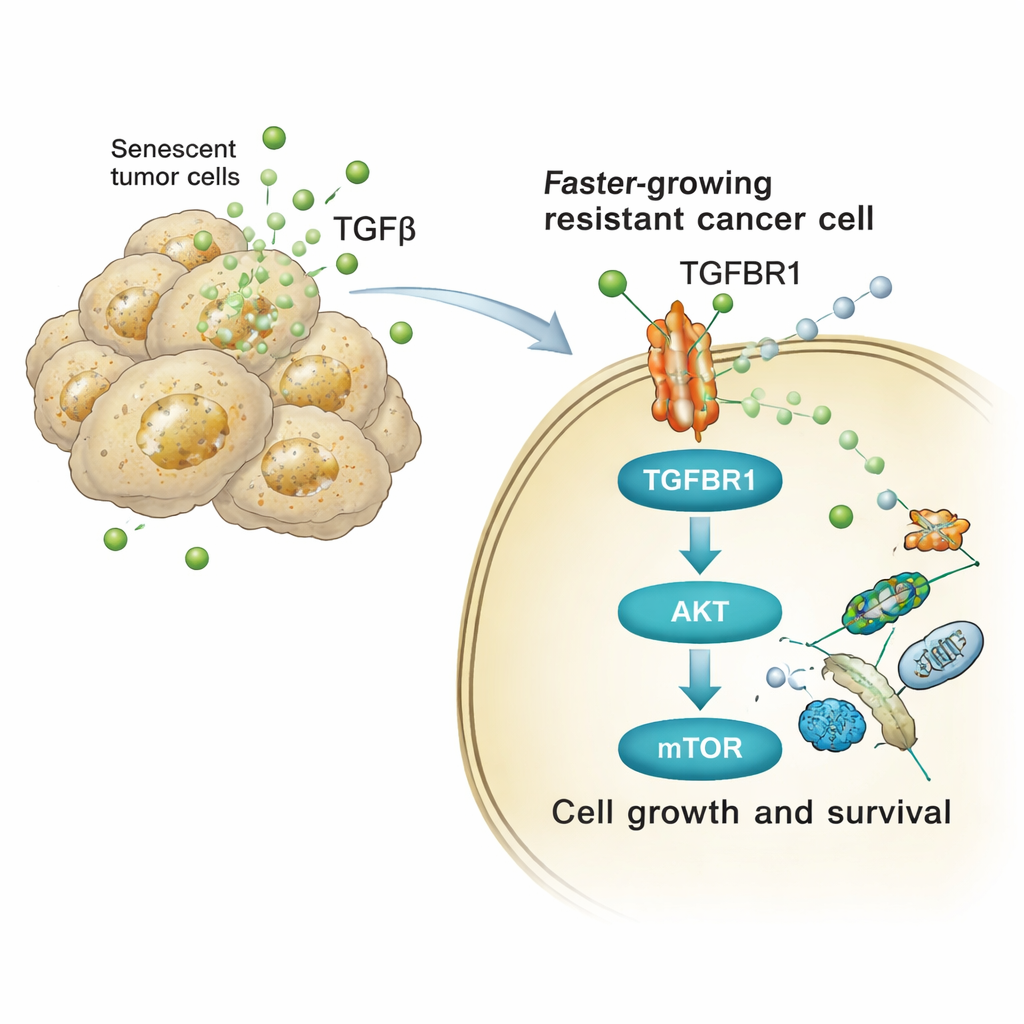
Nie wszystkie chemioterapie wywoływały te same szkodliwe wydzieliny. Porównując leki oparte na platynie z dwoma innymi powszechnymi środkami — docetakselem i palbocyklibem — tylko komórki traktowane platyną wytwarzały SASP, który silnie pobudzał wzrost guza. Łącząc badania ekspresji genów, pomiary białek i wysokoprzepustową analizę mikrośrodowiska, zidentyfikowano kluczowego sprawcę: cząsteczkę sygnałową transformujący czynnik wzrostu beta, czyli TGFβ. Komórki senescentne indukowane cisplatyną były wzbogacone w różne formy TGFβ i powiązane szlaki. Dodanie oczyszczonego TGFβ do komórek nowotworowych naśladowało efekt wzrostowy obserwowany po zastosowaniu płynu z komórek senescentnych, wskazując na tę rodzinę cytokin jako centralny czynnik pro-tumorowego sekretomu.
Jak sygnał przebudowuje komórki nowotworowe
Badanie śledziło następnie, w jaki sposób sygnały bogate w TGFβ zmieniają zachowanie sąsiednich komórek nowotworowych. Na powierzchni komórek odbierających TGFβ wiąże się ono z receptorem nazwanym TGFBR1. To z kolei uruchamia wewnętrzny kaskadę białek — zwłaszcza szlaki AKT i mTOR — które kontrolują wzrost komórki, metabolizm i przeżycie. Zarówno w ludzkich, jak i mysich komórkach raka płuca ekspozycja na wydzieliny po cisplatynie szybko zwiększała aktywowane (fosforylowane) formy AKT i jego docelowego białka p70S6K oraz podnosiła ekspresję genów cyklu komórkowego. Blokada TGFBR1 lekiem galunisertibem lub bezpośrednia inhibicja mTOR w dużej mierze wygaszały ten wzrost sygnalizacji i redukowały dodatkową proliferację, tworzenie kolonii i inwazyjny wzrost kul wywołany sekretomem senescentnym.
Od myszy do pacjentów: wspólny słaby punkt
Te mechanizmy nie ograniczały się do szalek Petriego. U myszy z guzami płucnymi mieszanie komórek senescentnych z niersenescentnymi prowadziło do szybszego wzrostu nowotworów i krótszego przeżycia, podczas gdy eliminacja komórek senescentnych lub blokada TGFBR1 hamowały ten efekt. Gdy standardowe leczenie cisplatyną zastosowano u myszy z genetycznie modyfikowanymi rakami płuca, guzy gromadziły markery senescencji wraz z wysoką aktywnością AKT/mTOR w pobliskich, wciąż dzielących się komórkach. Połączenie cisplatyny z inhibitorem TGFBR1 lub lekami senolitycznymi (selektywnie zabijającymi komórki senescentne) zmniejszało obciążenie guza i wydłużało przeżycie w porównaniu z samą chemioterapią. Co istotne, analizy próbek ludzkiego raka płuca i wysokozróżnicowanego surowiczego raka jajnika pobranych po terapii opartej na platynie ujawniły podobne wzorce: zwiększone markery senescencji i nasilona sygnalizacja AKT/mTOR w mikrośrodowisku guza, szczególnie w rejonach bogatych w komórki senescentne.
Przekształcanie słabości w przewagę
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że chemioterapia platynowa może pozostawić po sobie populację uszkodzonych, lecz niebezpiecznych „zombie” komórek. Te komórki senescentne już się nie dzielą, ale wyrzucają sygnały bogate w TGFβ, które pobudzają pobliskie komórki nowotworowe, pomagając guzom odrastać i opierać się dalszemu leczeniu. Dobrą wiadomością jest to, że tę słabość można zaatakować. W modelach przedklinicznych raka płuca i jajnika dodanie leków blokujących receptor TGFBR1 lub selektywnie usuwających komórki senescentne zwiększało skuteczność chemioterapii opartej na platynie i poprawiało przeżycie bez widocznego dodatkowego toksycznego efektu. Praca ta wskazuje kierunek przyszłych badań klinicznych łączących standardowe leczenie platynowe z strategiami senolitycznymi lub anty-TGFβ, z celem zachowania korzyści chemioterapii przy jednoczesnym unieszkodliwieniu jej ukrytych, napędzanych senescencją skutków ubocznych.
Cytowanie: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Słowa kluczowe: oporność na chemioterapię, senescencja komórkowa, sygnalizacja TGFβ, rak płuca, rak jajnika