Clear Sky Science · pl
Uszkodzenia DNA w makrofagach napędzają autoreaktywność immunologiczną poprzez prezentację antygenów jądrowych
Kiedy zużycie komórkowe obraca układ odpornościowy przeciw nam
Starzenie się zwiększa ryzyko chorób autoimmunologicznych, w których układ odpornościowy zaczyna atakować ciało, które ma chronić. Badanie to wskazuje zaskakującego sprawcę: codzienne uszkodzenia DNA wewnątrz komórek odpornościowych zwanych makrofagami. Śledząc, jak te uszkodzenia zmieniają to, co makrofagi pokazują innym komórkom układu odpornościowego, autorzy odkrywają możliwe brakujące ogniwo łączące starzenie się z rozwijaniem się chorób takich jak toczeń rumieniowaty.
Obrońcy organizmu poza scenariuszem
Makrofagi to pierwsza linia obrony, pochłaniająca drobnoustroje i szczątki, a następnie prezentująca fragmenty białek limfocytom T, pomagając układowi odpornościowemu zdecydować, co zaatakować. Zespół zmodyfikował myszy tak, by ich makrofagi miały defekt w kluczowym białku naprawy DNA, ERCC1-XPF, co powodowało utrzymywanie się uszkodzeń DNA w tych komórkach. W miarę starzenia się te myszy rozwijały cechy autoimmunizacji: ogniska zapalne w nerkach, złogi kompleksów immunologicznych i białek dopełniacza, powiększone śledziony oraz wysokie poziomy przeciwciał przeciwjądrowych podobne do obserwowanych u naturalnie starych zwierząt. Szczegółowy profil immunologiczny wykazał ekspansję komórek plazmatycznych, aktywowanych limfocytów T i komórek NK — wszystkie znaki przewlekłego pobudzenia układu odpornościowego.
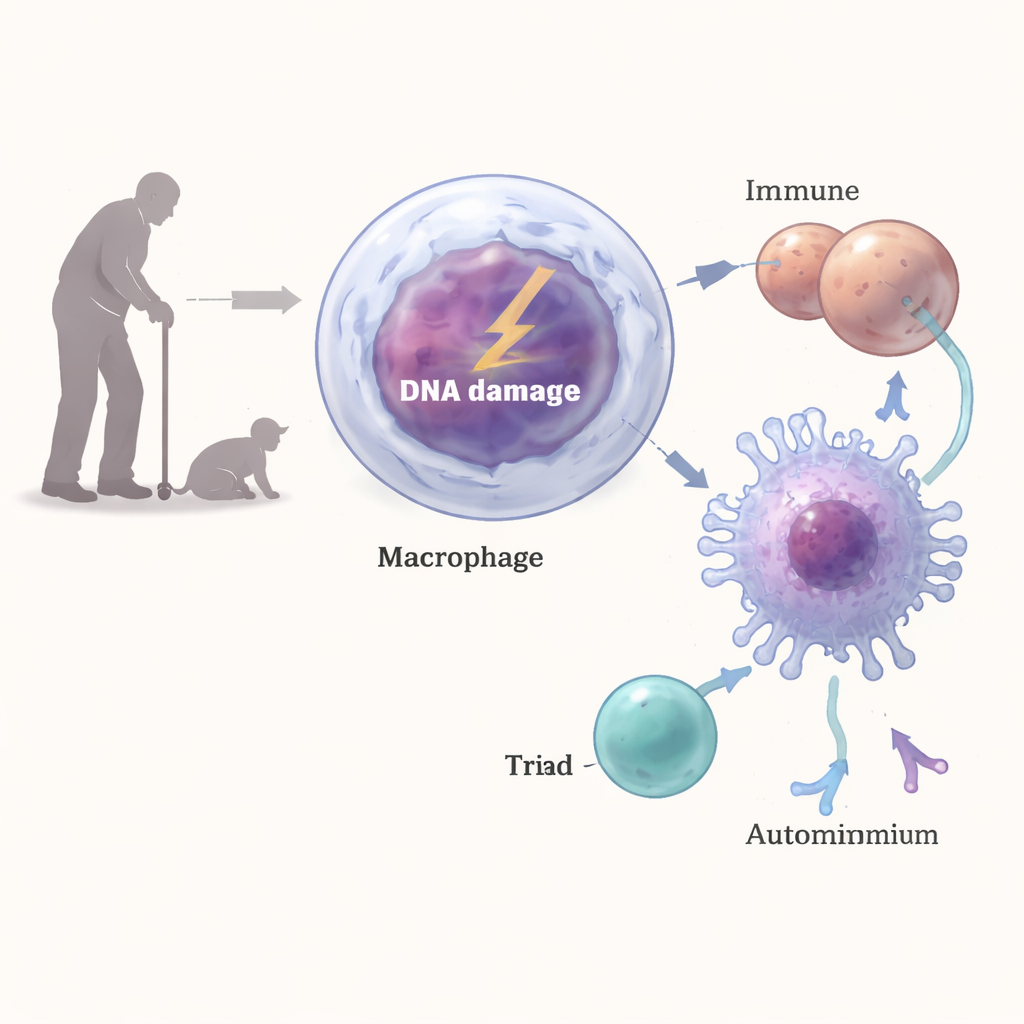
Od połamanych nici DNA do T komórek skierowanych przeciw sobie
W jaki sposób uszkodzone DNA w makrofagach mogło wywołać tak silną odpowiedź przypominającą autoimmunitet? Badacze stwierdzili, że pęknięcia DNA aktywowały klasyczną ścieżkę odpowiedzi na uszkodzenia w tych komórkach, obejmującą enzymy takie jak ATM, ATR i DNA-PK. To sygnalizowanie zwiększało poziomy MHC klasy II na powierzchni — molekularnych witryn do prezentacji fragmentów białek limfocytom CD4. Gdy makrofagi z uszkodzonym DNA zostały zmieszane z limfocytami T, powodowały silniejszą aktywację T i produkcję interferonu-γ niż makrofagi normalne. Zablokowanie MHC-II lub zakłócenie odpowiedzi na uszkodzenie DNA odwracało dużą część tego efektu, a in vivo przeciwciała blokujące MHC-II lub eliminujące limfocyty CD4 zmniejszały zapalenie nerek i poziomy autoantygenów.
Białka własne z jądra komórkowego wystawione na pokaz
Aby zobaczyć dokładnie, co uszkodzone makrofagi prezentowały limfocytom T, zespół wyizolował peptydy związane z MHC-II i przeanalizował je za pomocą spektrometrii mas. W porównaniu z komórkami normalnymi lub stymulowanymi lipopolisacharydem, makrofagi z uszkodzonym DNA prezentowały uderzająco inny zestaw peptydów. Zamiast głównie białek błonowych i zewnątrzkomórkowych, ich cząsteczki MHC-II były wzbogacone w fragmenty pochodzące z białek jądrowych i rybosomalnych, w tym histonów i innych składników ściśle związanych z DNA. Gdy niektóre z tych peptydów jądrowych zsyntetyzowano i użyto do ponownej stymulacji komórek odpornościowych pochodzących z modyfikowanych myszy, wywołały one silne odpowiedzi T, co sugeruje, że te fragmenty pochodzenia własnego były faktycznie immunogenne.
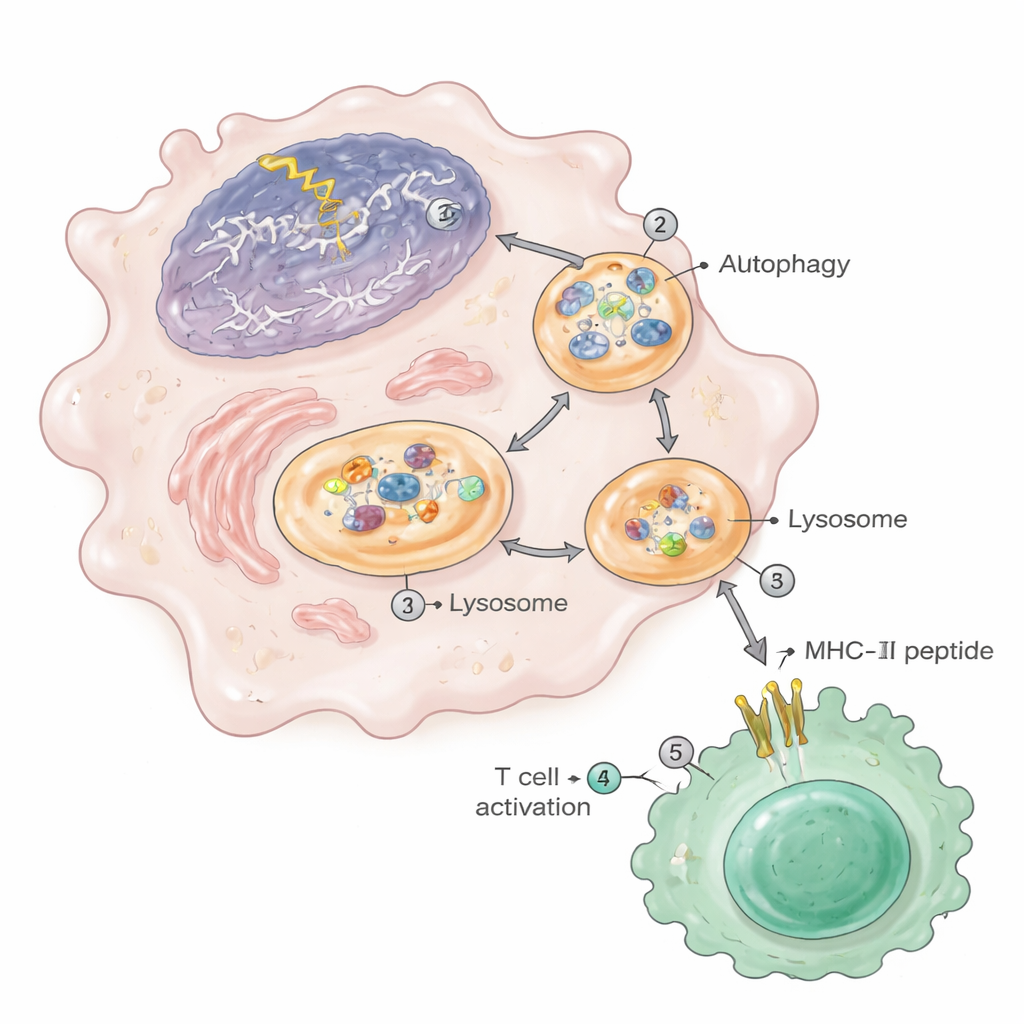
Autofagia: ścieżka sprzątająca, która podsyca autoimmunizację
Droga transportu materiału jądrowego do „gabloty” MHC-II w dużym stopniu zależała od autofagii — wewnętrznego systemu recyklingu komórki. Pod wpływem uszkodzeń DNA autofagia nasilała się i kierowała fragmenty chromatyny — z własnego jądra komórkowego — do autofagosomów, które potem łączyły się z lizosomami, gdzie białka są rozkładane na peptydy. W tych lizosomach uszkodzonych makrofagów stwierdzono podwyższone poziomy białek jądrowych i rybosomalnych. Gdy badacze zablokowali autofagię farmakologicznie lub genetycznie usunęli istotny gen autofagii (Atg5) w tych samych komórkach mieloidalnych, zwierzęta miały mniej zmian zapalnych w nerkach, mniej aktywowanych limfocytów T i komórek plazmatycznych oraz dramatyczne zmniejszenie liczby peptydów jądrowych pojawiających się na MHC-II. Podobne fragmenty chromatyny i zwiększona prezentacja antygenów zaobserwowano w makrofagach myszy podatnych na toczeń, w ludzkich liniach monocytarnych eksponowanych na leki uszkadzające DNA oraz w makrofagach bardzo starych myszy.
Dlaczego to ma znaczenie dla starzenia się i chorób autoimmunologicznych
Podsumowując, wyniki sugerują prosty, ale silny pomysł: w miarę starzenia się w makrofagach gromadzą się uszkodzenia DNA, które z kolei wykorzystują autofagię do usuwania jądrowych szczątków. W tym procesie przypadkowo rozdrabniają materiał jądrowy na peptydy, które są ładowane na MHC-II i pokazywane limfocytom T jakby były obce. Z czasem chroniczne wystawianie tych jądrowych autoantygenów może „wyuczyć” układ odpornościowy do reakcji przeciw własnemu organizmowi, sprzyjając autoimmunizacji. Wskazanie tej ścieżki — od uszkodzeń DNA, przez autofagię, po prezentację antygenów jądrowych — podkreśla nowe strategie łagodzenia autoimmunizacji związanej z wiekiem, takie jak wzmacnianie naprawy DNA, precyzyjne modulowanie autofagii lub selektywne blokowanie prezentacji jądrowych peptydów własnych bez wyłączania istotnych obron immunologicznych.
Cytowanie: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Słowa kluczowe: starzenie się i autoimmunizacja, uszkodzenia DNA, makrofagi, autofagia, przeciwciała przeciwjądrowe