Clear Sky Science · pl
Senotoksyny celują w starzenie poprzez specyficzne wiązanie lipidów, zaburzenie jonowe i przebudowę lipidomu
Dlaczego zabijanie „zombie” komórek może wzmocnić leczenie raka
W miarę jak się starzejemy — lub przechodzimy przez ciężkie terapie, jak chemioterapia — niektóre komórki przestają się dzielić, lecz odmawiają obumarcia. Te „zombie” komórki, zwane komórkami senescentnymi, mogą wydzielać zapalne molekuły uszkadzające tkanki i sprzyjające nawrotom nowotworów. Badanie to pokazuje zaskakujący sposób selektywnego eliminowania takich problematycznych komórek przy użyciu białka pochodzącego z jadu, co potencjalnie może uczynić terapie przeciwnowotworowe skuteczniejszymi i bezpieczniejszymi.
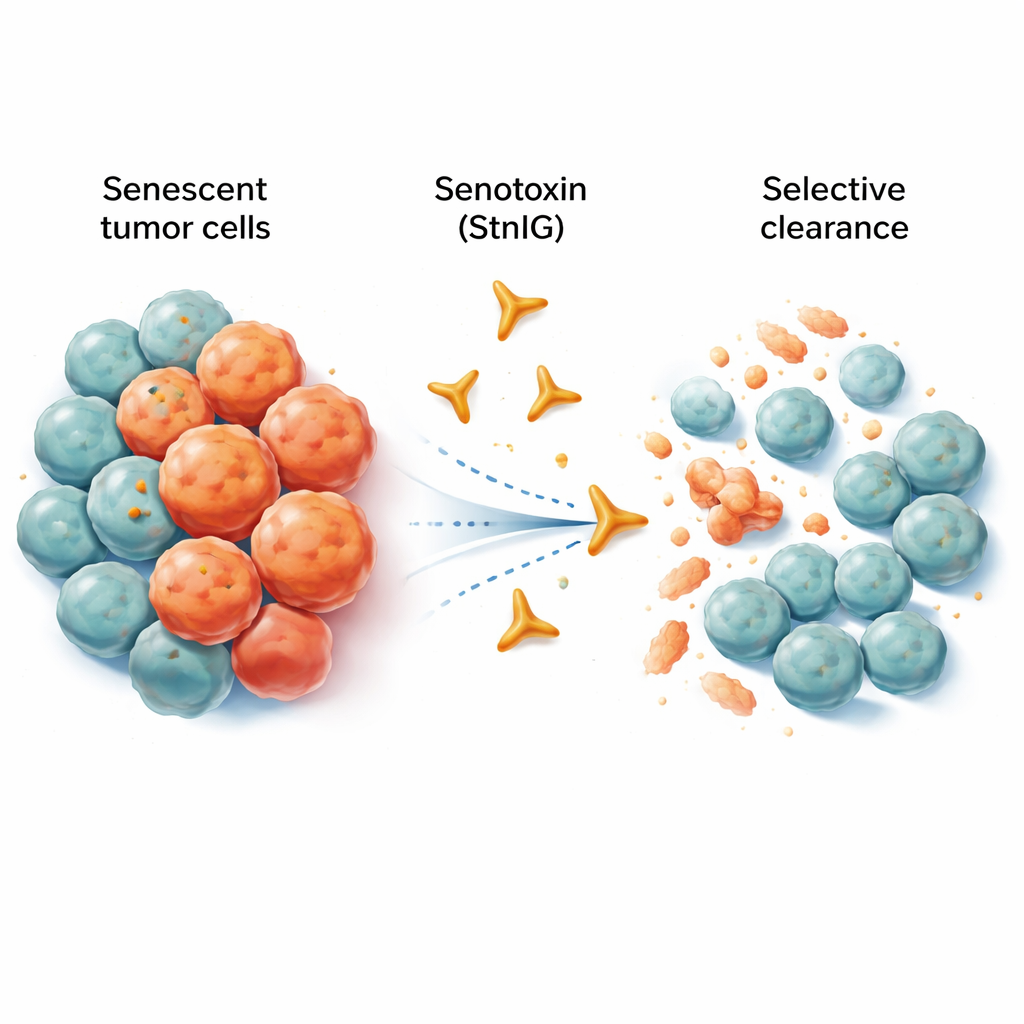
Stare komórki, które nie odchodzą
Komórki senescentne przypominają emerytów, którzy wciąż zajmują swoje biurka i zakłócają pracę. Nie dzielą się już, ale wydzielają mieszankę sygnałów zapalnych, które osłabiają otaczającą tkankę, sprzyjają procesom starzenia i mogą wspierać wzrost oraz rozprzestrzenianie się nowotworów. Chemioterapia, mimo że zabija wiele komórek nowotworowych, często pozostawia w i wokół guza ślad komórek senescentnych. Te przetrwałe komórki mogą napędzać przewlekłe zapalenie, działania niepożądane i w końcu wznowę choroby. Obecne eksperymentalne leki zwane senolitykami mają na celu usuwanie komórek senescentnych, ale wiele z nich uszkadza też zdrowe komórki, działa tylko w wąskim zakresie dawek lub ma słabą biodostępność.
Przekształcanie jadu ukwiału morskiego w narzędzie precyzyjne
Naukowcy zwrócili się do przyrody i jej wyspecjalizowanych narzędzi do zabijania komórek: jadowitych białek zwierzęcych. Skoncentrowali się na białku formującym pory zwanym sticholizyną I (StnI), obecnym w karaibskim ukwiale morskim. To białko potrafi robić maleńkie dziurki w błonach komórkowych. Zespół odkrył, że StnI oraz zmodyfikowana wersja, którą opracowali i nazwali StnIG, są znacząco lepsze w zabijaniu senescentnych komórek nowotworowych niż ich niesenescentne sąsiadki. W kilku typach ludzkich komórek nowotworowych (czerniak, wątroba, płuca i guzy pochodzenia nerwowego), które wprowadzono w senescencję za pomocą leków chemioterapeutycznych, StnI, a szczególnie StnIG, eliminowały starzejące się komórki przy znacznie niższych dawkach niż te potrzebne do wpływu na komórki aktywnie rosnące. StnIG okazał się bardziej selektywny niż wiodący eksperymentalny senolityk navitoklaks, co sugeruje, że precyzyjnie dostrojone toksyny mogą przewyższać obecne podejścia.
Dlaczego zmienione błony komórkowe stają się Achillową piętą
Komórki senescentne zmieniają nie tylko wnętrze; ich zewnętrzna błona — lipidowa „skóra” otaczająca komórkę — także ulega przebudowie. W zdrowych komórkach niektóre lipidy znajdują się głównie po wewnętrznej stronie błony, ukryte przed światem zewnętrznym. W komórkach senescentnych ta równowaga ulega zaburzeniu i te lipidy stają się odsłonięte. Dzięki szczegółowej analizie chemicznej i symulacjom komputerowym zespół wykazał, że StnIG rozpoznaje i wiąże się z tą zmienioną lipidową powierzchnią. Jego struktura jest szczególnie przystosowana do zakotwiczania się w określonych lipidach eksponowanych na powierzchni komórek senescentnych. Po przyłączeniu StnIG tworzy pory, które umożliwiają przepływ jonów w sposób wysoce niezrównoważony.
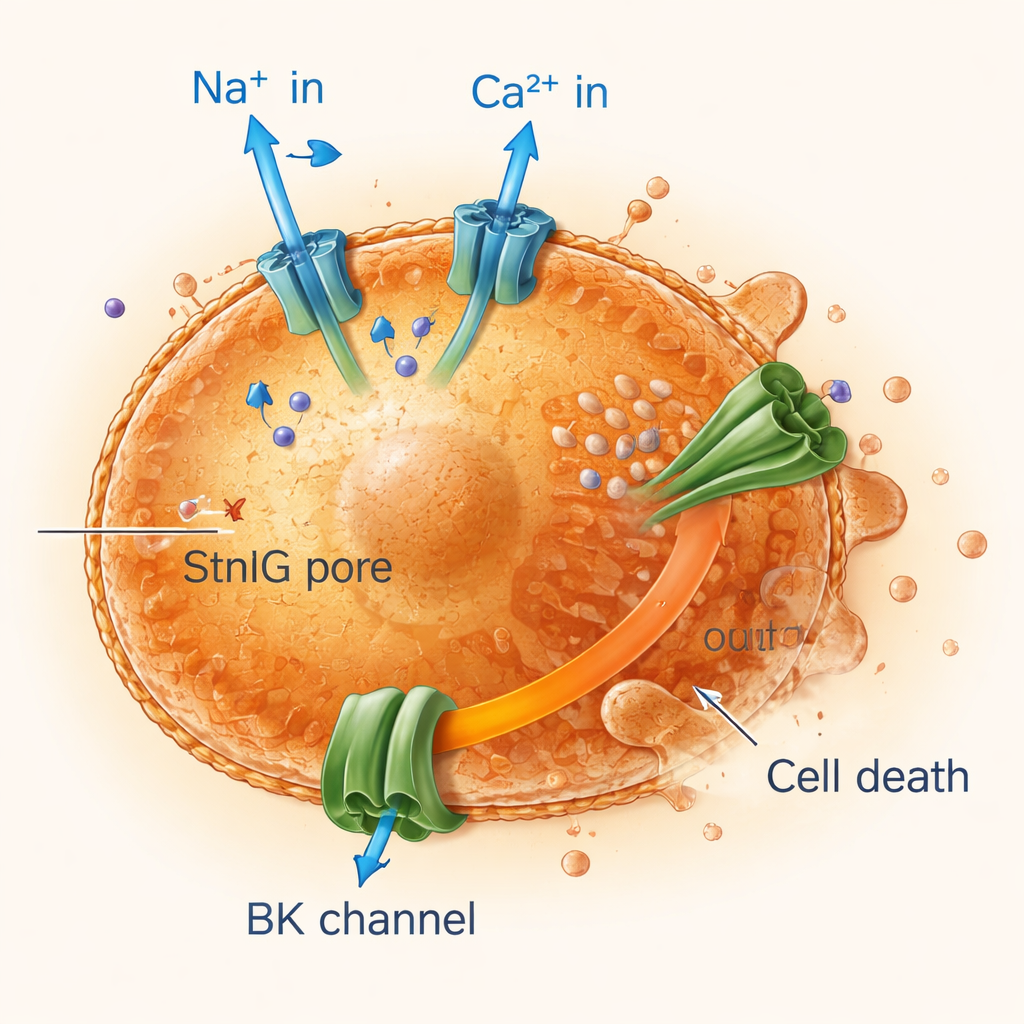
Wyłączanie starych komórek przez zaburzenie równowagi jonowej
Śledząc przepływ prądu i jonów przez błony komórkowe, badacze stwierdzili, że pory tworzone przez StnIG pozwalają na gwałtowny napływ jonów sodu i wapnia do komórek senescentnych, podczas gdy potas nieustannie ucieka na zewnątrz. Napływ wapnia uruchamia duże kanały potasowe, potęgując utratę potasu, który jest kluczowy dla utrzymania objętości i przeżycia komórki. Komórki senescentne, już mniej elastyczne i bardziej kruche niż zdrowe, nie radzą sobie z takim utrzymującym się zaburzeniem jonowym. Ich mitochondria — elektrownie komórkowe — tracą potencjał elektryczny, produkcja energii spada, a komórki przechodzą w zaprogramowane formy śmierci, w tym apoptozę i zapalną śmierć zwaną piroptozą. Blokada napływu wapnia lub kanałów potasowych chroniła komórki senescentne, potwierdzając, że to zaburzenie jonowe jest kluczowe dla działania toksyny.
Z hodowli komórek do organizmów żywych
Zespół sprawdził następnie, czy strategia działa także in vivo. W embrionach danio pręgowanego zawierających ludzkie komórki czerniaka w stanie senescencji, niskie dawki StnIG zmniejszały liczbę tych komórek równie skutecznie jak navitoklaks, bez oczywistej toksyczności. W modelach mysich czerniaka i raka wątroby chemioterapia z użyciem inhibitora cyklu komórkowego (palbociklib) spowalniała wzrost guza, powodując wejście wielu komórek nowotworowych w senescencję. Gdy badacze stosowali StnIG przerywanie, guzy kurczyły się lub przechodziły w remisję skuteczniej niż przy samej chemioterapii, porównywalnie z kombinacją chemioterapii i navitoklaksu. Co ważne, myszy leczone StnIG wykazywały ograniczone skutki uboczne i brak wyraźnych uszkodzeń głównych narządów, choć stężenie potasu we krwi wzrosło u zwierząt z senescentnymi guzami — prawdopodobnie odzwierciedlając masowy uwolnienie potasu podczas niszczenia komórek guza.
Co to oznacza dla przyszłej opieki onkologicznej
Praca ta wprowadza pojęcie „senotoksyn”: inżynieryjnie zmodyfikowanych białek inspirowanych jadem, które wykorzystują unikalne cechy błonowe i gospodarkę jonową komórek senescentnych. Celując w zmienione lipidy i wywołując śmiertelne zaburzenia jonowe, StnIG może selektywnie usuwać szkodliwe komórki senescentne, oszczędzając większość zdrowych tkanek. Stosowane razem z chemioterapią takie senotoksyny mogą w przyszłości pomóc oczyścić organizm z komórek „zombie”, które napędzają nawroty i przewlekłe zapalenie, zwiększając trwałość terapii przeciwnowotworowych i potencjalnie łagodząc niektóre długoterminowe skutki uboczne.
Cytowanie: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Słowa kluczowe: starzenie komórkowe, senolityki, terapia przeciwnowotworowa, leki pochodzące z jadu, kanały jonowe