Clear Sky Science · pl
Edytowanie zasadowe PIK3CD dostosowane do terapii CAR zwiększa przeciwnowotworową moc limfocytów T
Przeprogramowanie komórek walczących z rakiem
Terapia limfocytami T z chimerycznym receptorem antygenowym (CAR) zrewolucjonizowała leczenie niektórych nowotworów krwi, lecz wielu pacjentów wciąż doświadcza nawrotów lub nie reaguje. Jednym z głównych problemów jest to, że te zaprojektowane komórki odpornościowe mogą się wypalać lub nie utrzymywać wystarczająco długo w organizmie. W badaniu postawiono proste, lecz istotne pytanie: zamiast całkowicie przeprojektowywać CAR-y, co jeśli można subtelnie „dostroić” wewnętrzne okablowanie limfocytów T, aby pozostały silne dłużej i robiły to bezpiecznie?
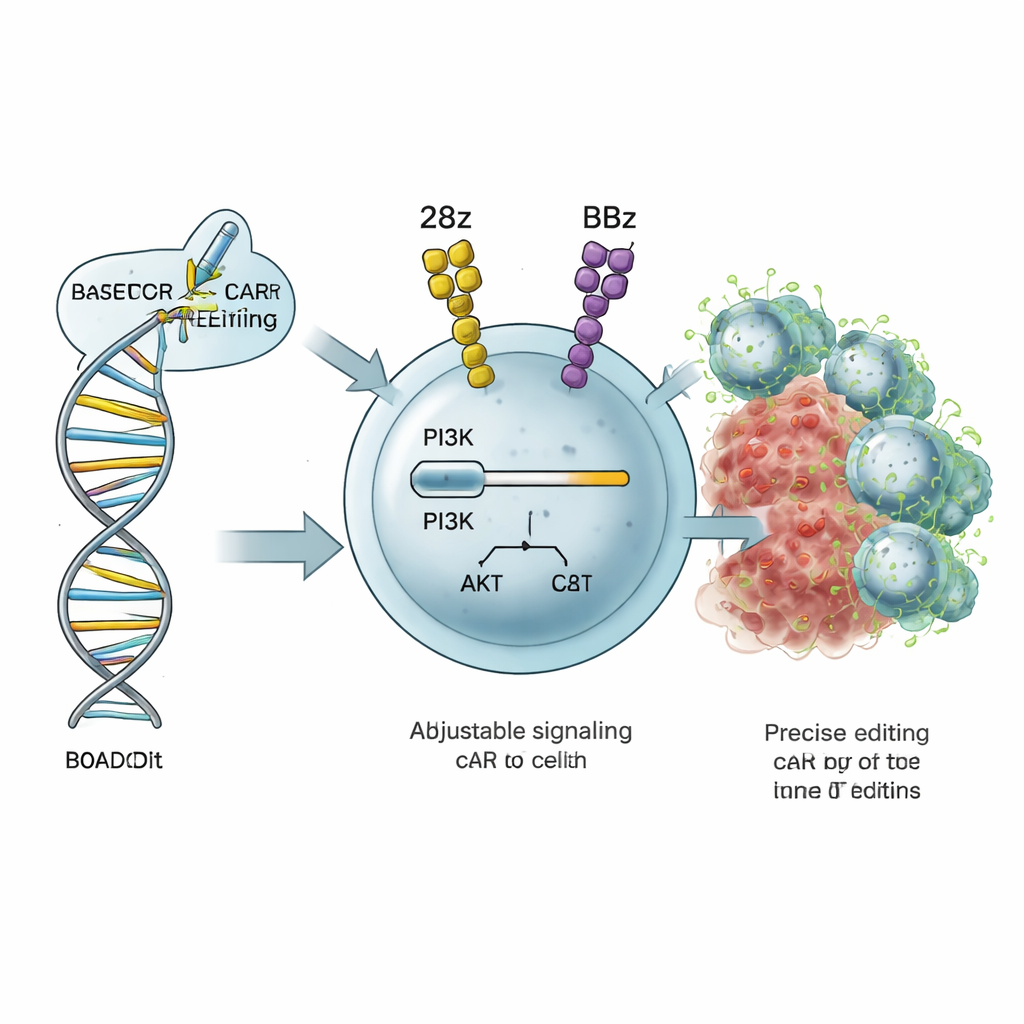
Celowanie w regulator głośności limfocytu T
Limfocyty T zabijające komórki nowotworowe opierają się na wewnętrznych układach sygnalizacyjnych, które wskazują, jak mocno mają się aktywować, jak szybko dzielić oraz czy stać się krótkożyjącymi wykonawcami czy długotrwałymi komórkami pamięci. Jednym z kluczowych układów jest szlak PI3K–AKT, w którym białko PI3Kδ — kodowane przez gen PIK3CD — działa jak pokrętło głośności dla aktywacji i metabolizmu. Autorzy opracowali strategię nazwaną ROADSTAR, wykorzystującą edytowanie zasadowe, wysoce precyzyjną formę inżynierii genomowej CRISPR, do zmiany pojedynczych „liter” w PIK3CD. Zamiast przełączać szlak całkowicie włączony lub wyłączony, ROADSTAR poszukuje drobnych mutacji, które łagodnie zwiększają lub zmniejszają sygnalizację w sposób najlepiej dopasowany do konkretnej konstrukcji CAR w limfocycie T.
Odkrywanie pomocnych mutacji
Zespół zbudował bibliotekę 34 różnych pojedynczych zmian liter w regionie regulacyjnym PIK3CD i wprowadził je do ludzkich limfocytów T, które już nosiły jedną z dwóch powszechnych konstrukcji CAR: 28z (opartą na cząsteczce CD28) i BBz (opartą na 4‑1BB). Te CAR-y różnią się sposobem stymulowania limfocytów T: 28z zwykle wywołuje silny, szybki atak, ale też wyczerpanie, podczas gdy BBz sprzyja lepszemu przetrwaniu i pamięci, lecz może być mniej agresywny. Edytowane limfocyty CAR T poddano „teście wytrzymałości” przez wielokrotne wystawianie ich na komórki białaczki. Przy użyciu głębokiego sekwencjonowania badacze śledzili, które mutacje pozwalały limfocytom CAR T prześcigać nieedytowane rówieśniki przez kilka tygodni.
Dwie mutacje wyróżniały się wyraźnie. W limfocytach BBz CAR zmiana nazwana E81K nieznacznie zwiększała aktywność PI3Kδ, wzmacniając sygnały w szlaku PI3K–AKT. W limfocytach 28z CAR inna zmiana, L32P, osłabiała aktywność PI3Kδ. Modele strukturalne sugerowały, że obie modyfikacje subtelnie zmieniają sposób, w jaki PI3Kδ oddziałuje ze swoim partnerem regulacyjnym, strojąc siłę sygnalizacji raczej niż przełączając ją w całości. Co ważne, korzystna mutacja dla jednej konstrukcji CAR nie była taka sama dla drugiej, podkreślając, że każda architektura CAR wymaga własnego optymalnego dostrojenia wewnętrznego.
Mocniejsze, sprawniejsze i dłużej działające limfocyty CAR T
Gdy obiecujące edycje przetestowano indywidualnie, E81K uczyniła limfocyty BBz CAR T bardziej aktywnymi po zetknięciu z komórkami nowotworowymi, lepiej proliferującymi i znacząco skuteczniejszymi w zabijaniu celów nowotworowych, w tym tych o niskim poziomie antygenu. Te komórki rozwijały się w efektorowe komórki pamięci, łącząc silną zdolność zabijania z umiejętnością długotrwałego przetrwania. W modelach mysich białaczki i przerzutującego neuroblastoma, limfocyty BBz CAR T z edycją E81K kontrolowały guzy bardziej kompletnie i znacznie dłużej niż nieedytowane komórki BBz, nawet pokonując wielokrotne rundy ponownego wyzwania nowotworowego. Szczegółowe badania pojedynczych komórek pod kątem RNA i metabolizmu wykazały, że komórki E81K miały poprawioną funkcję mitochondrialną, wyższą rezerwową zdolność oddechową i glikolityczną oraz mniej cech wyczerpania — zasadniczo były bardziej energetyczne i odporne.
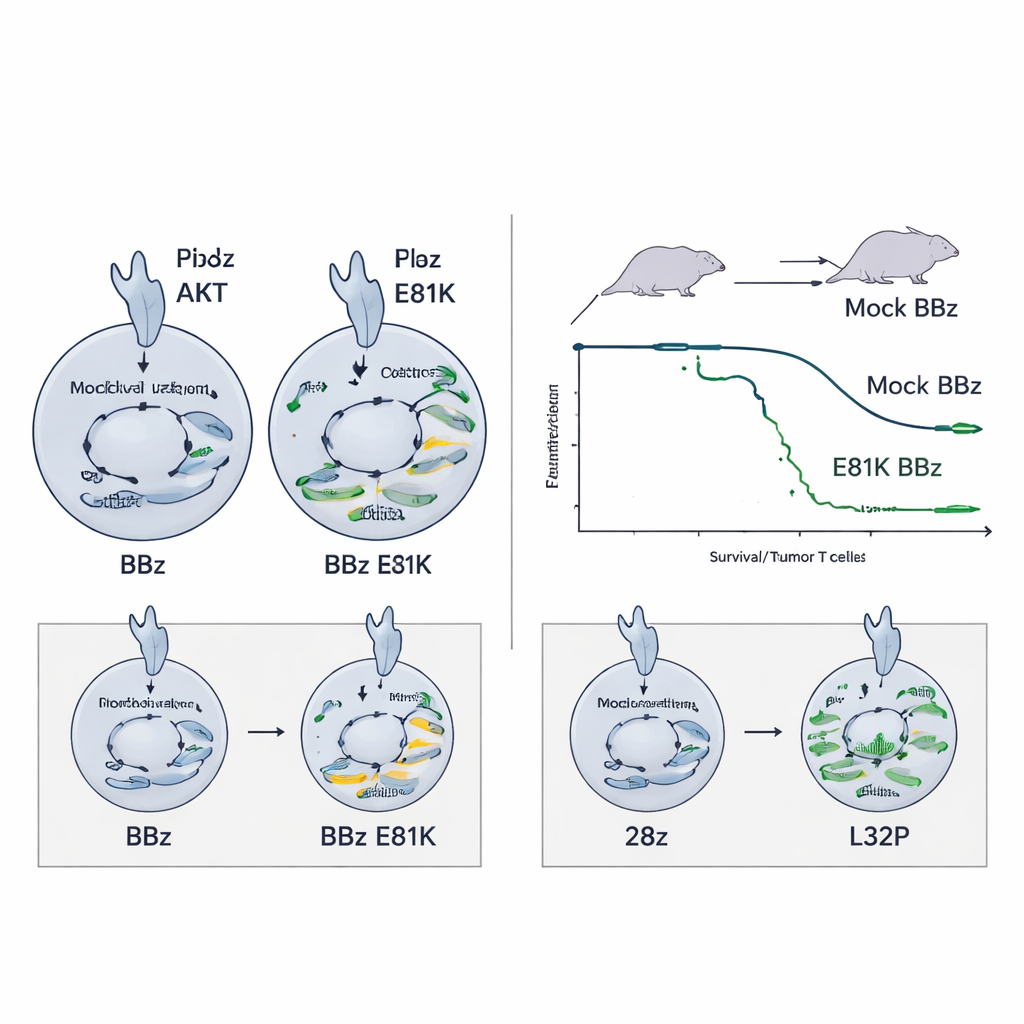
Zapobieganie wypaleniu w wysoce aktywnych CAR-ach
To samo wzmocnienie E81K nie pomagało — a nawet mogło zaszkodzić — limfocytom 28z CAR, które już sygnalizują bardzo silnie. W takim kontekście dodatkowa aktywność PI3K zwiększała markery wyczerpania bez poprawy funkcji. W tym przypadku mutacja L32P okazała się lepiej dopasowana: przez umiarkowane przyciszenie sygnalizacji PI3K–AKT, limfocyty 28z CAR T z edycją L32P wykazywały zmniejszoną aktywację w spoczynku, ale zachowały wysoką zdolność zabijania i lepiej proliferowały w czasie. Utrzymywały też mniej zróżnicowany, przypominający pamięć stan, w tym pulę komórek pamięci podobnych do komórek macierzystych, która uważa się za podtrzymującą długoterminowe odpowiedzi. W wymagającym modelu neuroblastoma komórki 28z CAR T zmodyfikowane L32P poprawiły przeżywalność w porównaniu z nieedytowanymi odpowiednikami.
Bezpieczeństwo i przyszłe perspektywy
Głównym zmartwieniem przy trwałym modyfikowaniu sygnalizacji immunologicznej jest ryzyko niekontrolowanego wzrostu lub wtórnych nowotworów. Dlatego autorzy przeprowadzili rozległe kontrole bezpieczeństwa. Limfocyty BBz CAR T z edycją E81K nie wykazywały nietypowego wzrostu w hodowli, nie powodowały uszkodzeń narządów ani kryzysów zapalnych u myszy i nie wykazywały oznak chłoniaka ani naciekania tkanek miesiące po infuzji. Bazy kliniczne również nie pokazują wzbogacenia tych konkretnych mutacji PIK3CD w białaczkach limfocytów T. Ogólnie praca pokazuje, że starannie dobrane pojedyncze edycje liter w genomie mogą działać jak precyzyjne regulatory zachowania limfocytów T — zwiększając moc przeciwnowotworową i trwałość przy jednoczesnym poszanowaniu unikalnej biologii każdego CAR-a. Podejście ROADSTAR może pomóc w opracowaniu następnej generacji terapii CAR T, które będą zarówno bardziej skuteczne, jak i bardziej niezawodne wobec nowotworów krwi, a potencjalnie także guzów litych.
Cytowanie: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Słowa kluczowe: limfocyty T CAR, sygnalizacja PI3K, edytowanie zasadowe, immunoterapia przeciwnowotworowa, metabolizm limfocytów T