Clear Sky Science · pl
De novo H3.3K27M-zmieniony rozlany glejak środkowej osi w organoidach pnia mózgu człowieka do analizy funkcji komórek CAR T rozpoznających GD2
Dlaczego to badanie dziecięcego nowotworu mózgu ma znaczenie
Rozlany glejak środkowej osi jest jednym z najgroźniejszych nowotworów mózgu u dzieci, atakując bardzo małe dzieci w pniu mózgu i pozostawiając rodzinom niemal brak skutecznych opcji leczenia. Ponieważ guzy znajdują się głęboko w mózgu i rzadko są operowane, badacze mają niewiele tkanki do analizy i niewiele bezpiecznych sposobów testowania nowych terapii. To badanie buduje realistyczny „mini‑pień mózgu na szalce” i wykorzystuje go do obserwacji, jak obiecująca immunoterapia — komórki CAR T przeciwko GD2 — zachowuje się przez tygodnie, w tym dlaczego czasem zawodzi.
Budowanie miniaturowego pnia mózgu w laboratorium
Zespół rozpoczął od ludzkich komórek macierzystych i krok po kroku poprowadził je do wzrostu w trójwymiarowe organoidy mózgu przypominające region pnia mózgu zwany mostem (pons), gdzie zwykle rozwijają się te guzy. Poprzez staranne dawkowanie sygnałów wzrostu uzyskali organoidy bogate w te same typy komórek podporowych, czyli gleju, które normalnie występują w tym obszarze. Szczegółowe analizy genetyczne wykazały, że typy komórek i ich dojrzewanie podążały za wzorcami obserwowanymi we wczesnym rozwoju ludzkiego mózgu, w szczególności liniami glejowymi typowymi dla mostu i sąsiedniej opuszki (medulla). To oznacza, że organoidy mogą służyć jako realistyczne tło do badania, jak ten nowotwór się zaczyna i rozwija.
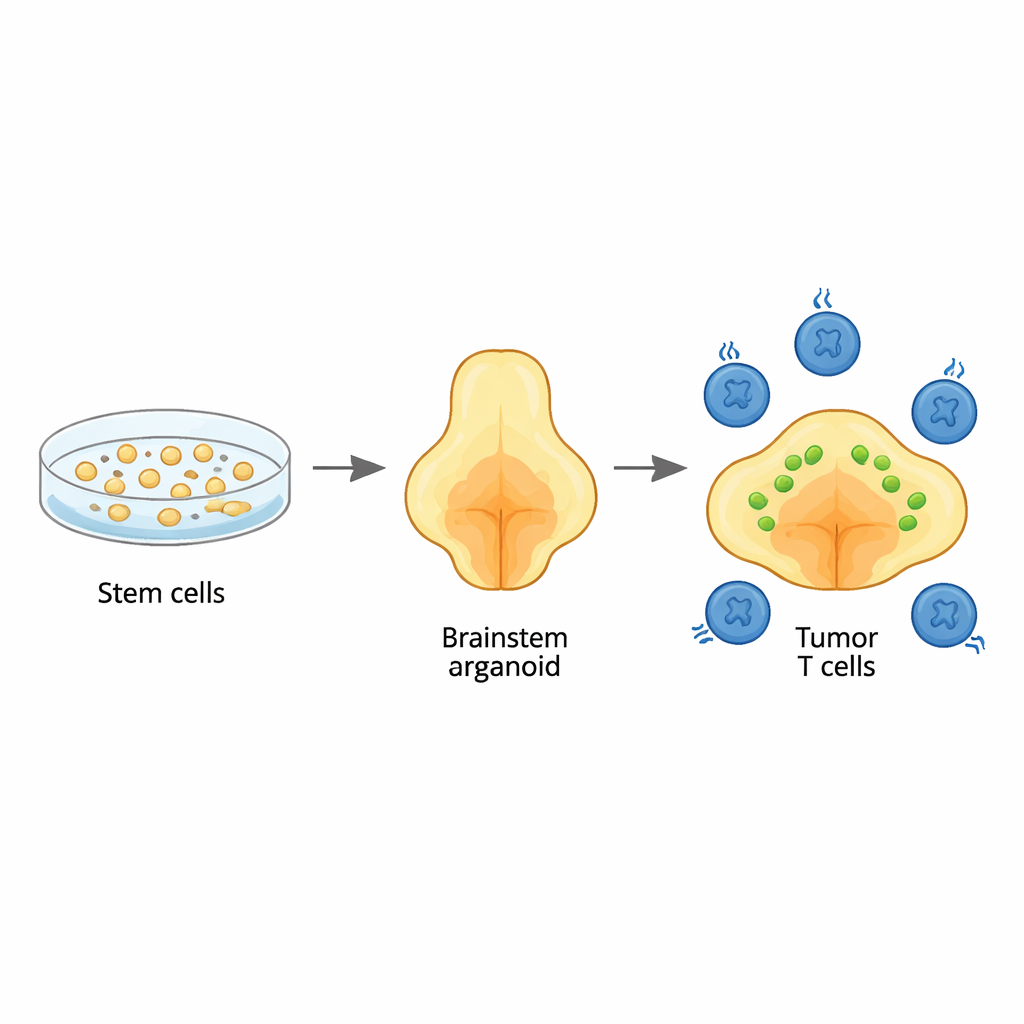
Odtworzenie guza dziecka wewnątrz organoidu
Aby naśladować rozlany glejak środkowej osi, badacze wprowadzili trzy kluczowe zmiany genetyczne do młodych organoidów: charakterystyczną mutację w białku histonowym (H3.3K27M), utratę supresora nowotworowego TP53 oraz aktywującą zmianę w receptorze wzrostu PDGFRA. Gdy zmiany te wprowadzono we wczesnym stadium rozwojowym, przekształciły wybrane komórki o cechach glejowych w nowotworowe. Powstałe guzy rozprzestrzeniały się rozlanie przez organoidy, tak jak w pniach mózgu dzieci, i miały te same szerokie sygnatury DNA i RNA obserwowane w guzach pacjentów. Sekwencjonowanie pojedynczych komórek ujawniło mieszankę stanów komórek nowotworowych, w tym niedojrzałe komórki glejowe specyficzne dla mostu, odpowiadające tym znalezionym w prawdziwych guzach pediatrycznych, co potwierdza, że model wiernie odtwarza ludzką chorobę.
Obserwowanie, jak terapie immunologiczne walczą — i się wyczerpują — w czasie
Majac ten model guza w pniu mózgu, zespół dodał komórki CAR T rozpoznające GD2 — limfocyty T pacjentów zmodyfikowane genetycznie do rozpoznawania cząsteczki GD2 na komórkach nowotworowych — i śledził zarówno rozmiar guza, jak i zachowanie komórek T przez okres do miesiąca. Niektóre organoidy wykazywały silne zmniejszenie guza, inne jedynie częściową kontrolę, odzwierciedlając mieszane wyniki obserwowane w badaniach klinicznych. Sekwencjonowanie RNA pojedynczych komórek ponad 20 000 komórek CAR T wystawionych na kontakt z guzami ujawniło zaskakującą różnorodność stanów komórek T. Niektóre komórki były wysoce cytotoksyczne — „egzekutorami”, inne aktywowane, ale nie w pełni zabójcze, a odrębna grupa wykazywała cechy wyczerpania, z osłabioną ekspresją genów zabijających nowotwór i wysoką ekspresją inhibitorowych „hamulców”. Wyjątkowo wyczerpane komórki przypominały wyeksploatowane limfocyty T spotykane w przewlekłych infekcjach i nowotworach u ludzi, co wskazuje, że system organoidowy odzwierciedla klinicznie istotne zmęczenie komórek T spowodowane ciągłym kontaktem z rakiem.
Wyszukanie potężnych, ale krótkotrwałych komórek T
Pogłębiając analizę, badacze zidentyfikowali podgrupę komórek CAR T oznaczonych białkiem powierzchniowym NCAM1, które były szczególnie skutecznymi zabójcami w krótkim terminie. Gdy te komórki pozytywne dla NCAM1 izolowano i stosowano oddzielnie, początkowo kontrolowały guzy silniej niż ich NCAM1‑ujemne odpowiedniki. Jednak szybko również ulegały wyczerpaniu i zanikały, co prowadziło do słabszej kontroli w dłuższej perspektywie. Ten kompromis między natychmiastową siłą a długotrwałą trwałością pomaga wyjaśnić, dlaczego terapie CAR T mogą dawać dramatyczne, ale przejściowe odpowiedzi, i sugeruje, że wstępna selekcja lub modyfikacja podtypów komórek T mogłaby zoptymalizować trwałość leczenia.
Jak komórki odpornościowe mózgu mogą osłabiać terapię
W prawdziwym mózgu guzy otaczane są nie tylko przez neurony i glej, lecz także przez mikroglej — rodzimy układ odpornościowy mózgu. Aby uchwycić ten poziom złożoności, naukowcy dodali do swoich organoidów mikroglej pochodzący z komórek macierzystych. Komórki te dojrzewały, przyjmowały morfologię i wzorce ekspresji genów specyficzne dla mikrogleju znajdującego się w rozlanym glejaku środkowej osi i wytwarzały cząsteczki związane ze środowiskiem immunosupresyjnym. Gdy komórki CAR T dodano do organoidów z guzem zawierających mikroglej, komórki T przechodziły jeszcze bardziej w kierunku stanów wyczerpania i niskiej efektywności, a kontrola guza pogarszała się. Jednocześnie wzrosły czynniki zapalne powiązane z działaniami niepożądanymi terapii, takie jak IL‑6, co sugeruje, że model może także pomóc w badaniu toksyczności związanej z terapią CAR T.
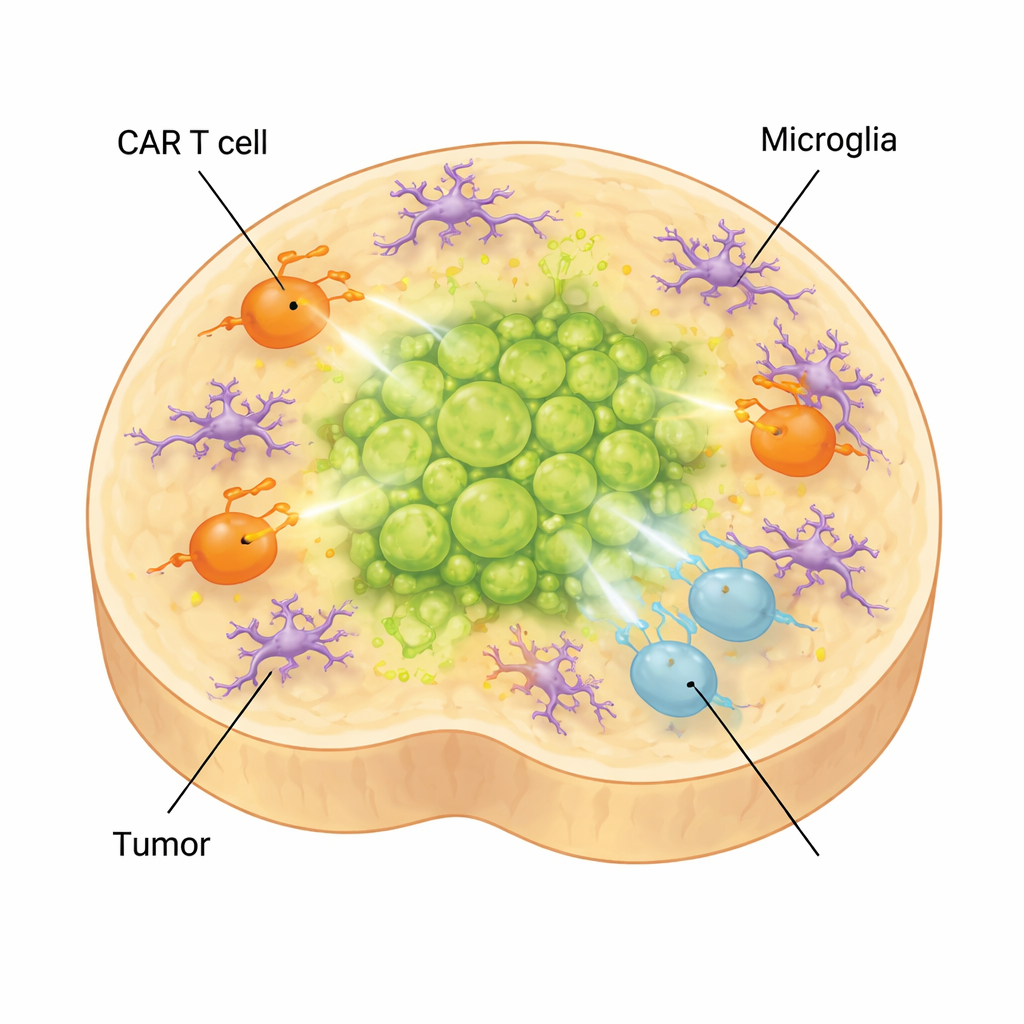
Co to oznacza dla dzieci z tym nowotworem
Dla rodzin zmagających się z rozlanym glejakiem środkowej osi ta praca nie daje jeszcze nowego lekarstwa, ale stanowi potężne pole do testów, które może przyspieszyć jego opracowanie. Odtwarzając środowisko pnia mózgu dziecka i guz w naczyniu, naukowcy mogą teraz obserwować w czasie rzeczywistym, jak różne komórki nowotworowe, typy komórek CAR T i mikroglej wchodzą w interakcje przez tygodnie. Pozwala to określić, które zmodyfikowane komórki T są najbardziej skuteczne, jak i kiedy ulegają wyczerpaniu oraz jak rezydujące w mózgu komórki odpornościowe podważają ich działanie. Ostatecznie takie modele organoidowe mogłyby być spersonalizowane dla poszczególnych pacjentów i używane do dopracowywania immunoterapii przed ich podaniem, zwiększając szanse, że przyszłe leczenia komórkami CAR T będą jednocześnie bezpieczniejsze i bardziej skuteczne dla dzieci.
Cytowanie: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Słowa kluczowe: rozlany glejak środkowej osi, organoidy mózgu, komórki CAR T, pediatryczny nowotwór mózgu, mikroglej