Clear Sky Science · pl
Prognozowanie i interpretacja odpowiedzi leków specyficznych dla typów komórek w reżimie małych danych za pomocą uprzednich indukcyjnych
Dlaczego te badania są ważne dla przyszłych leków
Gdy testuje się nowy lek, jednym z największych niewiadomych jest to, jak różnie wpłynie on na rozmaite typy komórek w naszym organizmie. Związek, który pomaga jednemu typowi komórek, może w innym nie dawać efektu, a nawet wyrządzić szkodę. Generowanie tych informacji eksperymentalnie dla tysięcy leków i niezliczonych typów komórek jest zbyt powolne i kosztowne. W artykule przedstawiono podejście komputerowe nazwane PrePR-CT, które uczy się przewidywać, jak poszczególne typy komórek reagują na leki, nawet gdy dostępne są tylko ograniczone dane. Praca wskazuje drogę do szybszych, tańszych i precyzyjniejszych metod badania potencjalnych leków in silico, zanim podejmie się kosztowne prace laboratoryjne i kliniczne.
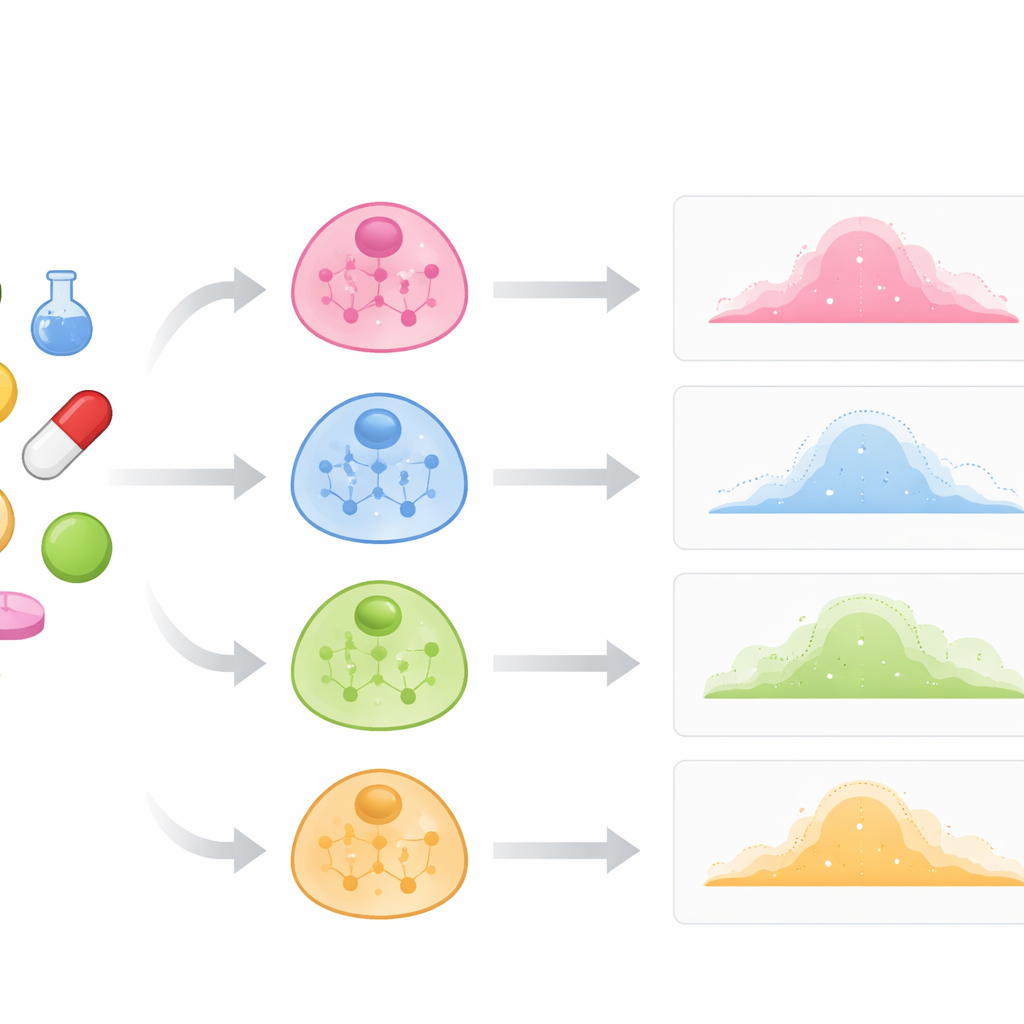
Patrzenie w głąb komórek zamiast tylko na leki
Tradycyjne przesiewy leków często traktują komórki tak, jakby były wszystkie takie same, i skupiają się głównie na średnich zbiorczych. W rzeczywistości komórki odpornościowe, wątrobowe czy nowotworowe mogą reagować bardzo różnie na ten sam związek. Autorzy argumentują, że aby przewidzieć te różnice, model musi rozumieć wewnętrzne powiązania charakterystyczne dla każdego typu komórek: które geny mają tendencję do wspólnej aktywacji i jak te wzorce definiują tożsamość komórki. Tworzą „mapy” typów komórek, badając, które geny w komórkach niepoddanych perturbacji (kontrolnych) wzrastają i maleją wspólnie. Każda mapa jest reprezentowana jako sieć, gdzie węzły odpowiadają genom, a łącza odzwierciedlają silną współaktywność. Sieci te służą jako uprzednia wiedza o organizacji danego typu komórki przed dodaniem jakiegokolwiek leku.
Silnik uczący się z uwzględnieniem sieci
PrePR-CT łączy trzy składniki: sieć aktywności genów dla danego typu komórek, bazowe (wyjściowe) poziomy ekspresji genów tego typu oraz zwartą reprezentację chemicznej struktury leku. Model wykorzystuje klasę sieci neuronowych zaprojektowanych dla grafów, aby przetrawić sieć genów i wyekstrahować streszczenie odzwierciedlające charakterystyczne wzorce. Równolegle każdy lek jest przekształcany w numeryczny odcisk palca pochodzący ze struktury molekularnej. Te elementy trafiają do modułu predykcyjnego, który uczy się, na podstawie dostępnych eksperymentów, jak dany lek przesunie rozkład aktywności genów w tym typie komórki. Zamiast zwracać jedną liczbę na gen, metoda estymuje zarówno średnią zmianę, jak i zmienność odpowiedzi między poszczególnymi komórkami, co jest kluczowe dla rozróżnienia subtelnych i silnych efektów.
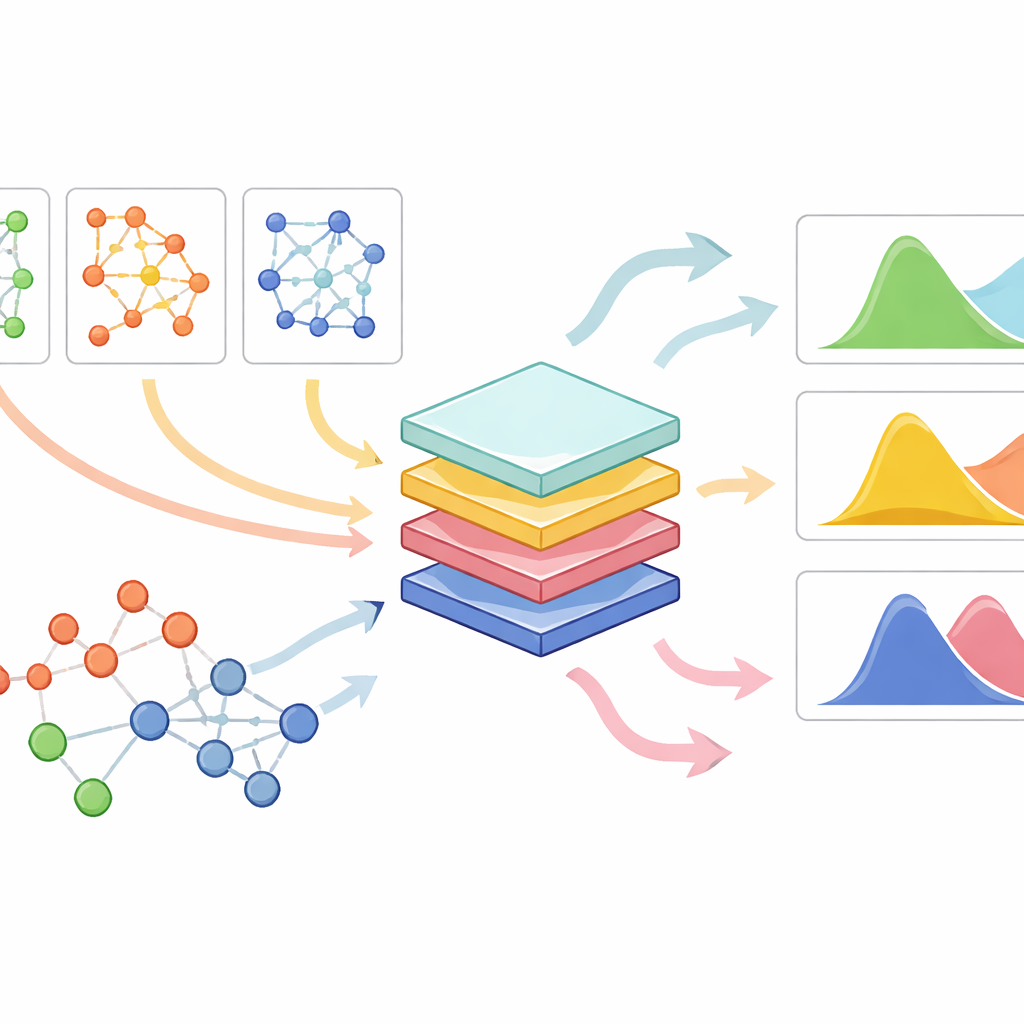
Praca na wielu typach komórek, lekach i małych zbiorach danych
Badacze przetestowali PrePR-CT na szerokim zbiorze danych, obejmującym między innymi ludzkie komórki krwi wystawione na sygnały immunologiczne, liczne linie komórkowe nowotworowe traktowane różnymi związkami, mysie komórki wątroby narażone na zanieczyszczenie oraz duże przesiewy leków z zasobów publicznych. W trudnych scenariuszach, gdy cały typ komórki był wyłączony z treningu, model wciąż potrafił przewidzieć, jak nowy typ komórki zareaguje na znany lek, często z dokładnością przewyższającą wcześniejsze modele generatywne. Podobnie, gdy wyłączono nowy lek przy znanym typie komórki, metoda poprawnie przewidywała jego wpływ, używając jedynie odcisku chemicznego. Co ważne, model pozostawał skuteczny przy treningu na stosunkowo małej liczbie komórek — w warunkach, w których wiele podejść głębokiego uczenia ma problemy.
Od czarnej skrzynki do wskazówek o mechanizmie
Ponad samymi predykcjami autorzy chcieli sprawdzić, czy model może dostarczyć wskazówek, które geny i szlaki napędzają odpowiedź komórki. Architektura oparta na grafach obejmuje mechanizm uwagi, który podkreśla geny, które model uznaje za szczególnie wpływowe dla każdego typu komórek. Wiele z tych „genów o wysokiej uwadze” nie było typowymi kandydatami wyróżnianymi przez standardowe analizy różnicowej ekspresji, a mimo to skupiały się w szlakach związanych z odpornością, zgodnych z biologią badanych leków. Gdy badacze celowo zakłócili obecność tych wpływowych genów na wejściu modelu, jakość predykcji spadła, zwłaszcza dla najbardziej responsywnych genów, co sugeruje, że oceny uwagi wskazują na sensowne, mechanistyczne elementy, a nie na szum.
Co to oznacza dla projektowania lepszych leków
Mówiąc prosto, praca pokazuje, że zapewnienie modelom sztucznej inteligencji uporządkowanego obrazu tego, jak każdy typ komórki jest połączony — jej wewnętrznej sieci genów — znacząco poprawia ich zdolność do przewidywania, jak leki przekształcą te komórki, nawet gdy dostępne są jedynie skromne zbiory danych. PrePR-CT nie zastępuje eksperymentów, ale może pomóc zawęzić wybór związków i typów komórek wartych dalszych testów oraz zasugerować, dlaczego niektóre komórki reagują w określony sposób. W miarę jak zbiory danych rosną i włączane będą dodatkowe cechy komórkowe, takie podejścia mogą stać się kluczowymi narzędziami do dopasowywania terapii do konkretnych tkanek lub typów komórek pacjenta, zmniejszając prób i błąd w laboratorium i przybliżając precyzyjniejsze leki do zastosowań klinicznych.
Cytowanie: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Słowa kluczowe: prognozowanie odpowiedzi na leki, transkryptomika pojedynczych komórek, grafowe sieci neuronowe, odkrywanie leków, specyficzność względem typu komórki