Clear Sky Science · pl
Raport o ponownym użyciu: Ocena wydajności modelu bazowego meta-uczenia przy przewidywaniu aktywności przeciwbakteryjnej produktów naturalnych
Poszukiwanie nowych antybiotyków, szybciej
Oporność na antybiotyki rośnie, a odkrywanie nowych leków przebiega boleśnie wolno i często opiera się na metodzie prób i błędów w laboratorium. W tej pracy badano, czy potężny rodzaj sztucznej inteligencji, pierwotnie wytrenowany na ogromnych zbiorach danych dotyczących leków, można szybko dostosować do przewidywania, które pochodzące z roślin związki naturalne mogą zwalczać bakterie — wykorzystując jedynie niewielkie ilości nowych danych eksperymentalnych. Jeśli się to powiedzie, takie narzędzia mogą pomóc naukowcom skupić cenny czas laboratoryjny na najbardziej obiecujących kandydatach i przyspieszyć poszukiwania kolejnej generacji antybiotyków.
Dlaczego chemia roślin ma znaczenie
Wiele naszych najlepszych antybiotyków pochodziło z produktów naturalnych roślin i mikroorganizmów. Te cząsteczki potrafią zatrzymać wzrost bakterii, ale znalezienie nowych w naturze przypomina szukanie igły w stogu siana. Badacze muszą testować wiele związków wobec różnych szczepów bakterii, a każdy test jest kosztowny. Co gorsza, duże, starannie oznaczone zbiory danych — których potrzebują nowoczesne metody głębokiego uczenia, by działać dobrze — są w tej dziedzinie rzadkie. To sprawia, że odkrywanie antybiotyków jest idealnym polem do testów dla „modeli bazowych”: dużych, uniwersalnych systemów AI, które można dostroić do konkretnych zadań, używając zaledwie kilku nowych przykładów.
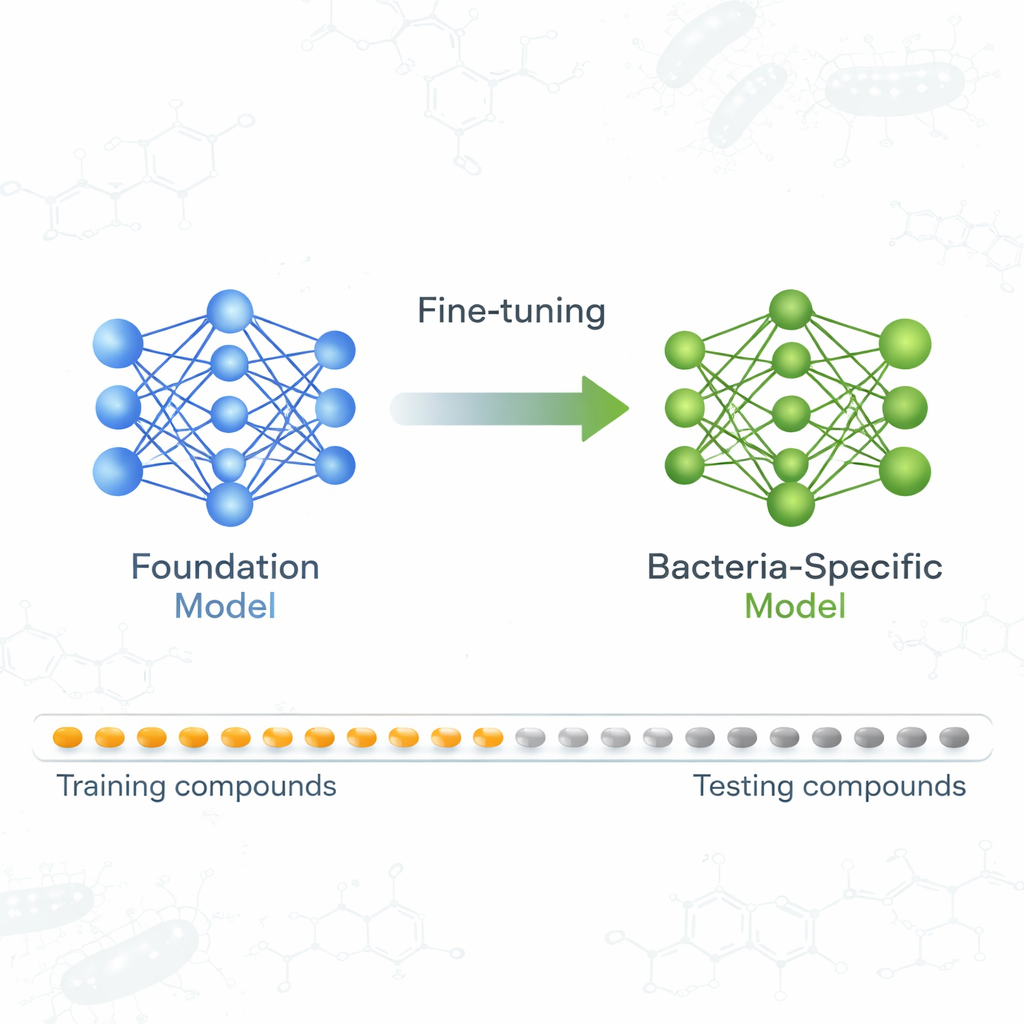
Model bazowy uczy się o zabójcach drobnoustrojów
Zespół skupił się na modelu bazowym nazwanym ActFound, pierwotnie wytrenowanym do przewidywania, jak silnie różne związki chemiczne wpływają na biologiczne cele, z wykorzystaniem ogromnych zbiorów danych z zasobów takich jak bazy ChEMBL i BindingDB. Zamiast przewidywać pojedynczą wartość dla każdego związku, ActFound uczy się przez porównywanie par związków w ramach tego samego eksperymentu i szacowanie, który z nich jest bardziej aktywny. To „uczenie parami”, połączone ze strategią treningową znaną jako meta-uczenie, ma pomóc modelowi w szybkim dostosowaniu się do nowych zadań predykcyjnych, gdy dostępna jest tylko niewielka liczba oznaczonych przykładów — dokładnie taka sytuacja występuje w wielu przesiewach w poszukiwaniu antybiotyków.
Testowanie modelu na danych z rzeczywistego świata — produkty roślinne
Aby sprawdzić, jak naprawdę nadaje się ActFound do ponownego użycia, autorzy dostroili go do kuratorowanego zbioru danych produktów naturalnych pochodzenia roślinnego, testowanych pod kątem zdolności do hamowania wzrostu różnych bakterii. Każdy szczep bakteryjny traktowano jako odrębne zadanie, a model adaptowano, używając tylko 8 do 128 związków na szczep lub stałych procentów dostępnych danych. Porównano też ActFound z prostszymi modelami meta-uczenia i transfer-learningu, które nie stosują porównań parami. W tych testach ActFound nie osiągnął dokładności, jaką wykazywał we wcześniejszych pracach na innych typach danych dotyczących leków. Jednak przy bardzo ograniczonych danych — mniej więcej kilku związkach na szczep — ActFound i jego wariant transfer-learningowy zazwyczaj dorównywały lub przewyższały alternatywne metody.
Kiedy podobieństwo pomaga — i kiedy szkodzi
ActFound zakłada, że podobne cząsteczki zachowują się podobnie, co działa dobrze, gdy zbiory danych budowane są wokół grup powiązanych chemicznie związków. Zbiór danych produktów naturalnych był jednak chemicznie zróżnicowany i często brakowało w nim blisko spokrewnionych „rodzin” związków. Ta różnorodność, choć cenna naukowo, podważała strategię uczenia parami: gdy związki w ramach eksperymentu są bardzo różne, model ma trudności z uczeniem stabilnych porównań. Autorzy stwierdzili również, że prosta diagnostyka zaproponowana w oryginalnym artykule ActFound, mająca przewidywać z wyprzedzeniem, jak dobrze model poradzi sobie z nowym zadaniem, nie sprawdziła się dla tych danych o produktach naturalnych, co uwypukla ważne ograniczenie przy przechodzeniu do nowych przestrzeni chemicznych.
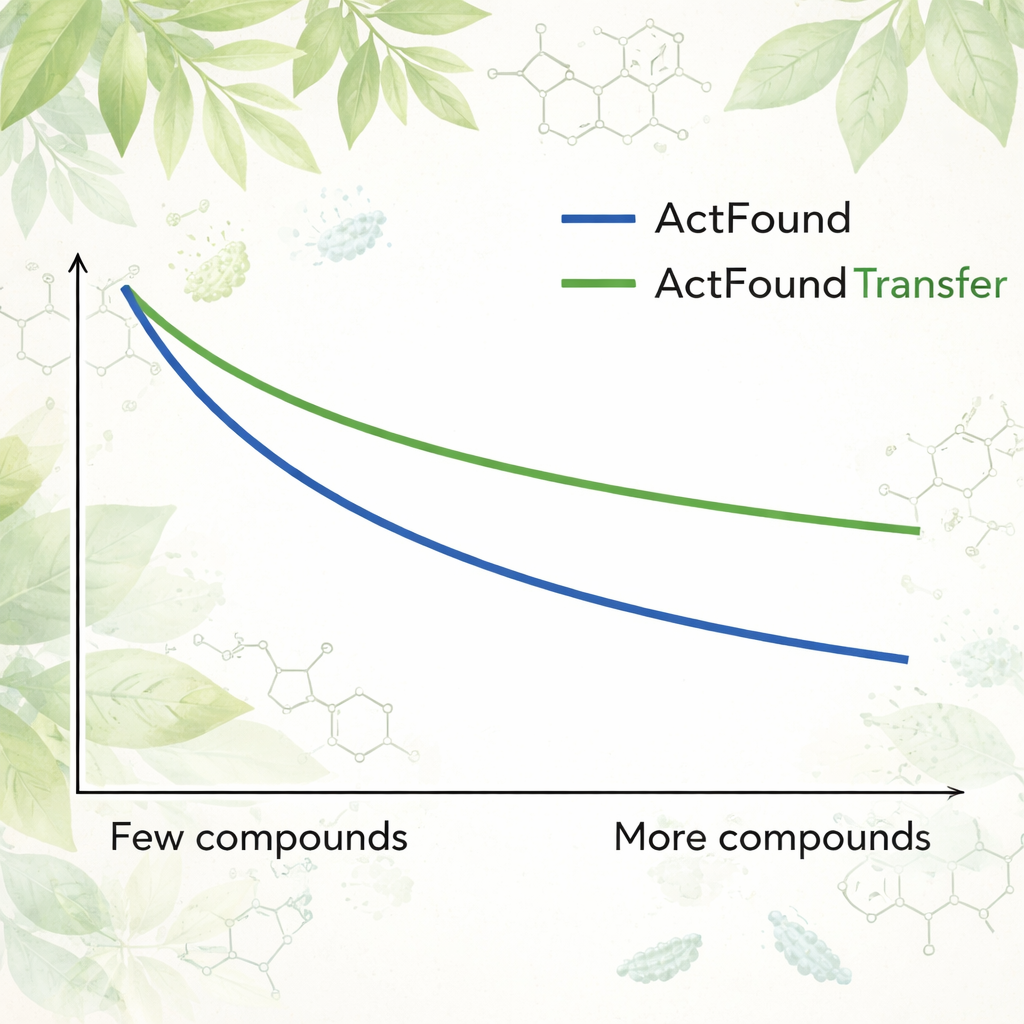
Co to oznacza dla przyszłego odkrywania leków
Dla osób niebędących specjalistami wnioskiem jest to, że modele bazowe takie jak ActFound są obiecującymi narzędziami w odkrywaniu leków, gdy danych jest mało, ale nie są rozwiązaniem cudownym. W tym badaniu ActFound i jego wersja transfer-learningowa często radziły sobie równie dobrze lub lepiej niż konkurencyjne metody, gdy do treningu dostępnych było tylko kilka związków roślinnych, lecz miały trudności na tym silnie zróżnicowanym zbiorze produktów naturalnych. Praca sugeruje, że modele te są najbardziej użyteczne, gdy dane zawierają wiele chemicznie podobnych związków — na przykład w ukierunkowanych studiach nad zależnością struktura–aktywność — lecz pozostają mniej wiarygodne przy przewidywaniu zachowania zupełnie nowych rodzajów cząsteczek. Innymi słowy, AI może pomóc zawęzić poszukiwania, ale najtrudniejsza część eksploracji rzeczywiście nowych obszarów chemicznych wciąż leży przed nami.
Cytowanie: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Słowa kluczowe: odkrywanie antybiotyków, produkty naturalne, głębokie uczenie, meta-uczenie, przesiewanie leków