Clear Sky Science · pl
Nienasycone kwasy tłuszczowe sprzyjają rozsprzężonej respiracji przez nośniki ATP/ADP w białych adipocytach
Dlaczego komórki tłuszczowe mogą pomagać spalać energię
Większość osób postrzega tkankę tłuszczową jako bierne magazynowisko kalorii. To badanie ujawnia zaskakująco aktywny aspekt białych adipocytów: w określonych warunkach potrafią marnować paliwo i wytwarzać ciepło. Odkrycie nowego mechanizmu „ucieczki” energii z komórek tłuszczowych otwiera nowe możliwości zwiększania wydatku energetycznego organizmu i potencjalnego przeciwdziałania otyłości.
Gdy zgromadzony tłuszcz zostaje ponownie przekształcony w paliwo
Na co dzień białe adipocyty spędzają większość czasu na magazynowaniu energii w postaci trójglicerydów — dużych kropli tłuszczu. Podczas wysiłku, postu czy ekspozycji na zimno sygnały stresowe uruchamiają rozkład trójglicerydów, uwalniając kwasy tłuszczowe i glicerol. Badacze potwierdzili, że stymulacja tego rozkładu w hodowlach białych komórek tłuszczowych prowadzi do wyraźnego wzrostu zużycia tlenu, co świadczy o zwiększonej pracy mitochondriów. Zablokowanie pierwszego etapu rozkładu tłuszczu zatrzymało zarówno uwalnianie kwasów tłuszczowych, jak i wzrost poboru tlenu, co pokazuje, że proces zależy od samych kwasów tłuszczowych.
Wolne kwasy tłuszczowe jako wyłączniki spalania energii
Kwasy tłuszczowe opuszczające adipocyt nie wszystkie wychodzą z tkanki — część pozostaje wewnątrz. Zespół wykazał, że te pozostające wolne kwasy tłuszczowe są kluczowe dla zwiększenia aktywności mitochondrialnej. Gdy w medium hodowlanym użyto białka pochłaniającego kwasy tłuszczowe, komórki wypuszczały więcej tłuszczu ogółem, lecz ich zużycie tlenu spadało, co sugeruje, że wysoki poziom wewnętrznych kwasów tłuszczowych — a nie sam rozkład tłuszczu — napędza dodatkową respirację. Odwrotnie, blokada ponownego estryfikowania trójglicerydów, szlaku zwykle przepakowującego kwasy tłuszczowe, podniosła zużycie tlenu i jeszcze bardziej obniżyła potencjał elektryczny błony mitochondrialnej. Razem te wyniki sugerują, że wolne kwasy tłuszczowe popychają mitochondria w tryb „nieszczelny”, marnujący energię.
Nowy uczestnik respiracji produkującej ciepło
W klasycznej brunatnej tkance tłuszczowej białko UCP1 tworzy pory w barierze mitochondrialnej, dzięki czemu energia z pożywienia jest uwalniana jako ciepło zamiast być magazynowana jako użyteczne paliwo komórkowe. Białe adipocyty mają niewiele lub wcale UCP1, więc autorzy poszukiwali innej drogi. Skupili się na nośniku ATP/ADP, białku transportowym, które zwykle wymienia walutę energetyczną komórki przez barierę mitochondrialną. Stosując specyficzny bloker chemiczny i narzędzia genetyczne do zmniejszenia ilości tego nośnika, wykazali, że jest on niezbędny dla wywoływanej przez kwasy tłuszczowe „nieszczelności”: blokada nośnika zachowywała ładunek mitochondrialny i zapobiegała wzrostowi zużycia tlenu podczas rozkładu tłuszczu, mimo że sam rozkład przebiegał normalnie. Wskazuje to, że wolne kwasy tłuszczowe współdziałają z nośnikiem, tworząc kontrolowany przeciek protonów przez barierę mitochondrialną i uruchamiając rozsprzężoną respirację.
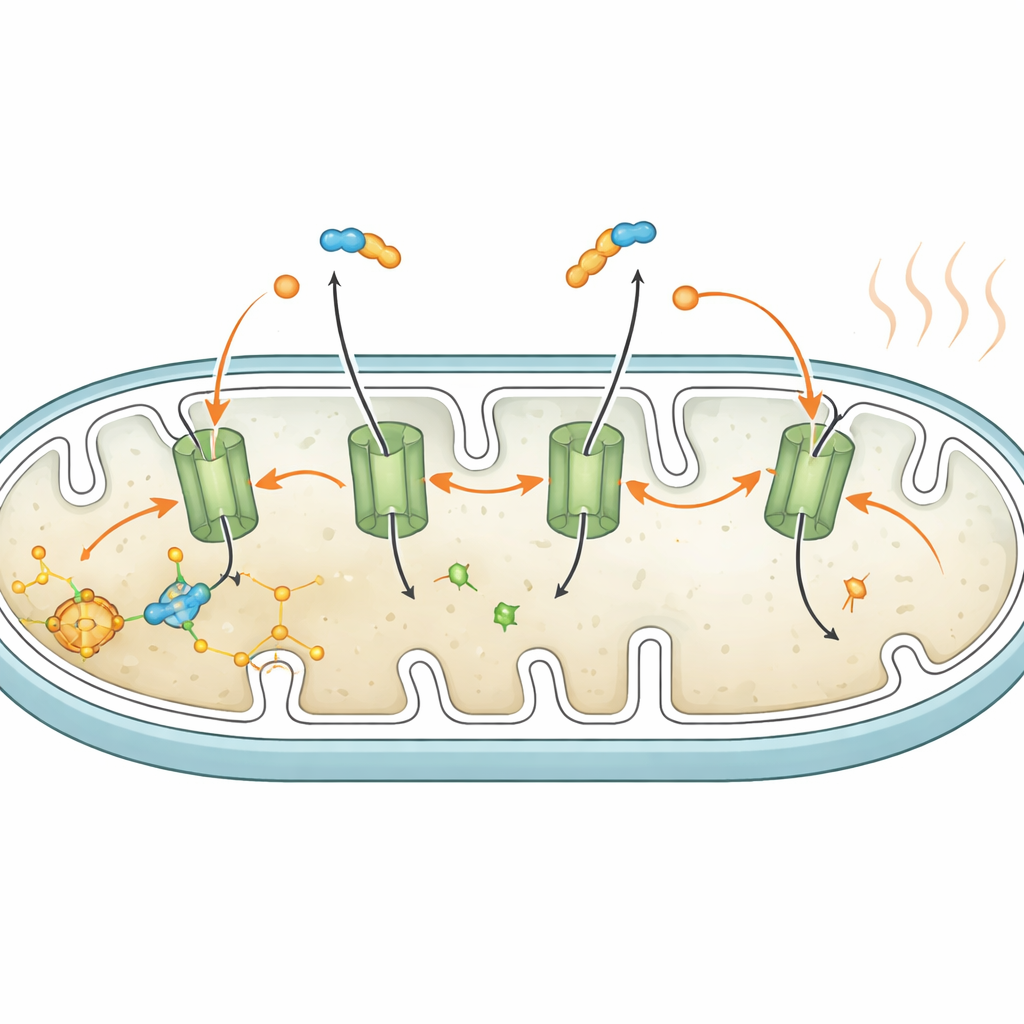
Od hodowli komórek do żywych zwierząt
Aby sprawdzić, czy ten wyciek energii ma znaczenie u całych zwierząt, badacze użyli myszy, u których białkowy przekaźnik STAT3 został usunięty specyficznie w komórkach tłuszczowych. Zwierzęta te prawidłowo przeprowadzają rozkład tłuszczu, ale wykazują osłabioną respirację napędzaną kwasami tłuszczowymi w tkance białej. W zwykłych warunkach laboratoryjnych, gdy brunatna tkanka tłuszczowa jest aktywna i odpowiada za większość obrony przed zimnem, myszy te utrzymywały ciepło podobnie jak ich normalne mioty. Jednak po uczynieniu myszy otyłymi i umieszczeniu ich w temperaturze, przy której brunatna tkanka jest w dużej mierze nieaktywna, zwierzęta pozbawione STAT3 w tkance tłuszczowej stały się wrażliwe na zimno i wykazywały słabszy wzrost całkowitego zużycia tlenu podczas ekspozycji na zimno lub farmakologicznego wywołania rozkładu tłuszczu. Co istotne, podobnych zmian nie zaobserwowano, gdy STAT3 usunięto wyłącznie w brunatnej tkance tłuszczowej, co wskazuje na specyficzną rolę tkanki białej.
Biała tkanka tłuszczowa jako ukryty ogrzewacz
Badanie konkluduje, że w białych adipocytach wolne kwasy tłuszczowe wytwarzane podczas aktywnego rozkładu tłuszczu mogą wiązać się z nośnikiem ATP/ADP w mitochondriach i wywołać wyciek energii, który wytwarza ciepło zamiast użytecznego paliwa komórkowego. U otyłych zwierząt utrzymywanych w cieple ta rozsprzężona respiracja w tkance białej istotnie przyczynia się do utrzymania temperatury ciała i całkowitego wydatku energetycznego, zwłaszcza gdy brunatna tkanka i drżenie mięśniowe są ograniczone. Ponieważ biała tkanka tłuszczowa jest obfita u dorosłych, szczególnie w otyłości, łagodne zwiększenie tego „przecieku” mogłoby stanowić nowy sposób na podniesienie codziennego spalania kalorii i wspomaganie terapii odchudzających, o ile można to zrobić bezpiecznie i bez uszczerbku dla innych tkanek.
Cytowanie: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Słowa kluczowe: tkanka tłuszczowa biała, kwasy tłuszczowe, rozsprzężenie mitochondrialne, termogeneza, otyłość