Clear Sky Science · pl
PFKM reguluje przemiany metaboliczne podczas różnicowania mięśni szkieletowych
Dlaczego komórki mięśniowe muszą mądrze gospodarować cukrem
Kiedy ćwiczymy lub po prostu wstajemy z krzesła, nasze mięśnie szkieletowe ruszają do pracy, spalając cukier, by zasilać każdy skurcz. Jednak młode komórki macierzyste mięśni i w pełni ukształtowane włókna mięśniowe nie przetwarzają glukozy w ten sam sposób. Badanie ujawnia wbudowany mechanizm przełączający — skupiony wokół pojedynczego enzymu nazwanego PFKM — który decyduje, czy glukoza ma być spalana dla natychmiastowej energii, czy przekierowana, by chronić i odbudowywać komórki. Zrozumienie tego przełącznika może otworzyć nowe drogi leczenia osłabienia mięśni, starzejących się mięśni i wrodzonych chorób metabolicznych.
Światło drogowe dla komórkowego paliwa
Glukoza wchodząca do komórki może podążać kilkoma trasami. Jedna główna droga, glikoliza, szybko przekształca cukier w energię i elementy budulcowe potrzebne rosnącym włóknom mięśniowym. Inna ścieżka, szlak pentozofosforanowy, wytwarza cząsteczki chroniące komórki przed oksydacyjnym stresem oraz wspierające syntezę DNA i lipidów. Badacze skupili się na PFKM, wersji enzymu fosfofruktokinazy-1, która znajduje się w kluczowym punkcie glikolizy. Mierząc setki metabolitów w ciągu minut do godzin po aktywacji sygnału wzrostu zwanego Wnt, odkryli, że komórki szybko gromadziły wczesne pośrednie produkty glikolizy, podczas gdy produkt PFKM malał, a metabolity szlaku pentozofosforanowego rosły. Sugeruje to, że komórki aktywnie dławiły aktywność PFKM, by przekierować glukozę w stronę reakcji ochronnych zamiast czystej produkcji energii. 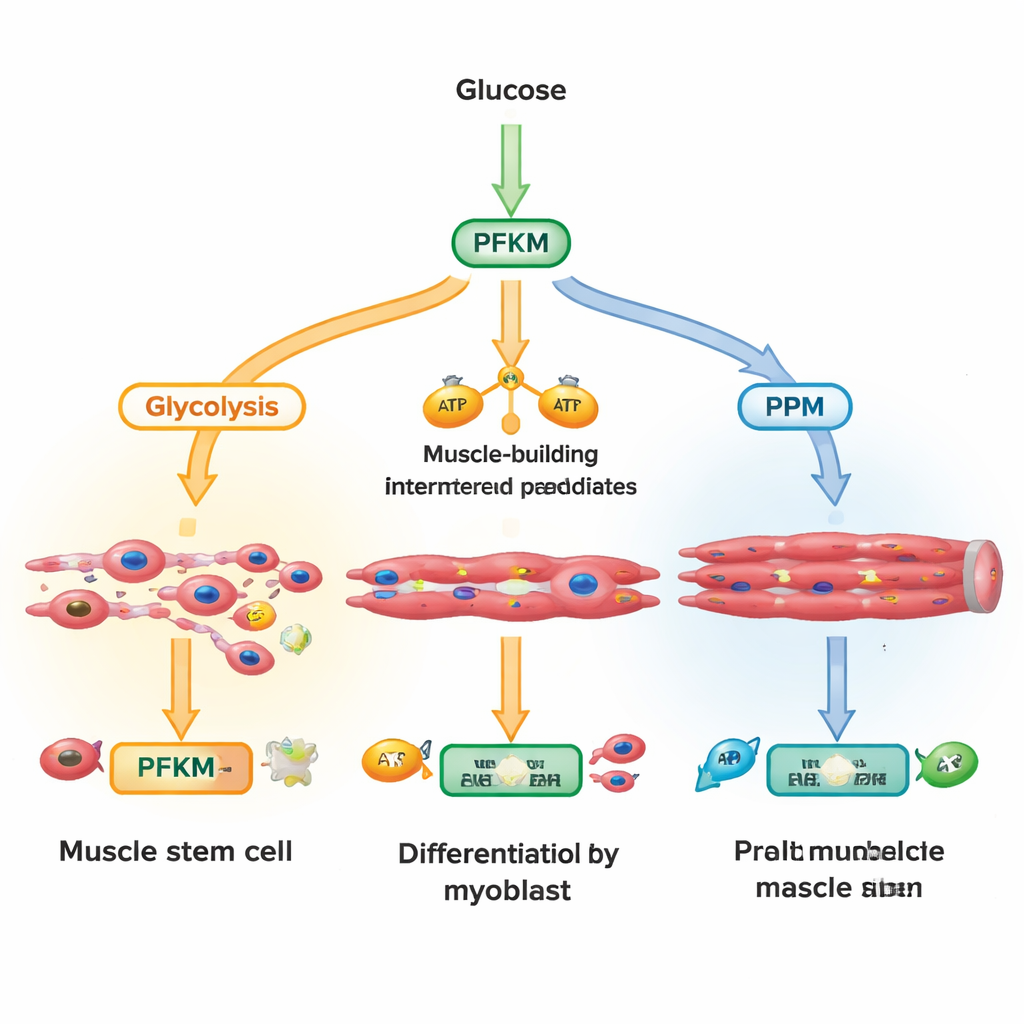
Oznaczanie i usuwanie enzymu-strażnika
Aby sprawdzić, jak kontrolowany jest PFKM, zespół śledził lokalizację białka w komórkach. W warunkach spoczynkowych PFKM był rozproszony w cytoplazmie. W ciągu minut od stymulacji Wnt gromadził się w jasnych kropkach, które nakładały się na lizosomy — komórkowe przedziały rozkładające białka. Dwa siostrzane enzymy, PFKL i PFKP, nie zmieniały lokalizacji ani poziomów, co wskazywało, że tylko izoforma mięśniowa PFKM była celem. Testy biochemiczne wykazały, że blokada funkcji lizosomów zapobiegała utracie PFKM, podczas gdy hamowanie proteasomu — drugiego głównego systemu usuwania białek — nie miało wpływu. Analiza sekwencji ujawniła krótki motyw „methyl arginine degron” unikalny dla PFKM. Enzym PRMT1 dodał specyficzną grupę metylo na argininie w tym motywie, a ta modyfikacja pozwalała maszynerii mikroautofagii, w tym białku VPS4, wciągnąć PFKM do lizosomów celem degradacji. Wyłączenie PRMT1 lub VPS4 stabilizowało PFKM i blokowało jego usuwanie.
Od komórki macierzystej do pracującego włókna mięśniowego
Korzystając z dużych ludzkich zestawów danych z pojedynczych komórek, autorzy mapowali poziomy PFKM w różnych typach komórek mięśniowych. Komórki macierzyste mięśni, które pozostają uśpione do czasu potrzeby naprawy, miały bardzo mało PFKM, ale wyrażały liczne geny szlaku pentozofosforanowego oraz komponenty lizosomalne. W miarę jak komórki zobowiązywały się do różnicowania w mięsień i łączyły w wielojądrowe włókna, transkrypty i białko PFKM gwałtownie wzrastały, podczas gdy cele Wnt i geny lizosomalne słabły. W hodowlach ludzkich i mysich komórek mięśniowych Wnt szybko kierowało PFKM do lizosomów w wczesnych, jednojądrowych komórkach, ale nie w dojrzałych wielojądrowych włóknach. Ten wzorzec wspiera model, w którym komórki niedojrzałe utrzymują niski poziom PFKM — poprzez lizosomalną degradację — aby faworyzować ochronny metabolizm, a następnie ponownie go eksprymują w trakcie przejścia w energetycznie wymagające włókna kurczliwe.
Co się dzieje, gdy przełącznik jest zablokowany
Aby sprawdzić znaczenie PFKM dla budowy mięśni, zespół obniżył jego poziomy za pomocą interferencji RNA. Komórki z niskim PFKM miały trudności z uruchomieniem charakterystycznych genów mięśniowych, produkowały mniej miozyny i tworzyły mniej oraz mniejsze włókna wielojądrowe, mimo że ogólna liczba komórek pozostała niezmieniona. Profilowanie metabolitów wykazało zmniejszenie dalszych pośrednich produktów glikolizy i paliw cyklu kwasu trójkarboksylowego, ale wzrost genów i znaczników szlaku pentozofosforanowego oraz zwiększoną odporność na stres oksydacyjny. Co ważne, dostarczenie komórkom 3‑fosfogliceranu — pośredniego produktu glikolizy zlokalizowanego zwykle poniżej PFKM — uratowało wiele defektów różnicowania. Markery mięśniowe i formowanie włókien odrodziły się, co pokazało, że brakujące metabolity, a nie sam utracony enzym PFKM, były główną przeszkodą. 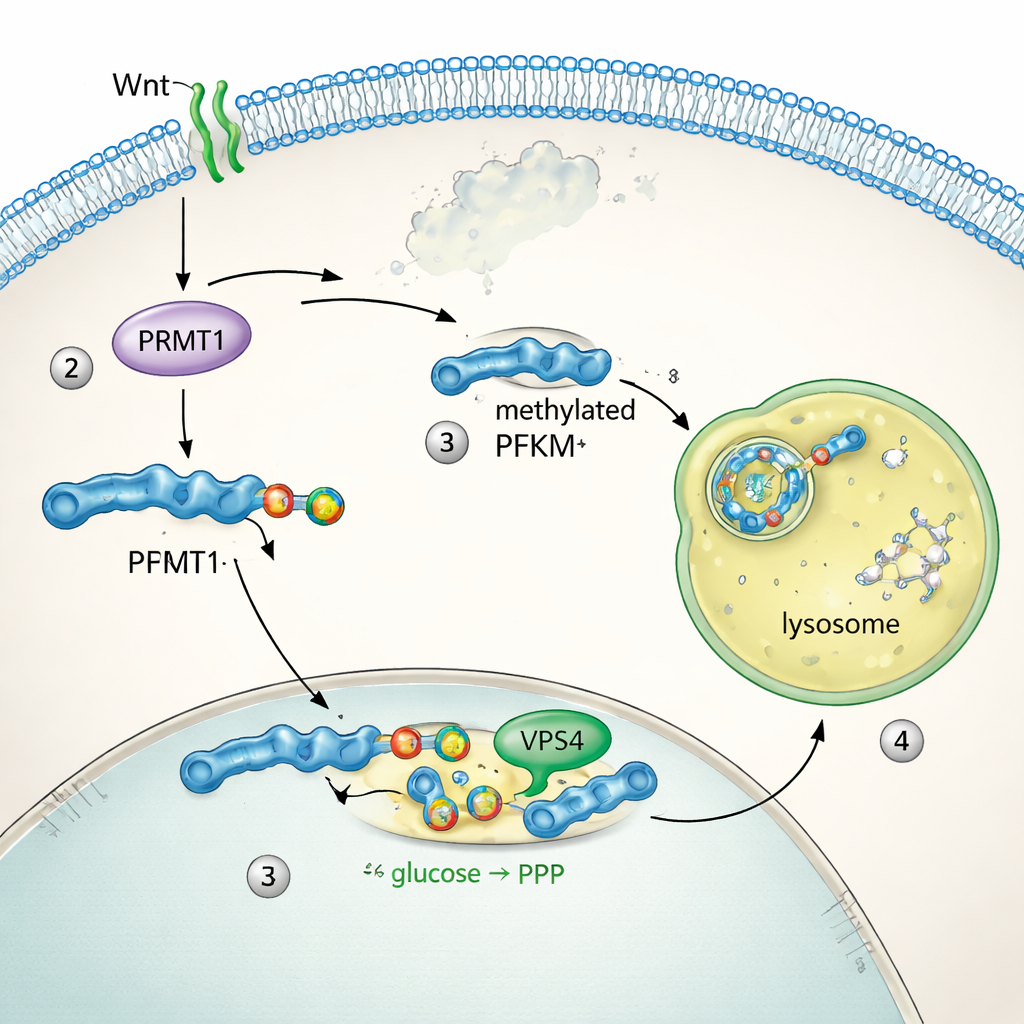
Znaczenie dla zdrowia i naprawy mięśni
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że komórki mięśniowe nie po prostu „spalają cukru” więcej lub mniej; świadomie przekierowują go między produkcją energii a ochroną komórkową w zależności od etapu życia. PFKM działa jak regulowany zawór w tym punkcie rozgałęzienia. W komórkach o cechach macierzystych oznaczanie prowadzane przez Wnt i lizosomalne niszczenie PFKM kieruje glukozę do ścieżki, która osłania komórki i przygotowuje je do przyszłego wzrostu. W miarę dojrzewania w pracujące włókna odbudowują zapasy PFKM i przesuwają metabolizm w stronę wysokowydajnego wytwarzania energii. Zakłócenie tej równowagi, jak w rzadkich chorobach związanych z niedoborem PFKM, zaburza prawidłowy rozwój mięśni. Odkrycie molekularnego uchwytu na tym przełączniku sugeruje, że przyszłe terapie mogłyby precyzyjnie modulować regenerację mięśni lub chronić mięśnie w chorobach i starzeniu poprzez łagodne dostosowanie aktywności PFKM lub dostarczanie odpowiednich metabolitów downstream.
Cytowanie: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Słowa kluczowe: różnicowanie mięśni szkieletowych, metabolizm glukozy, enzym PFKM, szlak pentozofosforanowy, lizosomalne rozkładanie białek