Clear Sky Science · pl
Ekspresja poza miejscem DHODH w cytozolu rozłącza de novo biosyntezę pirymidyn od mitochondrialnego transportu elektronów
Dlaczego przerwanie ukrytego powiązania w naszych komórkach ma znaczenie
Każda komórka w twoim ciele musi nieustannie kopiować i naprawiać swoje DNA, co wymaga stałych dostaw chemicznych „liter” zwanych pirymidynami. U większości zwierząt wytwarzanie tych liter jest ściśle powiązane z tym, jak mitochondria — elektrownie komórkowe — spalają paliwo przy użyciu tlenu. To sprzężenie oznacza, że gdy oddychanie mitochondrialne zawodzi, brakuje składników do budowy DNA i komórki mają trudności z wzrostem. Badanie podsumowane tutaj pokazuje, że zapożyczenie pojedynczego genu od drożdży piekarniczych potrafi jasno rozłączyć te dwa procesy. Taka modyfikacja genetyczna pozwala komórkom ssaczym utrzymywać produkcję liter DNA nawet gdy ich mitochondria są uszkodzone, otwierając nową drogę do badania, a może pewnego dnia leczenia, chorób napędzanych wadami metabolizmu energetycznego.
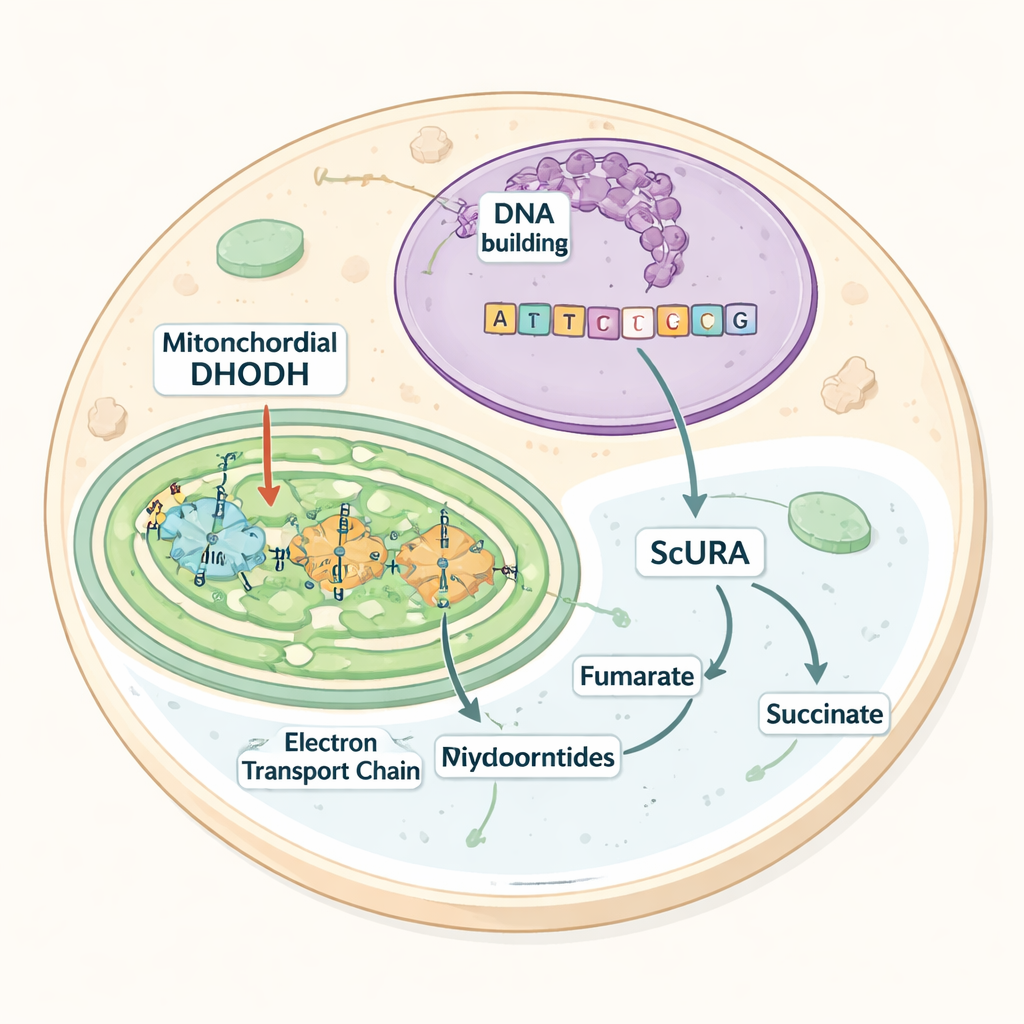
Narzędzie zapożyczone od drożdży
Praca koncentruje się na enzymie o nazwie dehydrogenaza dihydroorotanowa (DHODH), który wykonuje kluczowy etap w syntezie pirymidyn. U ssaków DHODH jest osadzony w wewnętrznej błonie mitochondrium i przekazuje elektrony do nośnika zasilającego łańcuch oddechowy. Jeśli przepływ elektronów zostanie zablokowany — na przykład przez inhibitory lekowe lub defekty genetyczne — DHODH przestaje działać, produkcja pirymidyn ustaje, a komórki stają się zależne od dietetycznego lub dostarczonego urydyny, gotowego składnika. Wiele drobnoustrojów żyjących bez tlenu omija ten wąskie gardło, używając alternatywnych wersji DHODH, które unoszą się w płynie komórkowym i korzystają z innych akceptorów elektronów. Autorzy zastanawiali się, czy mogą wprowadzić taką tlenoniezależną drogę do komórek ssaczych.
Przeprogramowanie sposobu wytwarzania liter DNA
Naukowcy wprowadzili gen URA1 z drożdży Saccharomyces cerevisiae do komórek ludzkich. URA1 koduje enzym cytosolowy, nazwany ScURA, który wykonuje ten sam krok chemiczny co mitochondrialny DHODH, ale przekazuje elektrony do cząsteczki zwanej fumaranem zamiast do mitochondrialnego nośnika. Testy biochemiczne wykazały, że ScURA tworzy aktywne dymery w cytozolu i dodaje nową, oporną na leki aktywność DHODH. W normalnych warunkach dodanie ScURA nie zakłócało struktury mitochondriów, oddychania ani wzrostu, co wskazuje, że działa jako ścieżka zapasowa, a nie dodatkowe obciążenie.
Komórki, które nie przejmują się przeszkodami mitochondrialnymi
Aby sprawdzić, czy ta rezerwowa ścieżka może zastąpić układ natywny, zespół chemicznie zablokował albo samą DHODH, albo łańcuch transportu elektronów mitochondriów — zabiegi, które zazwyczaj zatrzymują podział komórek, jeśli nie dostarczyć urydyny. Komórki wyrażające ScURA nadal proliferowały bez żadnej pomocy, nawet przy silnej inhibicji kompleksu oddechowego III lub po genetycznym usunięciu endogennego genu DHODH. Szczegółowe śledzenie atomów azotu i węgla z znakowanego glutaminą wykazało, że komórki z ScURA dalej syntetyzowały nukleotydy pirymidynowe pomimo tych blokad. Pomiary metabolitów ujawniły, że zamiast gromadzić toksyczne prekursory, komórki ScURA kierowały elektrony do fumaranów, produkując bursztynian i subtelnie przekształcając cykl kwasu trójkarboksylowego (TCA), by wspierać wymianę fumaran–bursztynian między cytozolem a mitochondriami.
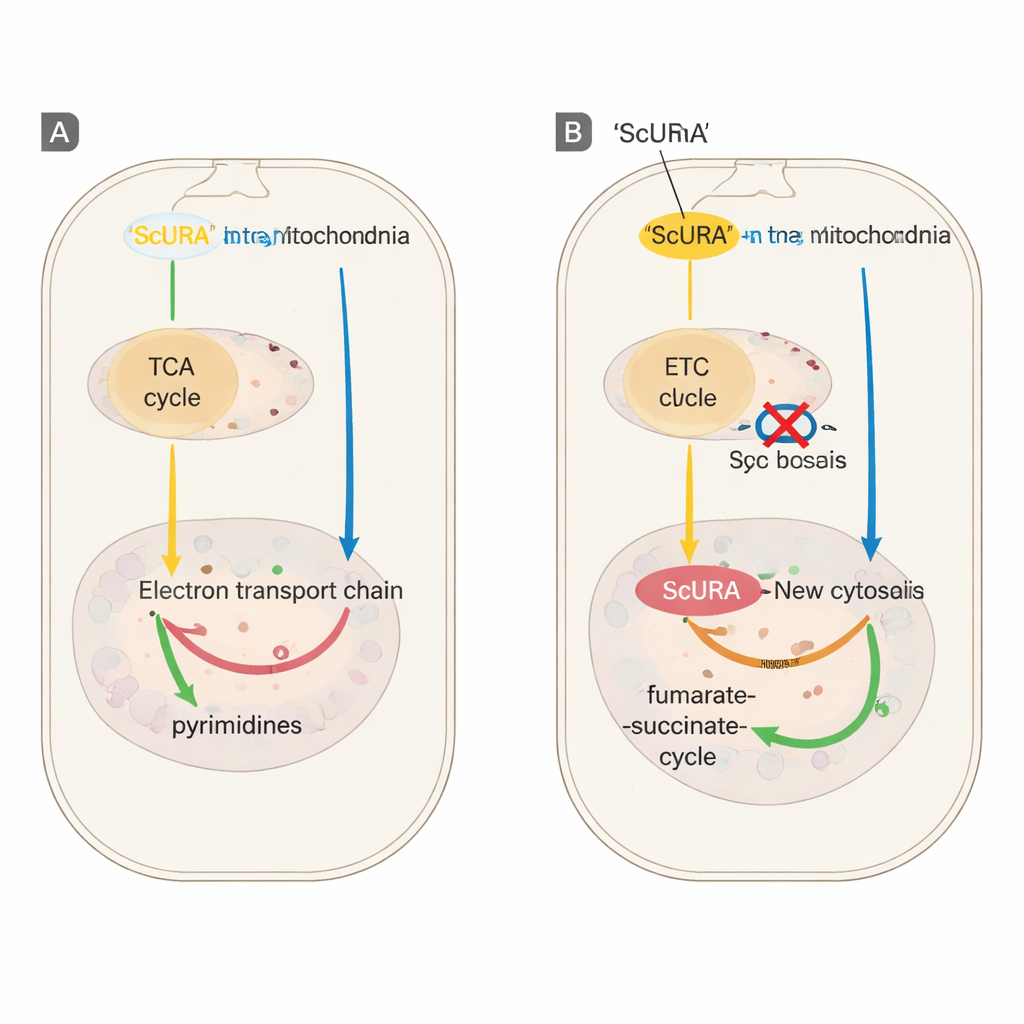
Ratowanie komórek z uszkodzonymi elektrowniami
Autorzy następnie przetestowali ScURA w modelach komórkowych chorób mitochondrialnych. Komórki pozbawione DNA mitochondrialnego lub niosące mutacje kaleczące kompleksy oddechowe III lub IV zwykle polegają na dodanej urydynie, by rosnąć. Po inżynierii polegającej na ekspresji ScURA te różne mutanty mogły proliferować bez urydyny, chociaż nadal wymagały pirogronianu, co odzwierciedla pozostające zapotrzebowanie na pewną aktywność mitochondrialną. Na poziomie ekspresji genów ScURA zapobiegała też wyciszeniu genów białek rybosomalnych, które zwykle następuje po przewlekłej inhibicji transportu elektronów, utrzymując zapasy pirymidyn wystarczająco wysokie, by podtrzymać produkcję RNA.
Co to oznacza dla zdrowia i chorób
Poprzez jasne oddzielenie syntezy pirymidyn od oddychania mitochondrialnego, ScURA daje badaczom potężną dźwignię: teraz mogą w wielu sytuacjach pytać, czy dany defekt lub efekt leku rzeczywiście wynika ze straty produkcji energii, czy raczej z niedoboru prekursorów DNA i RNA. W dłuższej perspektywie podobne strategie mogą uzupełniać istniejące terapie genowe chorób mitochondrialnych lub pomóc wyjaśnić, dlaczego niektóre nowotwory tak silnie polegają na przywróceniu funkcji mitochondriów. Choć przeniesienie enzymu drożdżowego do terapii ludzkiej wymaga dużej ostrożności, to badanie pokazuje, że pojedynczy, dobrze dobrany gen potrafi przepisać fundamentalne połączenie metaboliczne, które ewolucja długo utrzymywała splecione.
Cytowanie: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Słowa kluczowe: metabolizm pirymidyn, funkcja mitochondriów, łańcuch transportu elektronów, przeprogramowanie metaboliczne, choroba mitochondrialna