Clear Sky Science · pl
Regulowany przez karmienie metabolizm glikogenu napędza rytmiczne wydzielanie białek przez wątrobę
Dlaczego dobowy rytm wątroby ma znaczenie
Większość z nas myśli o tym, co jemy, ale rzadko o tym, kiedy nasza wątroba cicho pakuje i wysyła do krwiobiegu niezbędne białka. To badanie pokazuje, że „grafik wysyłek” wątroby wcale nie jest stały: podąża za dobowym rytmem, który silnie zależy od pory jedzenia i od tego, jak wątroba wykorzystuje zmagazynowany cukier zwany glikogenem. Zrozumienie tego zegara pomaga wyjaśnić, dlaczego pory posiłków, otyłość i niektóre rzadkie choroby genetyczne mogą zaburzać hormony, czynniki krzepnięcia i wiele innych białek krwi utrzymujących równowagę organizmu.
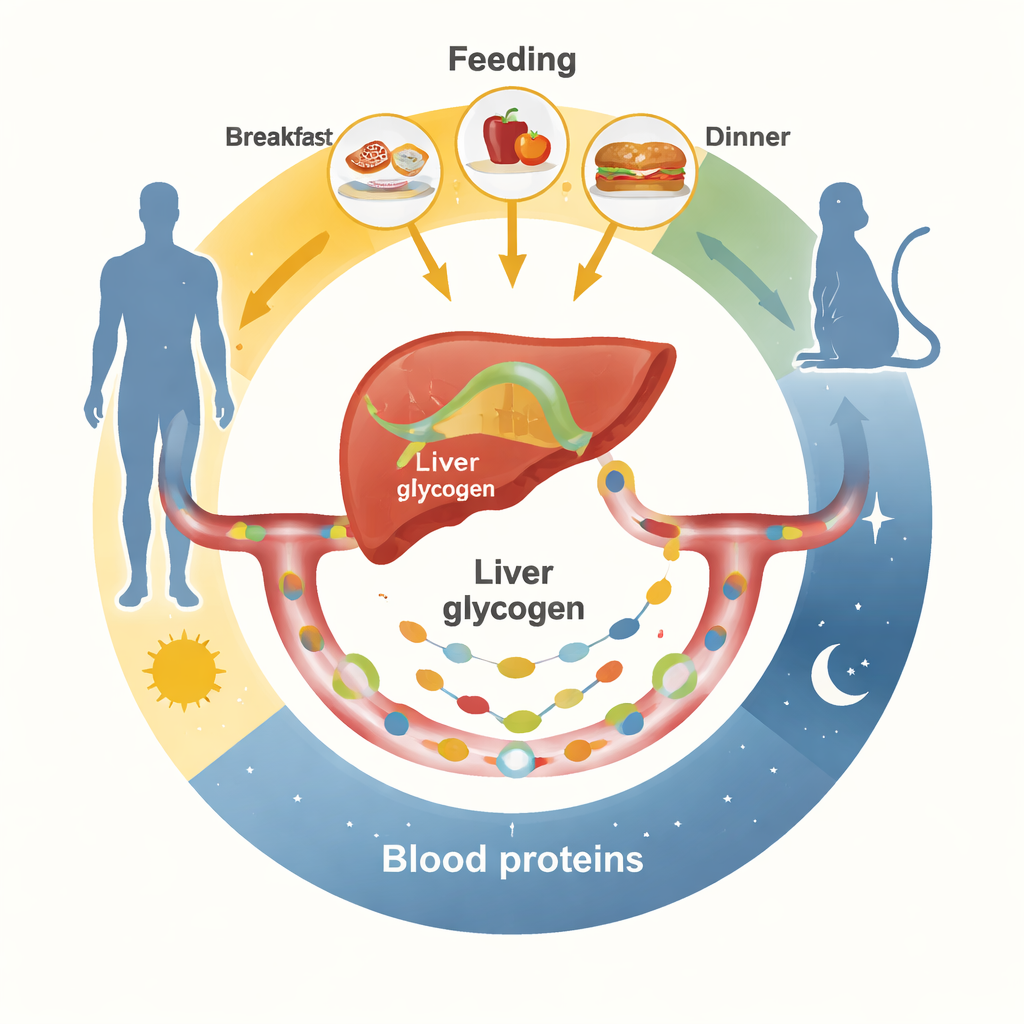
Posiłki nadają rytm białkom krwi
Naukowcy najpierw śledzili setki białek we krwi przez 24 godziny u zdrowych mężczyzn pod dwiema kontrolowanymi strategiami żywieniowymi. W jednym scenariuszu ochotnicy jedli regularne posiłki; w drugim te same kalorie były rozłożone równomiernie w ciągu dnia. Przy regularnych posiłkach wiele białek krwi wzrastało i opadało w wyraźnych dobowych falach, często osiągając szczyt wczesnym rankiem i późnym popołudniem. Były to m.in. hormony metaboliczne, czynniki krzepnięcia, białka odpornościowe i transportery w dużej mierze produkowane przez wątrobę. Gdy jedzenie było przyjmowane powoli i ciągle, większość tych rytmów wygładzała się. Podobne eksperymenty na myszach, którym zapewniano pokarm albo cały czas, albo tylko w określonych dziennych lub nocnych oknach, wykazały, że zmiana harmonogramu karmienia silnie przekształcała, które białka we krwi są rytmiczne i kiedy osiągają szczyt.
Linia sekrecyjna wątroby działa jak zegar
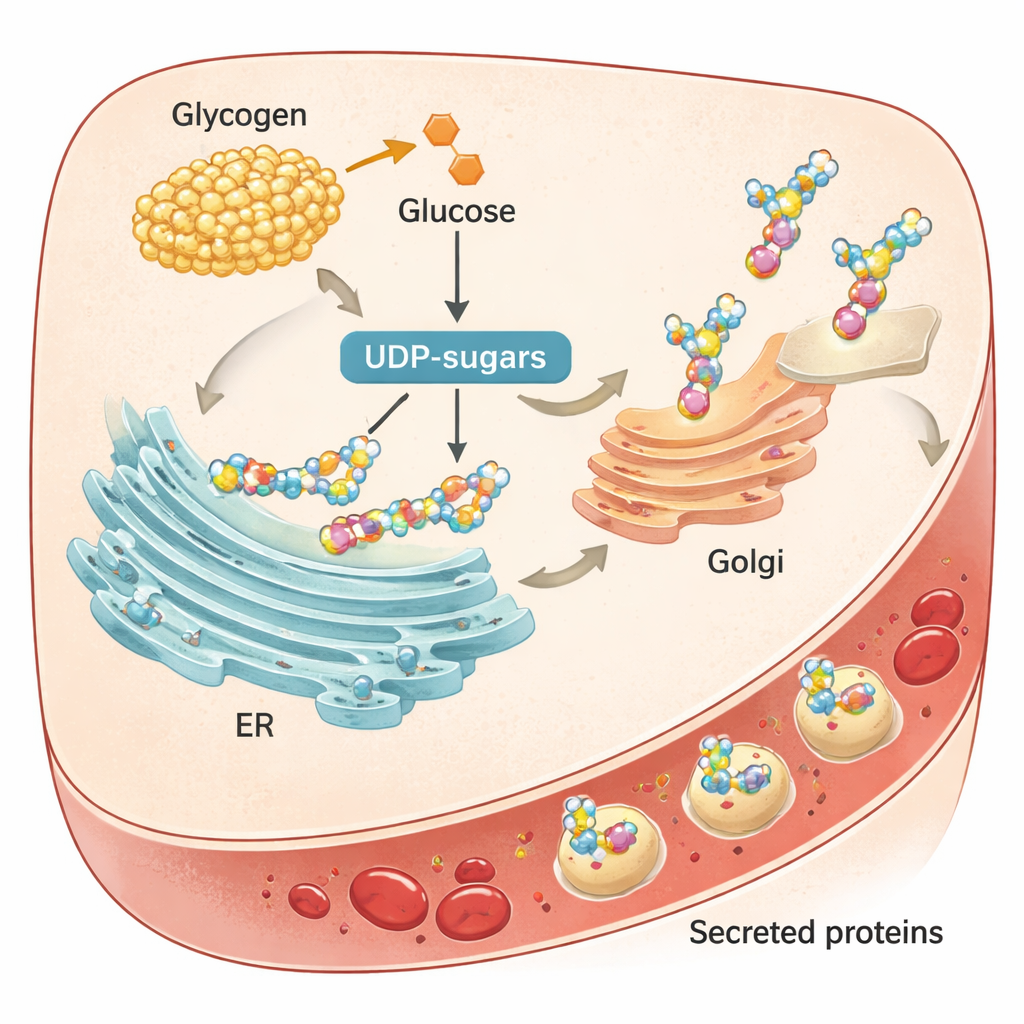
Aby dowiedzieć się, jak powstają te wzorce, zespół zajrzał do wnętrza wątroby. Stwierdzili, że białka zaangażowane w klasyczną „ścieżkę sekrecyjną” — gdzie nowo zsyntetyzowane białka wchodzą do siateczki śródplazmatycznej (ER), są modyfikowane w aparacie Golgiego, a następnie uwalniane — również wykazują dobowe wzrosty i spadki. Zamiast ciągłej taśmy produkcyjnej, ta ścieżka jest dostrojona do pory dnia. Większość rytmicznych białek krwi miała molekularne „peptydy sygnałowe” kierujące je tą drogą, a zablokowanie transportu ER–Golgi w plasterkach wątroby myszy radykalnie zmniejszyło uwalnianie białek. Natomiast markery uszkodzenia komórek i degradacji białek nie wykazywały silnych dobowych zmian, co wskazuje, że to wydzielanie, a nie degradacja, jest główną siłą napędową obserwowanych rytmów w krwi.
Glikogen: zapasowy cukier napędzający pakowanie białek
Autorzy powiązali następnie te efekty czasowe z tym, jak wątroba gospodaruje glikogenem, swoim głównym magazynem węglowodanów. Po posiłkach wątroba gromadzi glikogen; podczas postu rozkłada go w procesie zwanym glikogenolizą. Produkty rozpadu trafiają do „UDP-cukrów”, aktywowanych jednostek cukrowych wykorzystywanych do ozdabiania białek łańcuchami cukrowymi — modyfikacji zwanej glikozylacją. U myszy poziomy UDP-cukrów silnie oscylowały w ciągu dnia, zgodnie z aktywnością enzymów budujących i rozkładających glikogen. Gdy zespół zablokował kluczowy wątrobowy enzym glikogenolizy PYGL za pomocą leku, glikogen się kumulował, poziom cukru we krwi spadał podczas postu, a zasoby UDP-cukrów się zmniejszyły. Doprowadziło to do mniejszej glikozylacji białek wątroby, oznak stresu w ER i zmniejszonego wydzielania kilku ważnych białek do krwi.
Sygnały stresu i związki z chorobami
Zakłócenie rozkładu glikogenu zrobiło więcej niż tylko spowolnić eksport białek; uruchomiło system alarmowy kontroli jakości komórki. Komórki wątrobowe traktowane lekiem blokującym PYGL aktywowały odpowiedź na nieprawidłowo sfałdowane białka (unfolded protein response), zestaw szlaków stresu ER, które mogą zwiększać degradację białek i selektywnie zmieniać, które białka są wydzielane. U otyłych myszy, które naturalnie mają zmienione gospodarowanie glikogenem, normalne dobowe wahania glikogenu były stłumione, a liczba rytmicznych białek we krwi zmalała. Podobnie działo się u normalnych myszy poddanych ograniczonemu czasowi karmienia, co efektywnie zmniejszało kalorie. Wreszcie, w dużym ludzkim badaniu genetycznym osoby noszące warianty w genach związanych z chorobami magazynowania glikogenu lub wrodzonymi zaburzeniami glikozylacji wykazywały zmienione poziomy wielu białek we krwi, co wzmacnia związek między metabolizmem glikogenu, glikozylacją białek i ich wydzielaniem.
Co to oznacza dla zdrowia codziennego
Dla czytelnika niebędącego specjalistą przesłanie jest takie: wątroba prowadzi czasowy eksport białek do krwi, używając zmagazynowanego cukru jako paliwa niezbędnego do właściwego pakowania i uwalniania. Gdy wzorce karmienia, wewnętrzne zegary lub geny przetwarzające glikogen są zaburzone, harmonogram ten ulega rozregulowaniu, zmieniając poziomy hormonów, czynników krzepnięcia i białek odpornościowych w krwiobiegu. Zmiany te mogą pomagać wyjaśnić, dlaczego pory posiłków, otyłość i niektóre rzadkie schorzenia metaboliczne wiążą się z szerokim spektrum problemów zdrowotnych. Praca sugeruje, że nie tylko to, co jemy, ale także kiedy jemy, może wpływać na dobowy rytm „wysyłek” wątroby — i że lekarze mogą potrzebować brać pod uwagę porę dnia i harmonogram jedzenia przy interpretacji wyników badań krwi.
Cytowanie: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
Słowa kluczowe: rytmy dobowe, glikogen wątroby, wydzielanie białek, pory posiłków, metabolizm