Clear Sky Science · pl
Przepływ katabolizmu cysteiny regulowany przez Lamin A/C modyfikuje los komórek macierzystych poprzez przeprogramowanie epigenomu
Jak szkielet komórkowy rozmawia z metabolizmem
Dlaczego niektóre komórki pozostają młode i plastyczne w swoich możliwościach różnicowania, podczas gdy inne starzeją się lub utkną w niewłaściwej tożsamości? To badanie odsłania zaskakującą konwersację wewnątrz komórek między „rusztowaniem” jądra, które formuje DNA, a zawierającym siarkę składnikiem odżywczym — cysteiną. Pokazując, jak ten dialog kieruje komórki macierzyste ku zdrowym losom — albo ku przedwczesnemu starzeniu — praca sugeruje, że to, co komórki „spożywają” i jak to przetwarzają, mogłoby w przyszłości zostać dostrojone, by zapobiegać niektórym chorobom genetycznym, a może nawet spowalniać aspekty starzenia.
Ukryta rola powłoki jądrowej
Głęboko w każdej komórce DNA przylega do sieci białkowej zwanej blaszką jądrową, zbudowanej częściowo z białek lamin A i C. Te laminy nie tylko nadają jądru kształt; pomagają też decydować, które geny są zamknięte, a które pozostają dostępne. Autorzy badali mysie embrionalne komórki macierzyste w ich najbardziej plastycznym, „naiwnym” stanie i stwierdzili, że lamin A/C normalnie kontroluje dwie enzymatyczne osoby metaboliczne, CBS i CTH, które uczestniczą w tworzeniu i rozkładzie cysteiny. Gdy lamin A/C jest obecny i aktywny, te enzymy są powstrzymywane, a przetwarzanie cysteiny pozostaje niskie, co wspiera stabilny, młody stan komórki macierzystej. 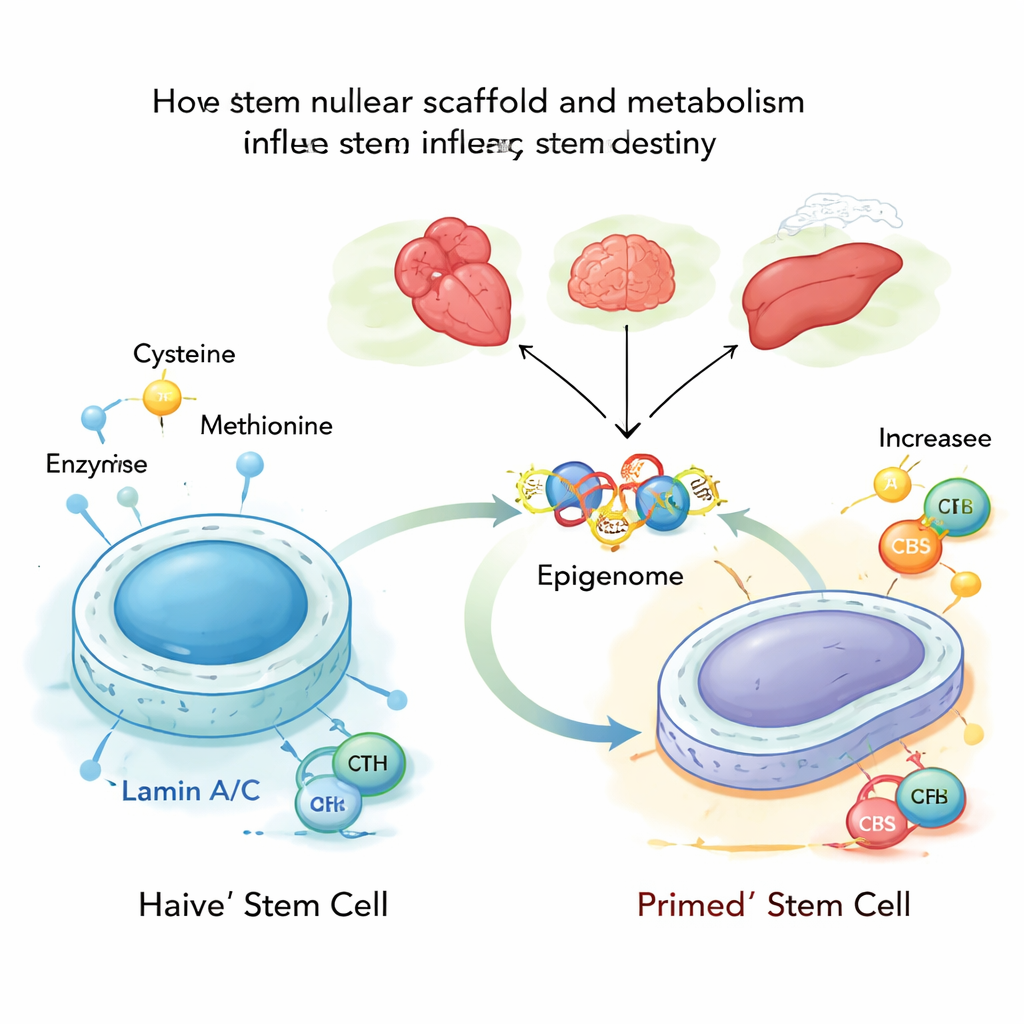
Kiedy struktura zawodzi, metabolizm przyspiesza
Następnie badacze usunęli lamin A/C lub wprowadzili mutację związaną z chorobą, która naśladuje ludzkie zaburzenie przedwczesnego starzenia zwanе Hutchinson–Gilford progeria. Bez prawidłowego lamin A/C geny CBS i CTH stają się bardziej dostępne i mocniej wiążą się z czynnikiem transkrypcyjnym SP1, co je aktywuje. Ta zmiana kieruje więcej cysteiny przez szlak metaboliczny prowadzący do acetyl‑CoA, małej cząsteczki przenoszącej grupy acetylowe używane do rozluźniania upakowania DNA. W miarę jak cysteina jest coraz bardziej skierowywana do acetyl‑CoA, grupy acetylowe są preferencyjnie dodawane do określonych miejsc na białkach histonowych — zwłaszcza dwóch pozycji w histonie H3 znanych jako K9 i K27 — ułatwiając włączanie pobliskich genów.
Od chemicznych znaków do decyzji o losie komórki
Te zmiany w „znakach” histonów działają jak globalne przestrojenie panelu kontrolnego komórki. W naiwnych komórkach macierzystych zwiększenie poziomu CBS i CTH, albo po prostu dostarczenie większej ilości cysteiny, popycha komórki w kierunku bardziej zaawansowanego stanu „primed”, bliższego tworzeniu prawdziwych tkanek. Geny związane z rozwojem serca i innymi liniami różnicowania stają się bardziej aktywne, a trójwymiarowe fałdowanie DNA zmienia się, faworyzując te programy. Odwrotnie, zmniejszenie aktywności CBS i CTH lub ograniczenie cysteiny pomaga przywrócić bardziej naiwną, młodą tożsamość nawet wtedy, gdy blaszka jądrowa jest uszkodzona. W modelach embrionalnych to metaboliczne „przekładanie” prowadziło do zaburzonego formowania trzech listków zarodkowych — wczesnych cegieł budulcowych wszystkich narządów — i nieprawidłowego uprzedzenia ku komórkom mięśnia sercowego, chyba że CBS i CTH zostały wyrównane. 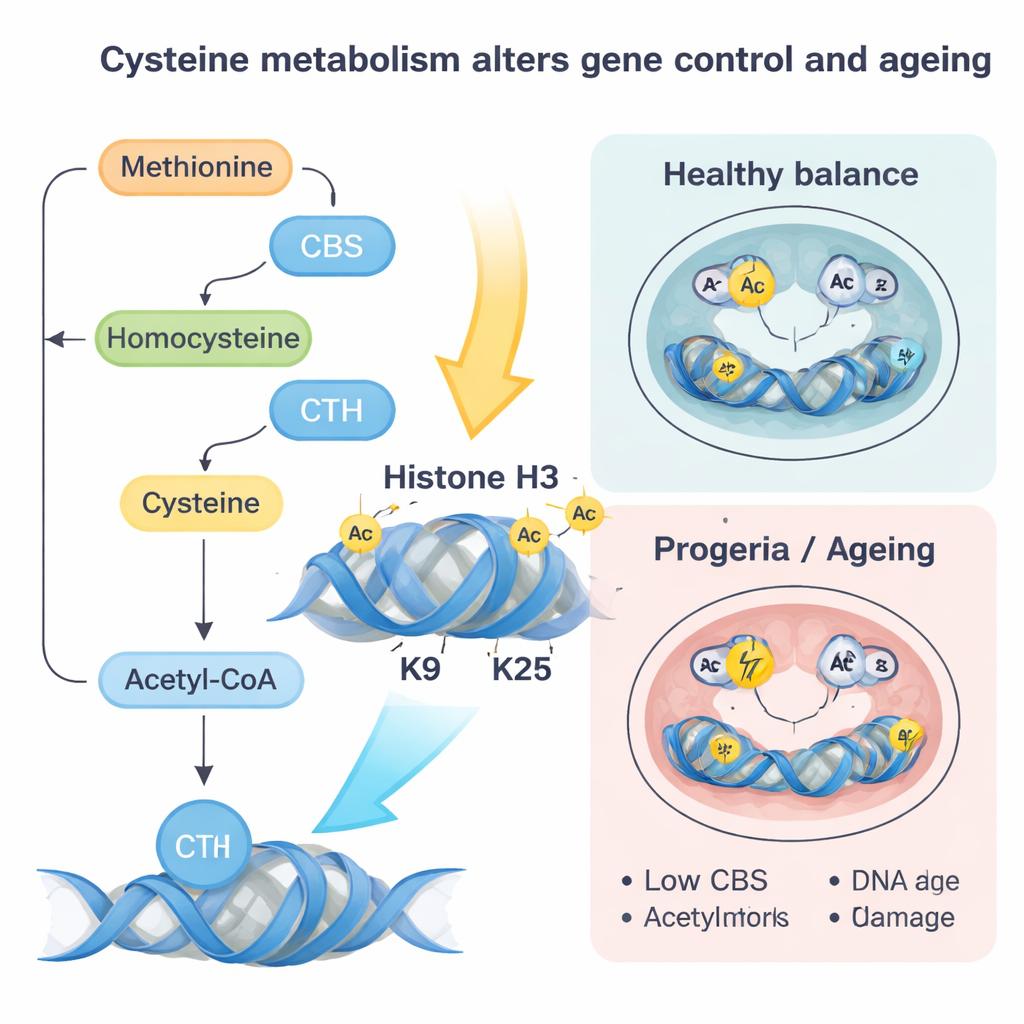
Metabolizm, znaczniki DNA i przedwczesne starzenie
Mutacja laminu przypominająca progerię opowiedziała komplementarną historię. W tym przypadku poziomy CBS i CTH spadają, redukując przepływ cysteiny i produkcję acetyl‑CoA z tej ścieżki. Jednocześnie homocysteina jest kierowana z powrotem do cyklu metioninowego, zwiększając poziomy SAM, uniwersalnego donora grup metylowych. To sprzyja dodatkowym znacznikom metylowym, zwłaszcza znacznikowi H3K9me3 umieszczanemu przez enzym SUV39H1, który uszczelnia chromatynę i wiąże się z upośledzoną naprawą DNA. Autorzy wykazali, że łagodne przywrócenie poziomu CBS lub ograniczenie metioniny obniżało SAM, zmniejszało te represyjne metylacje, poprawiało naprawę DNA, redukowało stres oksydacyjny i markery senescencji oraz częściowo ratowało różnicowanie komórek sercowych. Podobne spadki CBS i wzrosty represyjnych znaczników zaobserwowano w normalnie starzejących się sercach myszy oraz w ludzkich fibroblastach od starszych osób i pacjentów z progerią, co sugeruje, że ten obwód działa również w naturalnym starzeniu.
Co to oznacza dla zdrowia i starzenia
Dla czytelnika niebędącego specjalistą przesłanie jest takie: struktura komórkowa i jej metabolizm są ściśle powiązane — gdy powłoka jądrowa zbudowana z lamin A/C zostaje zaburzona, zmienia się sposób wykorzystania cysteiny, co z kolei przepisuje chemiczne markery na białkach pakujących DNA. Te markery decydują, które geny zostaną włączone podczas budowy ciała przez komórki macierzyste i wpływają na to, jak dobrze komórki naprawiają uszkodzenia przez całe życie. Poprzez ostrożne dostrojenie enzymów takich jak CBS i CTH — lub poprzez regulację podaży składników odżywczych, takich jak metionina i cysteina — może być możliwe skorygowanie części nieprawidłowego zapisywania tych znaków w chorobach związanych z laminami i być może złagodzenie aspektów przedwczesnego lub zwykłego starzenia.
Cytowanie: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Słowa kluczowe: komórki macierzyste, blaszkа jądrowa, metabolizm cysteiny, epigenetyka, starzenie się