Clear Sky Science · pl
Struktura i polidyspersyjność pojedynczych pęcherzyków lipidowych za pomocą mało-kątowego rozpraszania promieniowania X na European XFEL
Dlaczego małe bąbelki w wodzie mają znaczenie
Pęcherzyki lipidowe to mikroskopijne bąbelki zbudowane z tych samych rodzajów tłuszczowych cząsteczek, które tworzą błony komórkowe. Odgrywają kluczową rolę w dostarczaniu leków, kosmetykach oraz w transporcie hormonów i neuroprzekaźników przez komórki. Jednak ponieważ każdy pęcherzyk ma tylko kilkadziesiąt miliardowych części metra i znajduje się w wodzie, trudniej niż się wydaje zobaczyć jego szczegółową strukturę. W tym badaniu pokazano, jak badać pojedyncze pęcherzyki jeden po drugim za pomocą intensywnych błysków rentgenowskich, ujawniając nie tylko ich średnią strukturę, lecz także stopień ich zróżnicowania — informacje istotne zarówno dla biologii, jak i nanotechnologii.
Od rozmycia do przejrzystości pojedynczych cząstek
Przez dekady naukowcy używali metody zwanej mało-kątowym rozpraszaniem promieniowania X do badania miękkich materiałów, takich jak białka, nanocząstki i pęcherzyki lipidowe w roztworze. W typowym eksperymencie wąska wiązka promieniowania X przechodzi przez próbkę zawierającą astronomiczną liczbę kopii tego samego rodzaju cząstek. Wiązka ulega rozproszeniu, a otrzymany wzór zawiera informacje o ich ogólnym rozmiarze i wewnętrznej strukturze. Wadą jest to, że podejście to daje jedynie uśrednienia po bilionach cząstek, wszystkie w losowych orientacjach i o nieco różnych rozmiarach oraz kształtach. Wiele ciekawych szczegółów — na przykład jak szeroki jest rzeczywisty rozkład rozmiarów albo jak bardzo poszczególne cząstki odbiegają od idealnej sfery — zostaje przez to zatarte.
Zamrażanie ruchu ultrakrótkimi impulsami rentgenowskimi
Aby wyjść poza uśrednienia, autorzy wykorzystują rentgenowski laser swobodnego elektronu (XFEL) w ośrodku European XFEL. Urządzenie to generuje ultrakrótki, niezwykle jasny impuls rentgenowski trwający zaledwie kilka kwadrylionowych części sekundy. W tej chwili pojedynczy pęcherzyk może być zbadany, zanim intensywne promieniowanie zdąży go uszkodzić — koncepcja znana jako „dyfrakcja-przed-zniszczeniem”. Zespół stosuje rozpylacz aerozolowy, aby wyrzucać pojedyncze pęcherzyki z wody do próżni, gdzie krople szybko się schładzają i winktrystycznie (witrifikują), pozostawiając nienaruszone pęcherzyki otoczone cienką warstwą wody. Nanonastawiona wiązka rentgenowska, szeroka na tylko kilkaset nanometrów, uderza w jeden pęcherzyk na raz, a duży detektor rejestruje powstały wzór dyfrakcyjny.
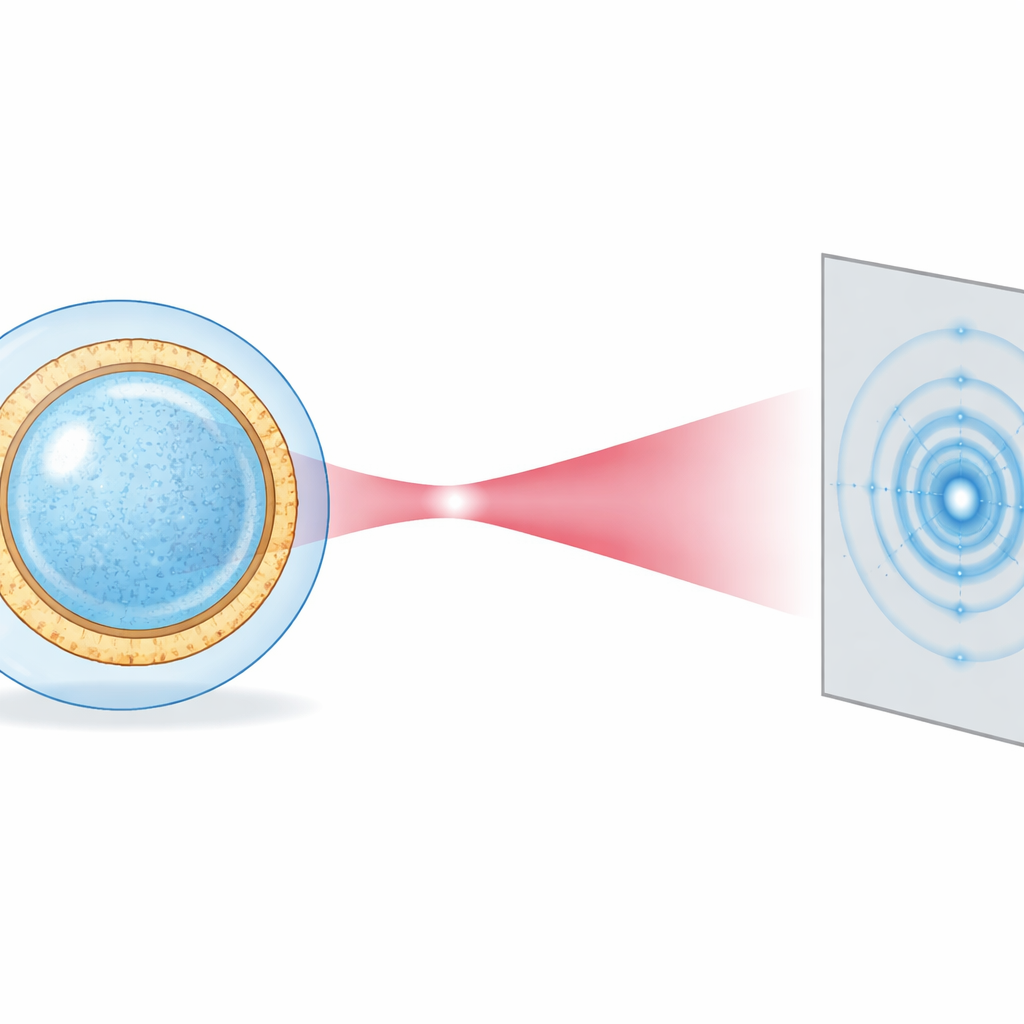
Przekształcanie wzorów w kształty i powłoki
Każdy pęcherzyk generuje słaby, pierścieniowy wzór zależny od jego promienia, odchylenia od idealnej sfery oraz szczegółowego rozmieszczenia bogatych elektronowo grup głowowych lipidów i bardziej rozproszonych ogonków tłuszczowych w membranie. Zamiast próbować rekonstruować pełny obraz piksel po pikselu — co wymaga wielu identycznych kopii — badacze dopasowują każdy wzór bezpośrednio do modelu fizycznego zapożyczonego z konwencjonalnego rozpraszania w roztworze. Pęcherzyk traktowany jest jako nieco spłaszczona sfera otoczona gładką wodną powłoką, a membrana opisana prostymi matematycznymi krzywymi dzwonowymi. Poprzez uśrednianie azymutalne każdego wzoru (przekształcając go w jednowymiarową krzywą) i przeprowadzanie dopasowań metodą najmniejszych kwadratów, wyodrębniają dla każdego pęcherzyka jego promień, eliptyczność (jak bardzo jest wydłużony lub spłaszczony) oraz oszacowanie wewnętrznego profilu gęstości membrany.
Mapowanie rzeczywistej zmienności
Dzięki pracy z dużą częstotliwością powtórzeń zespół rejestruje ponad milion obrazów podczas jednego przebiegu. Zautomatyzowane procedury „znajdowania trafień” wybierają te, które rzeczywiście zawierają pojedynczy pęcherzyk, a nie wiele cząstek czy puste strzały. Z tysięcy takich trafień badacze budują histogramy promieni i kształtów pęcherzyków. Okazało się, że pęcherzyki przygotowane jako sferyczne często stają się nieco spłaszczonymi elipsoidami podczas aerozolizacji, prawdopodobnie dlatego, że woda stopniowo opuszcza wnętrze, podczas gdy membrana pozostaje nawodniona z zewnątrz. Dane ujawniają również, jak silnie zróżnicowanie rozmiarów rozmywa charakterystyczne „falowania” krzywych rozpraszania oraz jak wybieranie podzbiorów pęcherzyków o podobnych promieniach lub kształtach — „oczyszczanie in silico” — przywraca bardziej wyraźne sygnały strukturalne dwuwarstwy membrany i jej cienkiej otaczającej warstwy wody.
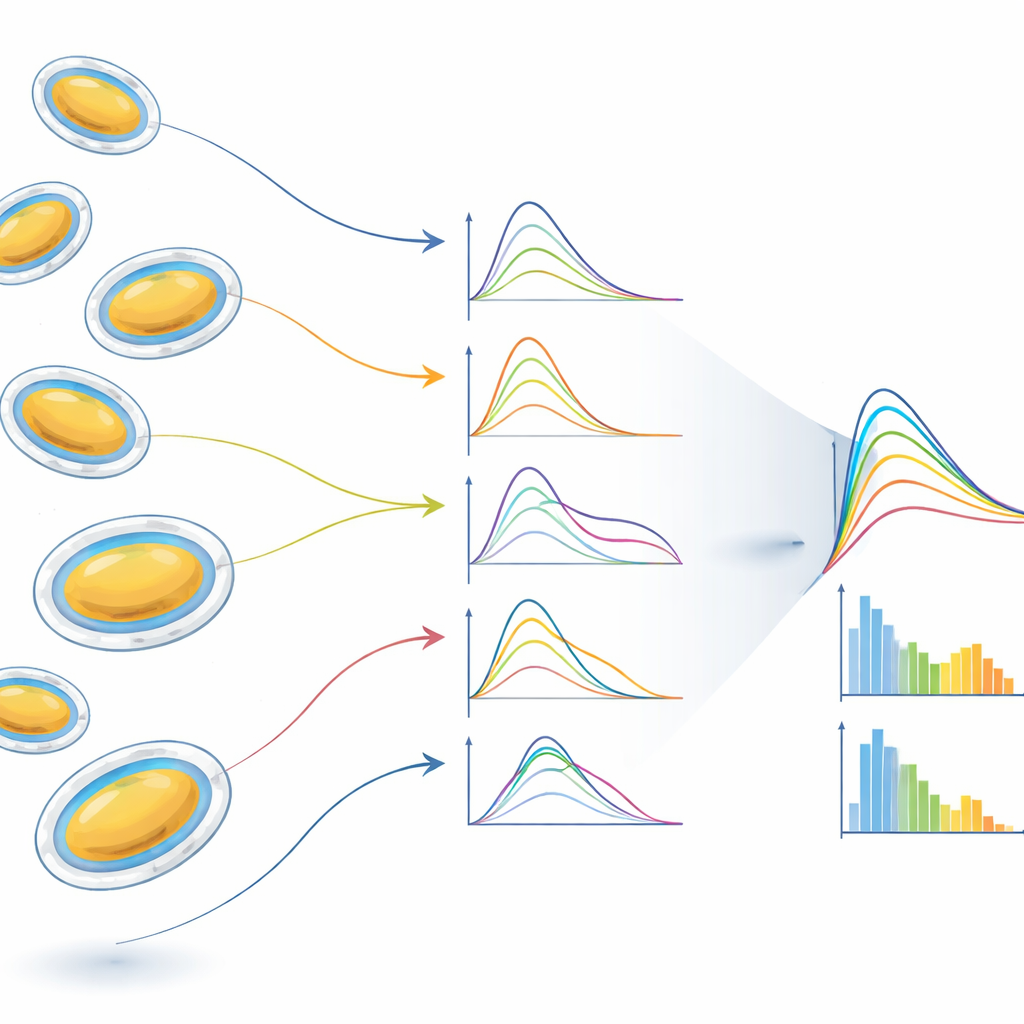
Nowe okno na miękkie nanostruktury
Łącząc impulsy XFEL, dostarczanie pojedynczych cząstek i analizę opartą na modelu, praca ta skutecznie sprowadza tradycyjne mało-kątowe rozpraszanie promieniowania X do poziomu pojedynczych pęcherzyków. Zamiast jednej średniej krzywej dla ogromnego zespołu, badacze mogą teraz uzyskać parametry strukturalne dla każdego pęcherzyka z osobna, a następnie celowo je pogrupować, by badać dobrze zdefiniowane podpopulacje. Umożliwia to zarówno zmniejszenie rozmycia spowodowanego polidyspersyjnością, jak i szczegółowe zmierzenie tej polidyspersyjności. Podejście ma szerokie zastosowanie w delikatnych systemach biologicznych i miękkich materiałach, które z natury są heterogeniczne — od liposomów niosących leki i proteo-liposomów po bardziej złożone przedziały komórkowe — otwierając drogę nie tylko do lepszych pomiarów struktury statycznej, lecz ostatecznie także do filmów w czasie rzeczywistym pokazujących zmiany strukturalne wyzwalane światłem lub innymi bodźcami.
Cytowanie: Neuhaus, C., Stammer, M.L., Alfken, J. et al. Structure and polydispersity of single lipid vesicles by small-angle X-ray scattering at European XFEL. Commun Phys 9, 93 (2026). https://doi.org/10.1038/s42005-026-02551-5
Słowa kluczowe: pęcherzyki lipidowe, sylotron rentgenowski (X-ray free-electron laser), mało-kątowe rozpraszanie promieniowania X, obrazowanie pojedynczych cząstek, nanobiotechnologia