Clear Sky Science · pl
ABEL-FRET wypełnia lukę czasową w pomiarach jednocząsteczkowych dynamiki strukturalnej receptora A2A adenozyny
Obserwacja maleńkich komórkowych przełączników w czasie rzeczywistym
Wiele współczesnych leków działa przez przełączanie molekularnych „włączników” na powierzchni komórek, zwanych receptorami. Te przełączniki nieustannie zmieniają kształt w trakcie włączania i wyłączania sygnałów, jednak większość narzędzi potrafi uchwycić jedynie bardzo najszybsze albo bardzo najwolniejsze ruchy — nie oba naraz. W artykule przedstawiono metodę pozwalającą obserwować pojedynczy receptor będący celem leku w roztworze znacznie dłużej niż wcześniej, ujawniając, jak utrzymuje się w określonych konformacjach istotnych dla działania leku.
Dlaczego te zmieniające kształt białka są ważne
Badanie koncentruje się na dużej klasie białek błonowych znanych jako receptory sprzężone z białkami G (GPCR). Białka te kontrolują kluczowe procesy, w tym widzenie, nastrój, ciśnienie krwi i odpowiedzi immunologiczne; ponad jedna trzecia zatwierdzonych leków działa na nie. Jeden z dobrze zbadanych przedstawicieli, receptor adenozyny A2A, pomaga regulować sen, ból, zapalenie i sygnalizację mózgową, i jest obiecującym celem w leczeniu schorzeń, takich jak choroba Parkinsona i nowotwory. GPCR są bardzo elastyczne: gdy różne cząsteczki wiążą się z receptorem, wypychają go w odmienne kształty faworyzujące konkretne ścieżki sygnalizacyjne. To właśnie ta elastyczność utrudnia projektowanie leków opartych na statycznych migawkach z rentgenografii czy krio‑elektronowej mikroskopii.
Śledzenie pojedynczego receptora bez unieruchamiania
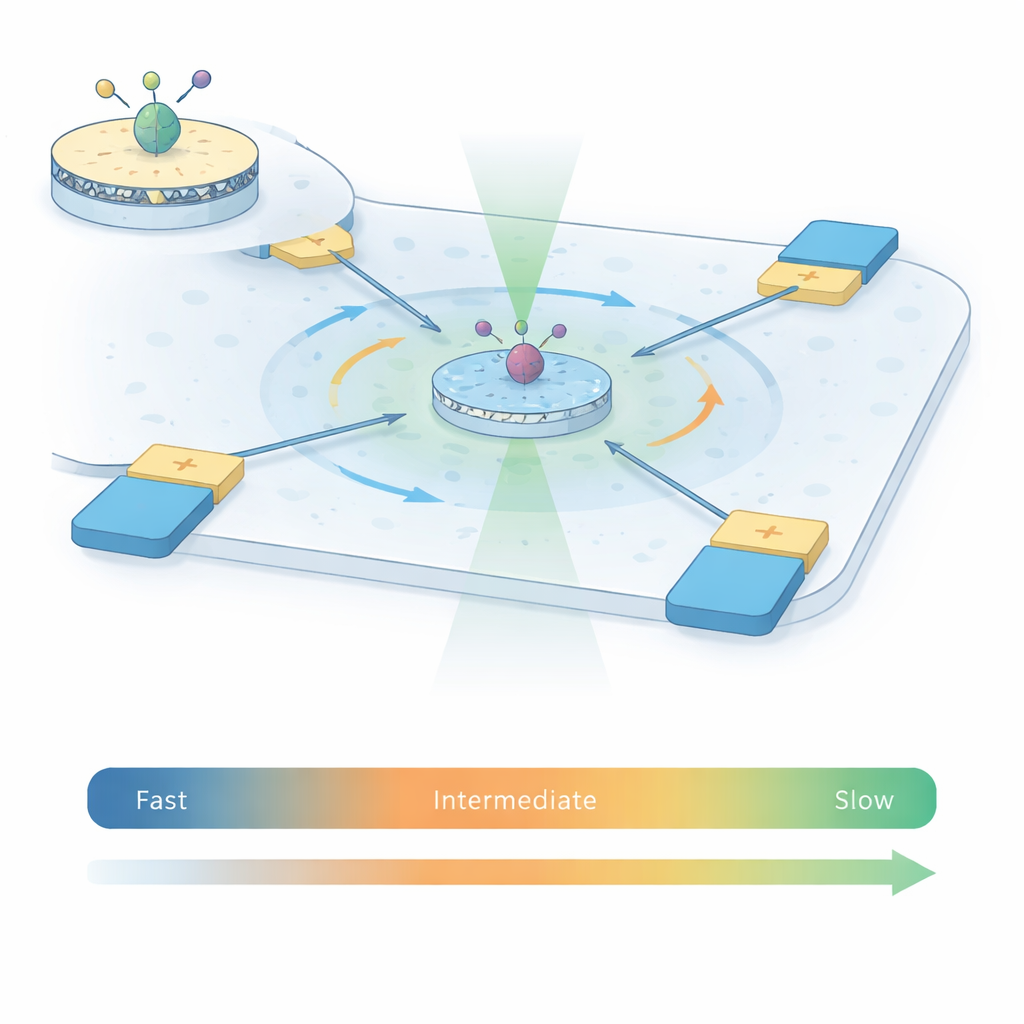
Aby uchwycić ruchy receptorów A2A, autorzy łączą dwie potężne techniki w podejście nazwane ABEL‑FRET. Po pierwsze, rekonstruują pojedyncze receptory w maleńkich fragmentach sztucznej błony zwanych nanodyskami, zapewniając każdemu białku bardziej naturalne środowisko niż detergent. Do wewnętrznych ruchomych elementów receptora przyczepiają parę fluorescencyjnych barwników. Gdy receptor zmienia kształt, zmienia się odległość i względna orientacja między tymi barwnikami, co wpływa na transfer energii między nimi — zjawisko znane jako rezonansowy transfer energii Förstera (FRET). Po drugie, zamiast przyklejać receptor do powierzchni, używają anty‑Brownowskiej elektrokinetycznej (ABEL) pułapki: mikrofluidycznej komory z elektrodami, które wykrywają pozycję fluorescencyjnej cząstki i delikatnie odprowadzają ją z powrotem do środka, przeciwdziałając przypadkowemu ruchowi Browna.
Wypełnianie brakującego przedziału czasowego
Tradycyjne eksperymenty jednocząsteczkowego FRET albo obserwują swobodnie dyfundujące receptory przez zaledwie kilka tysięcznych sekundy, albo unieruchomione receptory na powierzchni przez sekundy do minut. Każde podejście obejmuje inny przedział czasowy. Dzięki pułapce ABEL to badanie utrzymuje indywidualne receptory A2A w polu widzenia przez jedną do dwóch sekund, przy czym pozostają one wolne w roztworze — czyli około 100 razy dłużej niż w eksperymentach ograniczonych dyfuzją. Ten wydłużony czas obserwacji pozwala zespołowi zmierzyć, jak sygnał FRET fluktuuje w trakcie każdego zatrzymania oraz wśród tysięcy receptorów, w czterech warunkach: bez liganda, z antagonistą oraz z dwoma różnymi cząsteczkami aktywującymi (agonistami). Narzędzia statystyczne zapożyczone z analizy sygnałów — wariancja, korelacja i analizy rekurencji — pozwalają odróżnić losowy szum fotonowy od rzeczywistych, powolnych zmian strukturalnych receptora.
Ujawnione ukryte, długotrwałe kształty
Odczyty FRET pokazują, że receptory zajmują wiele odrębnych konformacji, które nie zamieniają się w pełni w trakcie typowych czasów obserwacji rzędu kilkuset milisekund. We wszystkich warunkach rozkład wartości FRET jest znacznie szerszy niż oczekiwano wyłącznie z powodu szumu, ujawniając heterogeniczność strukturalną: różne cząsteczki pozostają w różnych, długo żyjących kształtach. Gdy wiążą się cząsteczki aktywujące, średni poziom FRET przesuwa się w górę, co wskazuje, że receptor spędza więcej czasu w ułożeniu „przypominającym aktywne” wewnętrznych helis. Jednak nawet wtedy analizy korelacji pokazują, że gdy receptor znajduje się w stanie o wysokim lub pośrednim FRET, istnieje duża szansa, że pozostanie tam przynajmniej przez setki milisekund. Wyniki te aktualizują wcześniejsze oszacowania oparte na szybszych eksperymentach, wydłużając charakterystyczne „czasy pobytu” w długo żyjących stanach z zaledwie milisekund do znacznie ponad jednej dziesiątej sekundy.
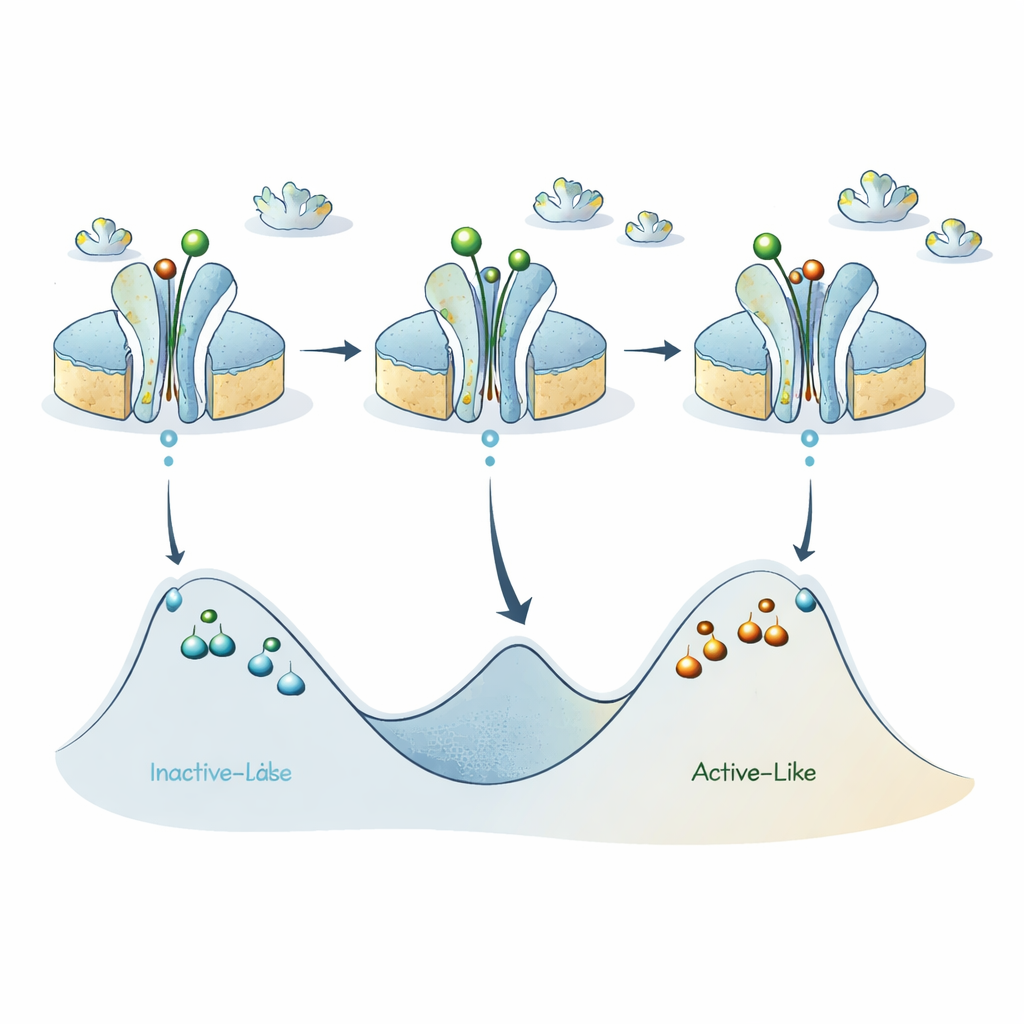
Nowa mapa krajobrazu energetycznego receptora
Łącząc te elementy, autorzy dopracowują wcześniejszy model, w którym receptor A2A przełącza się głównie między stanem przypominającym nieaktywny a stanem przypominającym aktywny. Nowe dane sugerują, że każda z tych dwóch szerokich kategorii w rzeczywistości ukrywa kilka podstanów oddzielonych znacznymi barierami energetycznymi, tak że pojedyncze receptory mogą pozostawać „utknięte” w danej wersji stanu aktywnego lub nieaktywnego przez zaskakująco długi czas. Ligandy aktywujące obniżają barierę między głównymi basenami nieaktywnym i aktywnym, sprzyjając szybszemu przełączaniu na podmilisekundowej skali, ale wewnętrzne bariery w obrębie każdego basenu pozostają wysokie, powodując powstawanie długo żyjących podstanów wykrywanych przez ABEL‑FRET.
Co to znaczy dla przyszłych leków
Dla czytelników nietechnicznych kluczowy wniosek jest taki, że cel leku, taki jak receptor A2A, nie przełącza się po prostu między „wyłączony” a „włączony”. Zamiast tego eksploruje nierówny krajobraz kształtów, z których niektóre utrzymują się wystarczająco długo, by mieć znaczenie dla sposobu przekazywania sygnałów wewnątrz komórek i działania leków w czasie. Dzięki wydłużeniu czasu, przez jaki pojedyncze receptory można obserwować w ich naturalnym, nieprzywiązanym stanie, ABEL‑FRET wypełnia istotną lukę między ultrakrótkimi a bardzo wolnymi pomiarami. Podejście to można teraz zastosować do wielu białek błonowych, oferując pełniejszy, rozdzielony w czasie obraz tego, jak potencjalne cele leków „oddychają”, zmieniają się i reagują na związki terapeutyczne.
Cytowanie: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Słowa kluczowe: Receptory sprzężone z białkami G, jednocząsteczkowy FRET, receptor adenozyny A2A, konformacyjne dynamiki białek, pułapka ABEL