Clear Sky Science · pl
Głębokość pozycji wiążącej modyfikuje skuteczność fotoswitchowalnych ligandów w receptorze 5-HT2A
Światło ujawnia przełączalne leki mózgowe
Wyobraź sobie lek, który można włączać i wyłączać błyskiem światła, precyzyjnie sterując receptorami mózgu i ograniczając skutki uboczne. Badanie to dotyczy dokładnie takiej koncepcji dla kluczowego receptora serotoniny związanego z nastrojem, percepcją i działaniem psychodelików. Naukowcy zbadali, dlaczego dwie niemal identyczne światłoczułe cząsteczki zachowują się tak różnie — jedna działa niemal jak idealny przełącznik on/off, druga zaś uporczywie odmawia całkowitego wyłączenia. Wyjaśnienie sprowadza się do zaskakująco prostej kwestii: jak głęboko cząsteczka osiada w receptorze.
Leki sterowane światłem w mózgu
Leki aktywowane światłem, zwane także narzędziami fotofarmakologicznymi, projektuje się tak, by wiązka światła przełączała część cząsteczki między dwoma kształtami — na przykład zgiętym i prostym. Te kształty mogą zmieniać siłę przyłączenia leku do celu. W tej pracy celem jest ludzki receptor 5-HT2A, białko na komórkach mózgowych reagujące na serotoninę i kluczowe zarówno dla efektów przeciwpsychotycznych, jak i psychodelicznych. Badane cząsteczki to pochodne N,N-dimetylotryptaminy (DMT) zmodyfikowane o światłoczułą jednostkę azobenzenu. Dwie wersje różnią się tylko położeniem małej grupy metoksy — albo w pozycji „para”, albo „meta” na pierścieniu — a mimo to ich zachowanie biologiczne pod wpływem światła jest diametralnie różne.
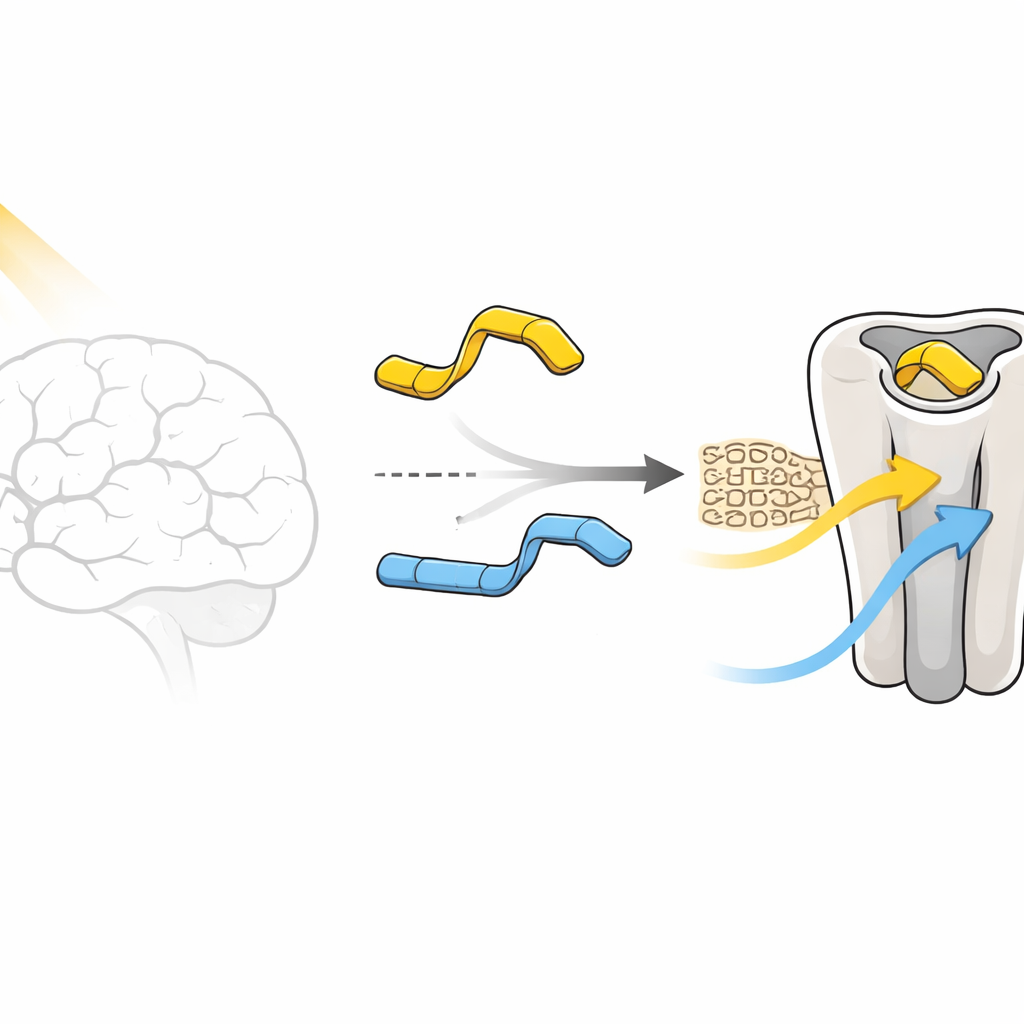
Dwie niemal bliźniacze cząsteczki, zupełnie inne przełączniki
W testach komórkowych wersja para, nazwana związkiem 1, zachowuje się prawie jak cyfrowy przełącznik. W ciemności jej forma „trans” ledwie aktywuje receptor, a nawet lekko go blokuje, działając jako słaby antagonista. Gdy światło przekształca ją w formę „cis”, ta sama cząsteczka staje się umiarkowanym aktywatorem, częściowo włączając receptor. Wersja meta, związek 2, nie współpracuje w ten sposób: zarówno jej formy świetlne, jak i ciemne utrzymują receptor w stosunkowo aktywnym stanie, nigdy nie dostarczając prawdziwego „wyłączenia”. Centralną zagadką pracy jest to, dlaczego tak minimalna korekta chemiczna — przesunięcie jednej małej grupy na pierścieniu — tak silnie zmienia odpowiedź receptora.
Zajrzeć do środka dzięki filmom na poziomie atomowym
Aby to rozwiązać, zespół zastosował rozległe, all-atomowe symulacje dynamiki molekularnej, w praktyce uruchamiając szczegółowe filmy każdego atomu w receptorze, otaczającej błonie, wodzie i każdym ligancie przez łącznie około 80 mikrosekund. Symulowali obie cząsteczki w obu ich kształtach sterowanych światłem oraz w formach nieaktywnych i aktywnych receptora 5-HT2A. Śledząc znane wewnętrzne „mikroprzełączniki” strukturalne w białku — takie jak kluczowy tryptofan, który się odwraca, most solny, który pęka, oraz ruch sodu i wody głęboko w jądrze — mogli ocenić, kiedy receptor skłania się ku stanowi wyłączonemu lub włączonemu. Porównali też, na ile nowe cząsteczki naśladują pozycję wiążącą LSD, dobrze przebadanego częściowego aktywatora, używając nakładania się systemów pierścieni jako wskazówki.
Głębokość ma większe znaczenie niż sam kształt
Główną obserwacją jest to, że skuteczność cząsteczek zależy przede wszystkim od tego, jak głęboko wchodzą w kieszeń wiążącą receptora. W nieaktywnym receptorze forma trans związku para tworzy specyficzny zestaw wiązań wodorowych, który ciągnie ją niezwykle głęboko, poniżej obszaru, gdzie zachodzą typowe kontakty aktywujące. To „nadmierne wnikanie” uniemożliwia jej dotknięcie kluczowych polarnych reszt, które pomagają przełączyć receptor w stan aktywny, przez co stabilizuje stan wyłączony. Forma trans związku meta nie może utworzyć tych samych kotwiczących kontaktów i zamiast tego znajduje się wyżej, w bardziej LSD-podobnej pozycji kompatybilnej z aktywacją, co tłumaczy jej pozostałą aktywność. Gdy światło przełącza obie cząsteczki do form cis, generalnie przesuwają się one w płytsze, bardziej aktywatoropodobne pozycje. Nawet wtedy jednak geometryczne uwarunkowania mają znaczenie: w aktywnym receptorze cis związek 2 może wsunąć się głębiej do hydrofobowego tunelu między dwoma helisami i utworzyć trwałe wiązanie wodorowe wzmacniające jego silne działanie agonistyczne, podczas gdy cis związek 1 jest sterycznie zablokowany przed tym.
Precyzyjna kontrola wewnętrznej wody i jonów
Symulacje pokazują też, że głębokość wiązania subtelnie dostraja wewnętrzną kieszeń sodową i szlak wodny, które są znane z wpływu na aktywację receptora. Głębokie, sztywne wiązanie przez związek para w formie trans utrzymuje jon sodu ściśle uwięziony, a otaczający obszar stosunkowo suchy — cechy związane ze stanem wyłączonym. Dla kontrastu, bardziej ruchome wiązanie związku meta lub form cis pozwala większej ilości wody wnikać i rozluźnia środowisko sodu, przygotowując receptor do aktywacji. Kluczowa aromatyczna reszta „przełącznika” może łatwiej zmienić orientację, gdy ligandy są elastyczne i nie są nadmiernie zakotwiczone, dodatkowo popychając receptor w stronę stanu przypominającego włączenie, szczególnie w przypadku cis związku 2.
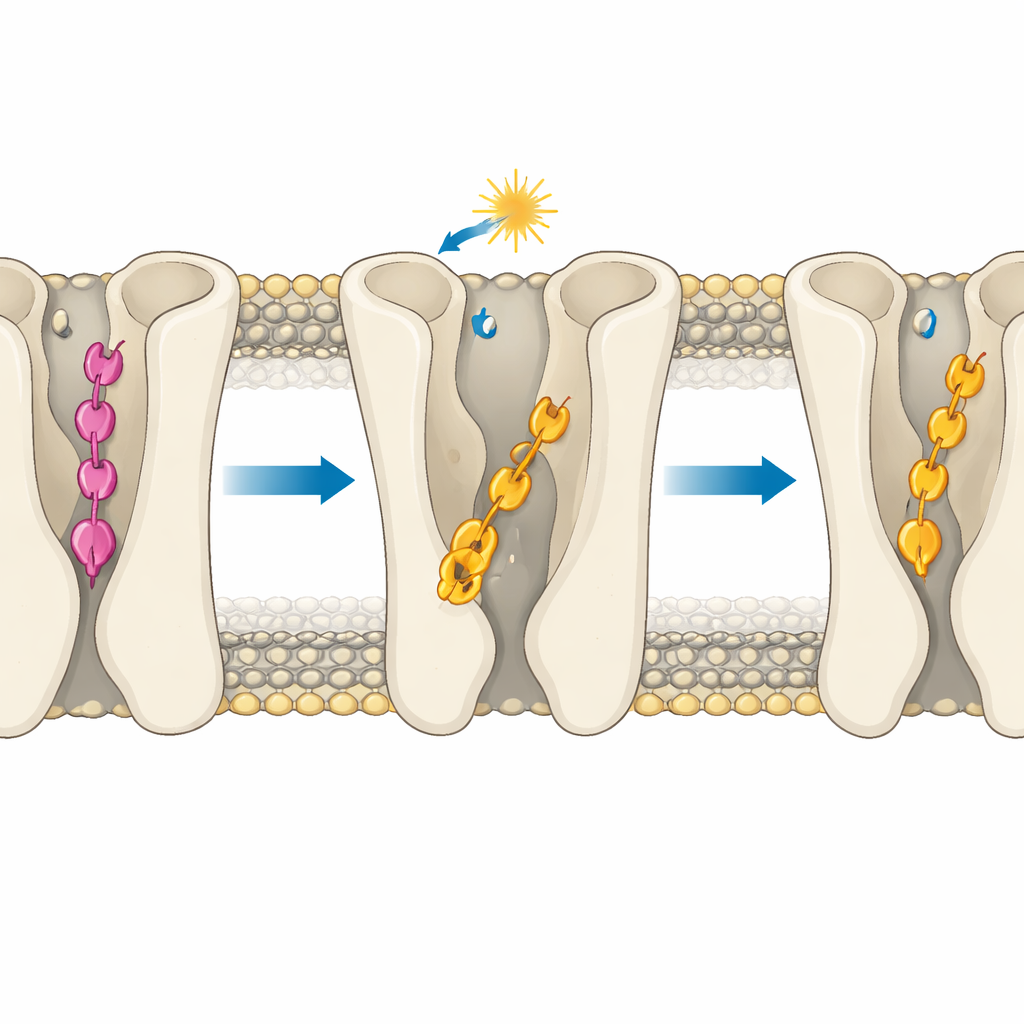
Zasady projektowania przyszłych leków sterowanych światłem
Dla nied specjalisty przesłanie jest takie: dokładna głębokość, na której lek osiada w kieszeni receptora, może decydować o różnicy między wyłączonym, częściowo włączonym a silnie włączonym stanem — nawet gdy zmiana chemiczna wydaje się minimalna na papierze. Pokazując, jak jeden ligand fotoswitchowalny może nadmiernie się wsunąć i zablokować receptor w stanie wyłączonym, podczas gdy blisko spokrewniony ligand utrzymuje się na głębokości sprzyjającej aktywacji, badanie proponuje klarowną zasadę projektową: kontroluj głębokość insercji równie starannie jak zmiany kształtu wywołane światłem. Te wnioski mogą ukierunkować tworzenie nowej generacji związków światłoczułych, które z bezprecedensową precyzją leczą zaburzenia mózgu, sterując szlakami sygnałowymi w sposób kontrolowany i odwracalny, przy jednoczesnym minimalizowaniu skutków ubocznych.
Cytowanie: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Słowa kluczowe: fotofarmakologia, receptor serotoniny 5-HT2A, ligandy fotoswitchowalne, aktywacja GPCR, symulacje dynamiki molekularnej