Clear Sky Science · pl
Zachowanie „rusztowania” i organizacja strukturalna w wieloskładnikowych kondensatach białkowych ujawnione przez badanie kropelek tau/TDP-43
Białka zachowujące się jak maleńkie krople oleju
W wnętrzu naszych komórek wiele białek nie pozostaje równomiernie wymieszanych w wodnistym środowisku. Zamiast tego skupiają się w maleńkich ciekłych kroplach, trochę jak olej w wodzie. W tym badaniu przyjrzano się, jak dwa takie białka — tau i TDP-43 — które są ściśle związane z chorobą Alzheimera i innymi otępieniami, tworzą wspólne kropelki. Odkrywając, jak te krople powstają, mieszają się i organizują, praca dostarcza wskazówek, dlaczego szkodliwe agregaty białkowe pojawiają się w starzejących się mózgach i jak moglibyśmy kiedyś nimi sterować.
Dlaczego te dwa białka mózgowe są ważne
Tau i TDP-43 są znane z tworzenia toksycznych agregatów w chorobach neurodegeneracyjnych. Tradycyjnie naukowcy badali każde z nich osobno, ale sekcje zwłok ludzkich mózgów coraz częściej pokazują, że obydwa białka mogą kończyć w tych samych uszkodzonych obszarach. To rodzi kluczowe pytanie: gdy tau i TDP-43 występują razem w komórkach, jak dzielą przestrzeń wewnątrz kropelek i czy to współistnienie sprzyja chorobowemu agregowaniu? Autorzy wybrali uproszczony, lecz realistyczny model wykorzystujący tau i niskozłożony ogon TDP-43 (LCD), który jest fragmentem najbardziej odpowiedzialnym za tworzenie kropelek i ich ostateczne krystalizowanie się.
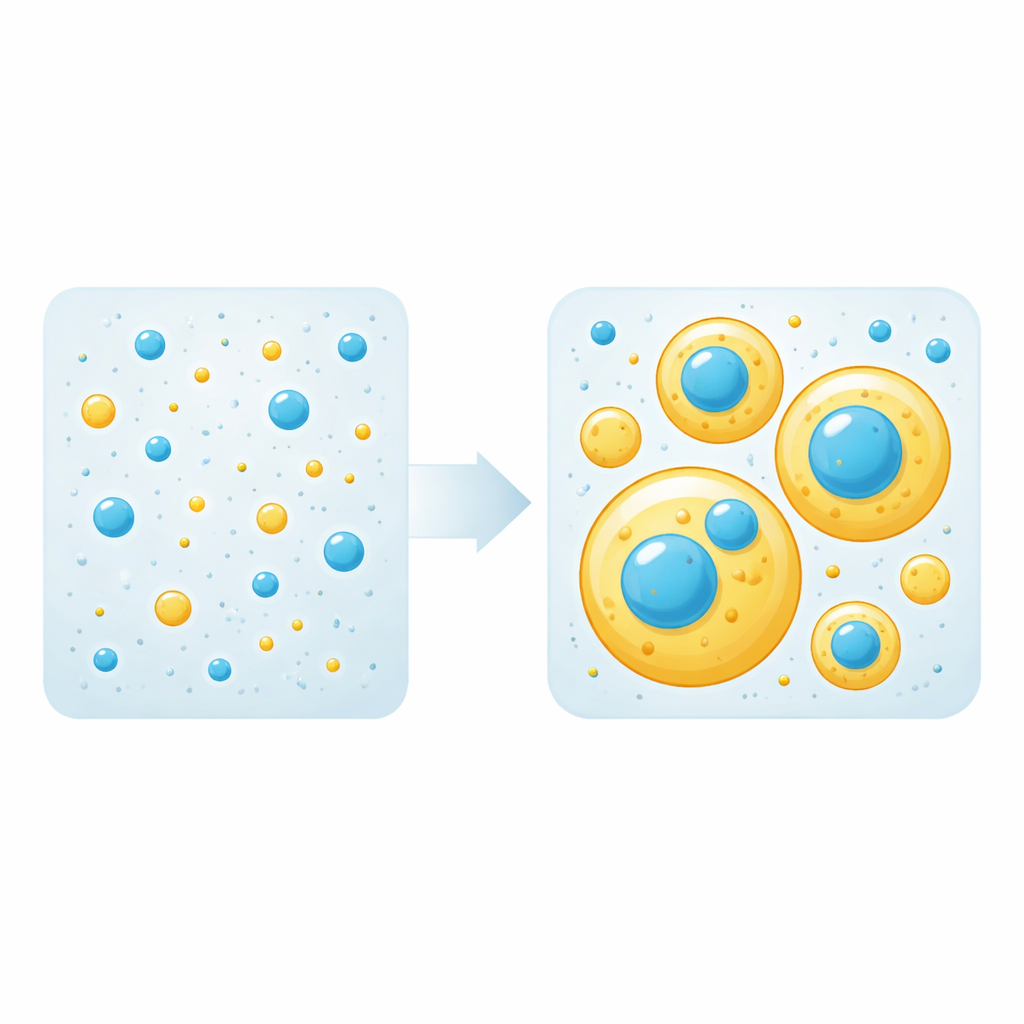
Kropelki, „rusztowania” i „pasażerowie”
Ciekłe kropelki takie jak te powstają, gdy przyciąganie między białkami przewyższa przyciąganie białko-woda, powodując podział roztworu na fazę gęstą (kropelki) i rozcieńczoną. W mieszaninach tylko niektóre białka są potrzebne do zbudowania kropelek; nazywa się je „rusztowaniami”. Inne po prostu wchodzą do kropelek jako „pasażerowie”. Zespół najpierw zmierzył próg stężenia, przy którym każde białko samo zaczyna tworzyć kropelki. Następnie zmieszali różne ilości tau i LCD TDP-43 i obserwowali za pomocą mikroskopii fluorescencyjnej, czy pojawiają się kropelki i jak białka się w nich układają. Co uderzające, stwierdzili, że każde z białek może pełnić rolę rusztowania lub pasażera zależnie wyłącznie od swojego stężenia: powyżej własnego progu buduje kropelki, poniżej tego progu jest biernie rekrutowane do kropelek utworzonych przez drugie białko.
Warstwowe kropelki i tajemnicza halo
Gdy oba białka były wystarczająco liczne, aby tworzyć kropelki samodzielnie, nie mieszały się w jedną jednorodną kroplę. Zamiast tego większe krople bogate w tau otaczały mniejsze krople bogate w TDP-43, tworząc warstwową, wielofazową strukturę. Pomiary zwilżalności kropelek na szkle pokazały, że kropelki TDP-43 mają wyższe napięcie powierzchniowe, więc energetycznie korzystne jest, aby znajdowały się wewnątrz bardziej zwilżających kropelek tau. Na tych granicach pojawił się uderzający element: tau gromadził się w szczególnie wysokich stężeniach jako jasne „halo” pokrywające powierzchnię kropelek TDP-43, nawet gdy samo tau było poniżej własnego progu tworzenia kropelek. Z czasem obszary bogate w TDP-43 miały tendencję do usztywniania się w materiał bardziej przypominający ciało stałe, podczas gdy obszary bogate w tau pozostawały ciekłe, co sugeruje różne skłonności do przekształcania się w długotrwałe agregaty.
Dostrajanie oddziaływań i badanie mechanizmu mikroskopowego
Autorzy następnie przetestowali, jak specyficzne siły molekularne kontrolują, które białko działa jako rusztowanie lub pasażer. Selektywnie osłabili oddziaływania hydrofobowe (odpychające od wody), które napędzają kondensację LCD TDP-43, używając 1,6-heksanodiolu, a oddzielnie osłabili oddziaływania elektrostatyczne (oparte na ładunku), które napędzają kondensację tau, podnosząc poziom soli. W każdym przypadku wyłączenie kluczowych oddziaływań jednego białka uniemożliwiało mu tworzenie kropelek i zmieniało je w pasażera wewnątrz kropelek drugiego, naśladując efekt obniżenia stężenia. Aby zrozumieć halo głębiej, zmieniali zasolenie, by zobaczyć, ile tau wnika do kropelek TDP-43, i użyli symulacji komputerowych traktujących każdy aminokwas jako uproszczoną kulkę. Te symulacje odtworzyły halo i pokazały, że pierwsze ~40 aminokwasów ujemnie naładowanego regionu N‑końca tau kotwiczy się na powierzchni kropli, podczas gdy reszta cząsteczki rozciąga się na zewnątrz do otaczającego płynu, tworząc „amfifilową” (częściowo lubiącą kropelki, częściowo lubiącą wodę) powłokę. Eksperymenty z skróconym fragmentem tau pozbawionym tego odcinka N‑końca potwierdziły, że bez niego halo znika.

Co to znaczy dla chorób mózgu
Wyniki ujawniają ogólny zestaw zasad dotyczących tego, jak wieloskładnikowe kropelki białkowe składają się i organizują. W układzie tau/TDP-43, który odzwierciedla sytuacje w chorych neuronach, stężenie i siła oddziaływań wspólnie decydują, które białka budują kropelki, a które je zajmują. Napięcie powierzchniowe i amfifilowe ułożenia następnie kształtują warstwowe kropelki i halo, które mogą koncentrować wiele białek związanych z chorobą w tej samej ograniczonej przestrzeni, potencjalnie sprzyjając ich utwardzaniu w agregaty. Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że tau i TDP-43 nie zlepiają się przypadkowo; samorzutnie organizują się w uporządkowane ciekłe kropelki, których architektura jest rządzona przez proste zasady fizyczne. Zrozumienie i ostateczne kontrolowanie tych zasad może otworzyć nowe drogi do spowalniania lub zapobiegania szkodliwemu gromadzeniu białek w chorobach neurodegeneracyjnych.
Cytowanie: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Słowa kluczowe: kondensaty białkowe, separacja fazy ciekłociekłej, tau, TDP-43, neurodegeneracja