Clear Sky Science · pl
Badanie stabilności BOx na różnych nieorganicznych nośnikach
Czystsze paliwa z pospolitego pierwiastka
Przekształcenie zwykłego propanu — tego z butli do grilla — w bardziej wartościowe składniki do produkcji tworzyw sztucznych zwykle wymaga gorących, energochłonnych procesów, które także generują dużo dwutlenku węgla. W pracy tej analizuje się, jak związki boru, stosunkowo pospolitego pierwiastka, mogą ułatwić tę przemianę w sposób łagodniejszy i czyściejszy. Odkrywając, jak bor zachowuje się na różnych stałych powierzchniach w wysokich temperaturach, autorzy wskazują nowe sposoby projektowania katalizatorów, które wytwarzają użyteczne związki przy mniejszych odpadach i niższym zużyciu energii.
Dlaczego chemia propan→tworzywa jest istotna
Współczesne życie w dużym stopniu opiera się na lekkich olefinach, takich jak propen i eten, które są kluczowymi składnikami tworzyw sztucznych, włókien i niezliczonych codziennych materiałów. Obecnie większość tych związków wytwarza się z ropy lub gazu ziemnego w energetycznie wymagających procesach, które emitują duże ilości CO₂. Alternatywny proces, zwany utleniającą dehydrogenacją propanu, w zasadzie może produkować te olefiny w niższych temperaturach i z mniejszą ilością niepożądanych produktów. Materiały na bazie boru pojawiły się ostatnio jako obiecujące katalizatory tej reakcji, ponieważ są wysoce selektywne: sprzyjają przekształceniu propanu w olefiny zamiast jego całkowitego spalenia do CO₂. Mimo to badacze wciąż nie rozumieją w pełni, jak wyglądają „aktywne” formy boru ani gdzie dokładnie przebiega reakcja — na powierzchni katalizatora, w fazie gazowej, czy w obu miejscach jednocześnie.
Zaskakująca mobilność boru w gorących reaktorach
Autorzy skupili się na tlenku boru, prostym związku boru i tlenu zapisywanym jako BOx, osadzonym na trzech powszechnych materiałach nieorganicznych: czystej krzemionce, czystym tlenku glinu oraz mieszaninie krzemionki i tlenku glinu. Przy użyciu kombinacji technik śledzących gazy opuszczające powierzchnię podczas jej podgrzewania oraz metod badających lokalną strukturę atomów w ciałach stałych wykazali, że bor nie zawsze pozostaje na miejscu. Na krzemionce tlenek boru ma tendencję do tworzenia luźno związanych klastrów, które mogą parować, tworząc lotne związki zawierające bor w strumieniu gazu. Natomiast na nośnikach bogatych w glin bor silniej wiąże się z tlenami powiązanymi z aluminium, tworząc bardziej stabilną, szklistą sieć, która opiera się wypłukiwaniu do fazy gazowej. Proste testy płukania potwierdziły ten obraz: większość boru można było zmyć z próbek na krzemionce, podczas gdy znacznie mniej z tych opartych na glinie.
Powiązanie stabilności boru z zachowaniem katalitycznym
Różnice w mobilności boru okazały się ściśle korelować z zachowaniem katalizatorów w reakcji propanowej. Tlenek boru na krzemionce zaczynał przekształcać propan w olefiny przy temperaturach około 80 °C niższych niż katalizatory zawierające glin, chociaż wszystkie trzy systemy ostatecznie wykazywały bardzo podobne zależności między stopniem przereagowania propanu a selektywnością do olefin. Podgrzewanie próbek przy jednoczesnym monitorowaniu fragmentów zawierających bor w fazie gazowej wykazało, że krzemionka uwalniała znacznie więcej tlenku boru i powiązanych gatunków w temperaturach reakcji niż glin. Sugeruje to, że nośniki, które łatwiej pozwalają borowi uciec, mogą wywoływać reakcję wcześniej, ponieważ więcej reaktywnych pośredników zawierających bor trafia do fazy gazowej, gdzie mogą zapoczątkować łańcuchowe reakcje przemieniające propan.
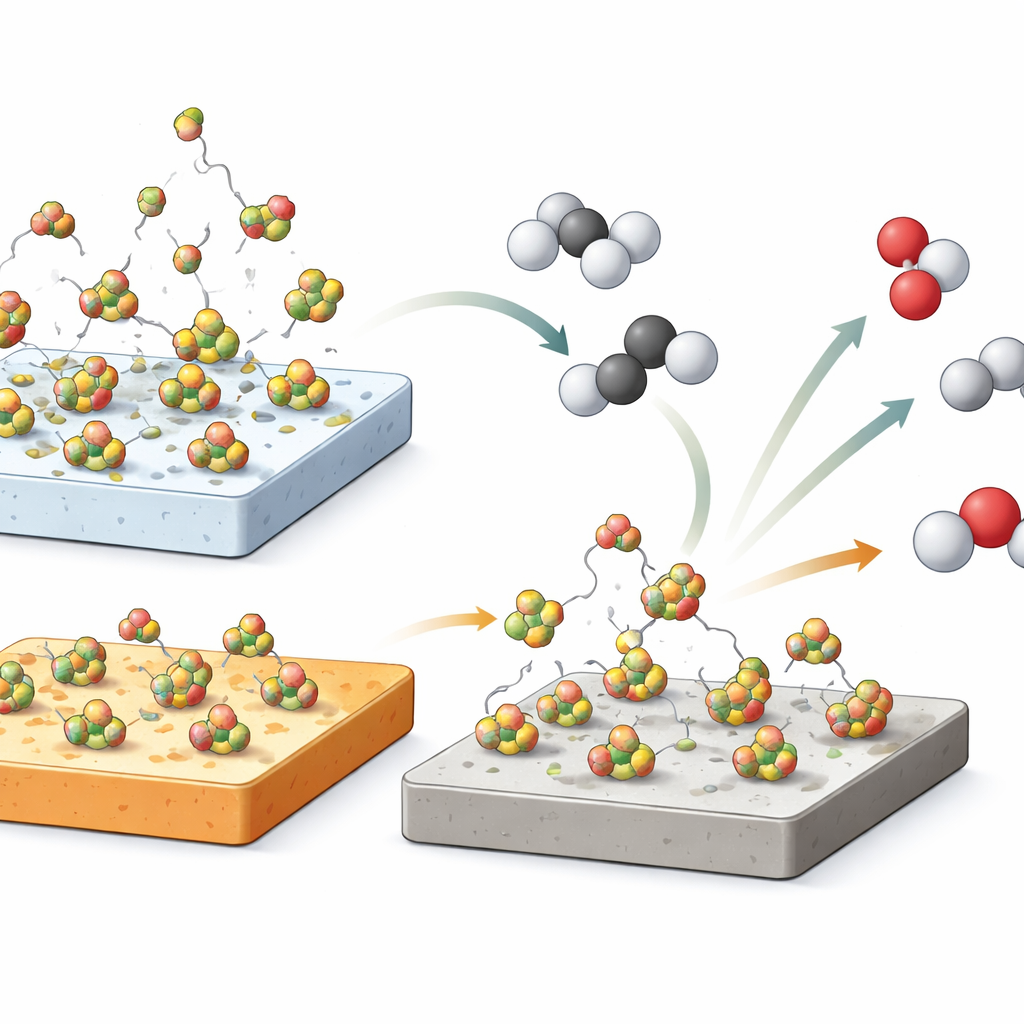
Bor w fazie gazowej jako niewidoczny pomocnik
Aby sprawdzić, czy sam bor w gazie może napędzać chemię, badacze przeprowadzili zaskakujący eksperyment: całkowicie usunęli stały katalizator i wstrzykliwanych do gorącego, pustego reaktora małą dawkę roztworu kwasu borowego, odpowiadającą około jednej siedemdziesiątej boru zwykle obecnego na katalizatorze. Gdy roztwór szybko rozkładał się do tlenku boru w 500 °C, konwersja propanu wzrosła o około 20%, przy selektywności do olefin podobnej do obserwowanej nad stałymi katalizatorami. Test kontrolny z samą wodą dał tylko niewielki, krótkotrwały efekt. W połączeniu z pomiarami desorpcji wynik ten silnie wskazuje, że lotne gatunki boru w fazie gazowej odgrywają istotną rolę, prawdopodobnie inicjując łańcuchy rodnikowe przekształcające propan w propen i eten.
Co to oznacza dla przyszłych katalizatorów
Dla osób nietechnicznych główny wniosek jest taki, że stały nośnik pod katalizatorem na bazie boru nie jest tylko bierną podporą — aktywnie kontroluje, ile boru może wydostać się do gazu i tym samym, jak łatwo rozpoczyna się reakcja. Nośniki takie jak krzemionka, które łatwiej uwalniają bor, prowadzą do aktywacji propanu w niższych temperaturach, podczas gdy nośniki bogate w glin silniej wiążą bor i wymagają wyższych temperatur, choć wszystkie osiągają podobne selektywności produktów, gdy reakcja już przebiega. Ta obserwacja sugeruje, że staranne dostrojenie siły zakotwiczenia boru do nośnika może pozwolić chemikom projektować katalizatory równoważące stabilność i aktywność, umożliwiając czyściejsze, bardziej energooszczędne ścieżki od prostych paliw, takich jak propan, do molekuł stanowiących podstawę współczesnych materiałów.
Cytowanie: Johánek, V., Wróbel, M., Knotková, K. et al. Exploring the stability of BOx at various inorganic supports. Commun Chem 9, 116 (2026). https://doi.org/10.1038/s42004-026-01926-7
Słowa kluczowe: katalizatory tlenku boru, utleniająca dehydrogenacja propanu, chemia rodnikowa w fazie gazowej, nośniki z krzemionki i glinu, produkcja olefin