Clear Sky Science · pl
Synergistyczne efekty kation–powierzchnia przyspieszają kinetykę alkalicznej ewolucji wodoru na schodkowanych powierzchniach Pt
Dlaczego ma to znaczenie dla czystej energii
Produkcja czystego wodoru z wody jest kluczowym elementem wielu planów osiągnięcia zerowej emisji netto, lecz obecne praktyczne urządzenia tracą energię, ponieważ reakcja tworząca pęcherzyki wodoru może być zaskakująco powolna w roztworach zasadowych. To badanie sięga poziomu pojedynczych atomów i cząsteczek wody, aby wyjaśnić, dlaczego niektóre powierzchnie platyny działają lepiej niż inne oraz jak powszechne rozpuszczone jony w cieczy mogą współdziałać z powierzchnią metalu, przyspieszając produkcję wodoru.
Formowanie powierzchni metalu, które kieruje wodą
Naukowcy koncentrują się na platynie, wzorcowym materiale do rozszczepiania wody, i porównują dwa rodzaje atomowych krajobrazów na jej powierzchni. Jedna jest płaska, jak gładki taras (oznaczany Pt(111)); druga jest schodkowana, przypominająca maleńkie schody (Pt(311)). Przy użyciu zaawansowanych symulacji kwantowo‑mechanicznych obejmujących zarówno elektrony, jak i ruchome cząsteczki wody, modelują zachowanie tych powierzchni pod realistycznymi napięciami pracy w alkalicznym elektrolicie. Celem jest zobaczyć, jak lokalne otoczenie tuż przy metalu — gdzie spotykają się woda, jony i elektrony — kontroluje szybkość pierwszego kroku w tworzeniu wodoru.
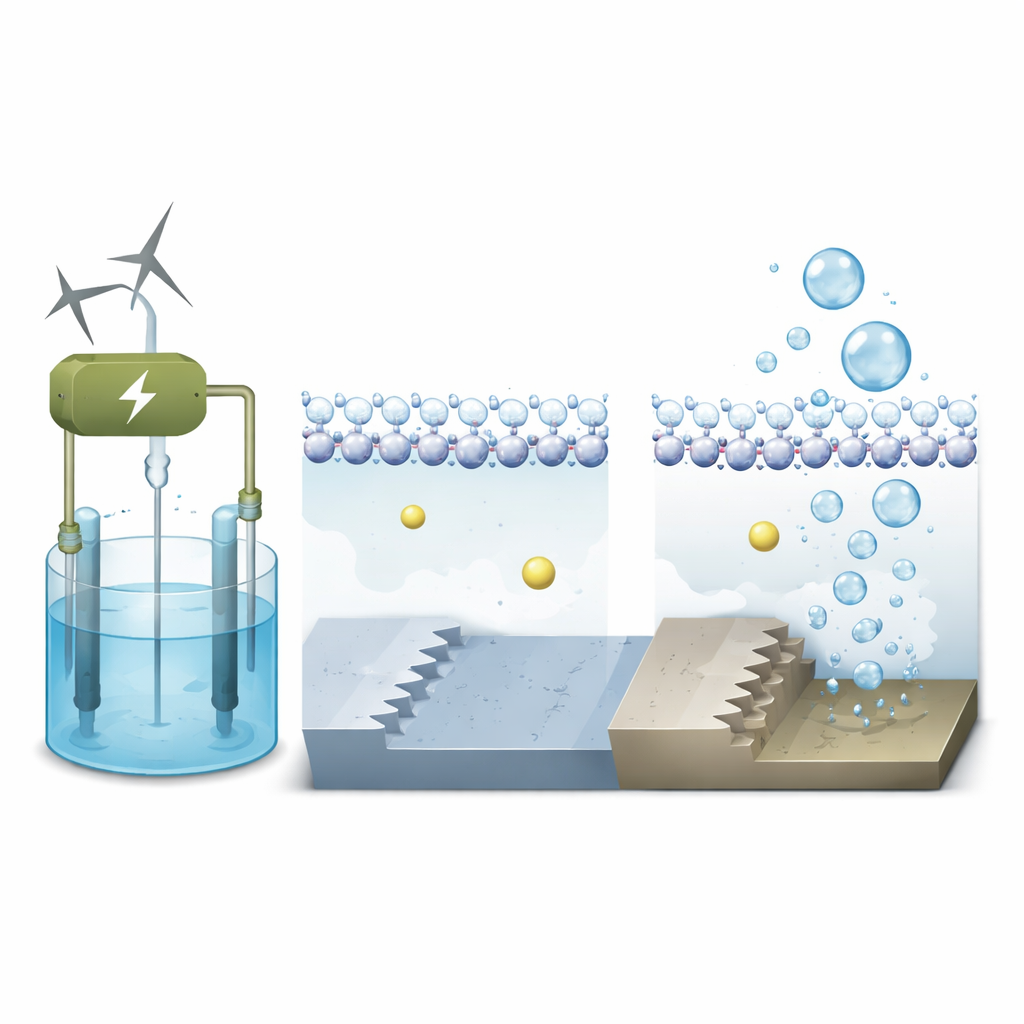
Jony solne jako ukryci pomocnicy
W alkalicznych elektrolizerach ciecz zawiera kationy metali alkalicznych, takie jak sód. Te dodatnio naładowane jony robią więcej niż tylko dryfują; mogą gromadzić się w pobliżu elektrody i subtelnie przekształcać pole elektryczne na styku. Symulacje pokazują, że na płaskim tarasie platyny woda tworzy zwartą, uporządkowaną warstwę z atomami wodoru skierowanymi w dół ku ujemnie naładowanej powierzchni. Jony sodu pozostają dalej, oddzielone od metalu tą warstwą wody, więc ich wpływ na reakcję jest umiarkowany. Na powierzchni schodkowanej natomiast atomy o niższej koordynacji na krawędzi stopnia wiążą wodę silniej i tworzą chropowatszą, bardziej nieuporządkowaną lokalną strukturę wody.
Szczególny klaster przy powierzchni, który przyciąga jony bliżej
W tych krawędziach stopni zespół odkrywa powtarzalny motyw strukturalny: cząsteczkę wody przyłączoną bezpośrednio do platynowego stopnia, która z kolei utrzymuje pobliski jon sodu otoczony dodatkowymi cząsteczkami wody. Ten zwarty klaster platyna–woda–sód efektywnie przyciąga jon około 2,3 angstroma bliżej metalu niż na powierzchni płaskiej. Zwiększona bliskość znacząco wzmacnia lokalne pole elektryczne w tym małym regionie, co silnie polaryzuje sąsiednie cząsteczki wody. Symulacje ujawniają, że jeden wiązanie O–H w tych cząsteczkach wydłuża się bardziej niż zwykle, wskazując, że jest częściowo nastawione do zerwania jeszcze zanim reakcja formalnie się rozpocznie.
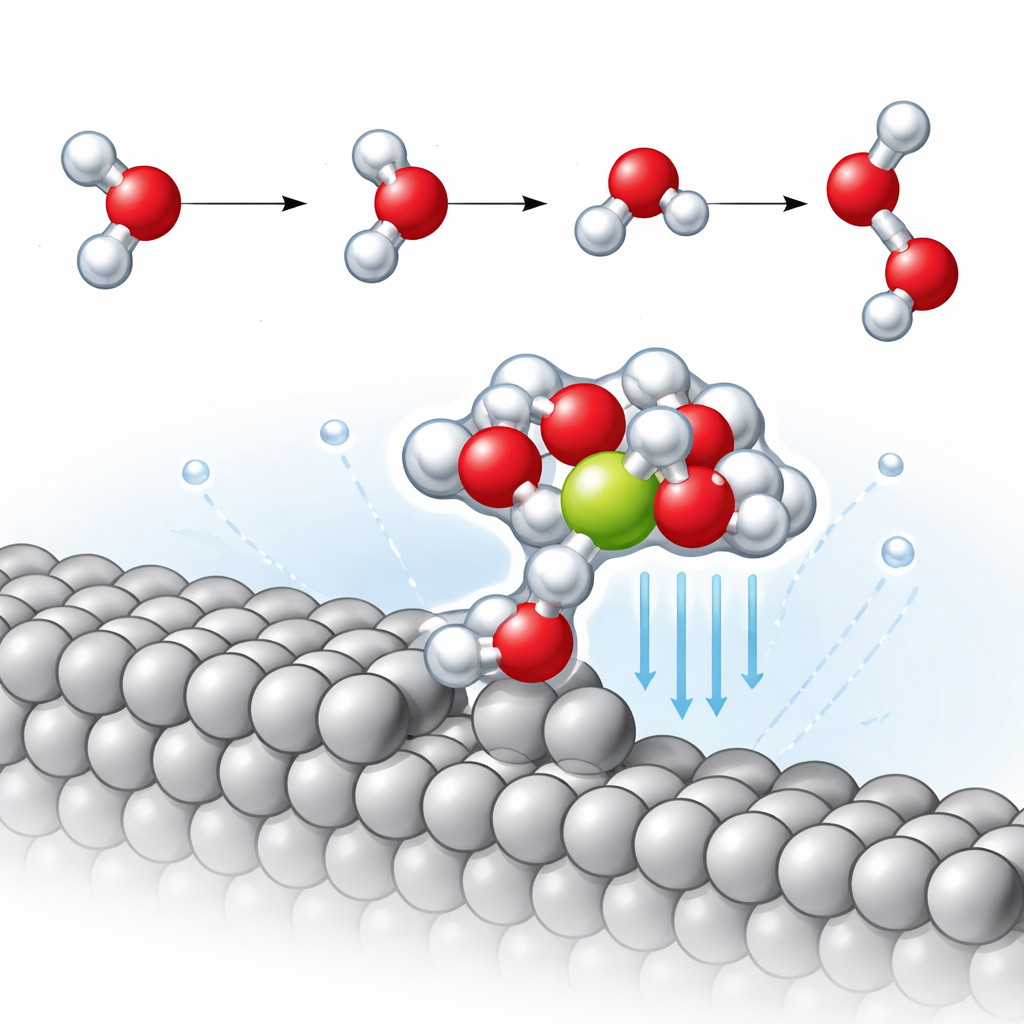
Obniżenie bariery tworzenia wodoru
Kluczowy wolny krok w alkalicznej ewolucji wodoru znany jest jako krok Volmera, w którym cząsteczka wody rozpada się: atom wodoru wiąże się z metalem, a pozostały wodorotlenek trafia do cieczy. Śledząc ścieżkę reakcji o minimalnej energii, autorzy stwierdzają, że na płaskiej powierzchni platyny sód ma jedynie niewielki wpływ na barierę energetyczną tego kroku. W przeciwieństwie do tego, na powierzchni schodkowanej pobliski klaster stabilizowany przez sód obniża energię aktywacji o około 0,14 elektronowolta — mniej więcej trzykrotnie większą poprawę niż obserwowaną na płaskim fasetcie. Szczegółowa analiza ruchów drgań pokazuje, że wiązanie O–H skierowane w stronę powierzchni staje się znacząco słabsze w obecności bliskiego jonu, co ułatwia jego zerwanie i tym samym przyspiesza tworzenie wodoru.
Zasada projektowania lepszych katalizatorów wodoru
W sumie badanie konkluduje, że najlepsza wydajność w alkalicznej produkcji wodoru nie wynika wyłącznie z powierzchni metalu ani samego elektrolitu, lecz z ich synergii. Schodkowane miejsca na platynie, które mogą zakotwiczyć specjalne klastry woda–jon, przyciągają kationy alkaliczne blisko, wzmacniają lokalne pole elektryczne, częściowo przygotowują wiązania wody do zerwania i silnie przyspieszają kluczowy pierwszy krok ewolucji wodoru. Dla laika wniosek jest taki, że poprzez staranne rzeźbienie mikroskopowego kształtu powierzchni katalizatora oraz dobór elektrolitów, które doprowadzą właściwe jony we właściwe miejsca, inżynierowie mogą pokonać niektóre fundamentalne spowolnienia urządzeń alkalicznych i zaprojektować bardziej wydajne, oszczędzające energię systemy do produkcji czystego wodoru.
Cytowanie: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Słowa kluczowe: ewolucja wodoru, alkaliczna elektroliza, katalizator platynowy, woda przyinterfejsowa, kationy metali alkalicznych