Clear Sky Science · pl
Strukturalne podstawy tworzenia filamentów ludzkiego RegⅢα
Jak nasze jelita zwalczają zarazki
Nasze jelita są stale wystawione na działanie miliardów bakterii, z których wiele jest nieszkodliwych, a nawet pożytecznych. Gdy jednak pojawiają się groźne mikroby, organizm potrzebuje szybkich i precyzyjnych mechanizmów ataku, które nie uszkadzają własnych tkanek. W tym badaniu przyjrzano się z bliska jednemu z takich naturalnych białek obronnych, zwanemu RegIIIα, i ukazano, jak zmienia ono kształt, by zabijać bakterie, a następnie przechodzi w bezpieczniejszą, mniej szkodliwą formę. Zrozumienie tej metamorfozy może pomóc naukowcom lepiej pojąć, jak utrzymujemy równowagę mikrobioty jelitowej oraz co idzie nie tak w chorobie.
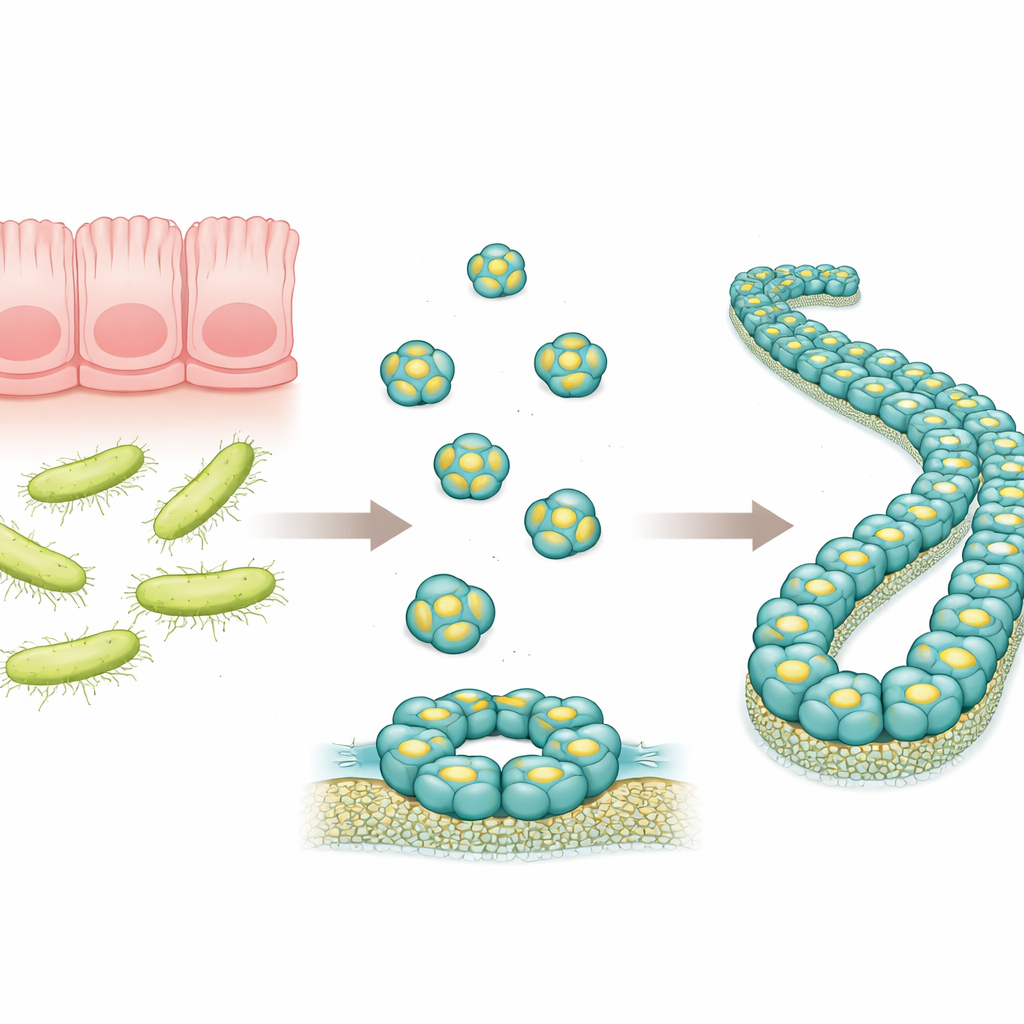
Mały obrońca w jelicie
RegIIIα to białko wytwarzane w przewodzie pokarmowym, które celuje w określone bakterie, zwłaszcza te o grubych ścianach zewnętrznych, znane jako bakterie Gram-dodatnie. Wcześniejsze badania sugerowały, że RegIIIα może przebijać błony bakterii, tworząc struktury podobne do pierścieni, co pozwala na wyciek zawartości mikroba i prowadzi do jego śmierci. Badacze zauważyli też, że z czasem te pierścieniowe struktury mogą się układać w długie filamenty, co wydaje się zmniejszać zdolność białka do zabijania. Dokładne uporządkowanie cząsteczek RegIIIα w tych większych zespołach nie było jednak znane szczegółowo, co utrudniało zrozumienie mechanizmu działania białka i kontroli jego aktywności.
Widok filamentu w skali atomowej
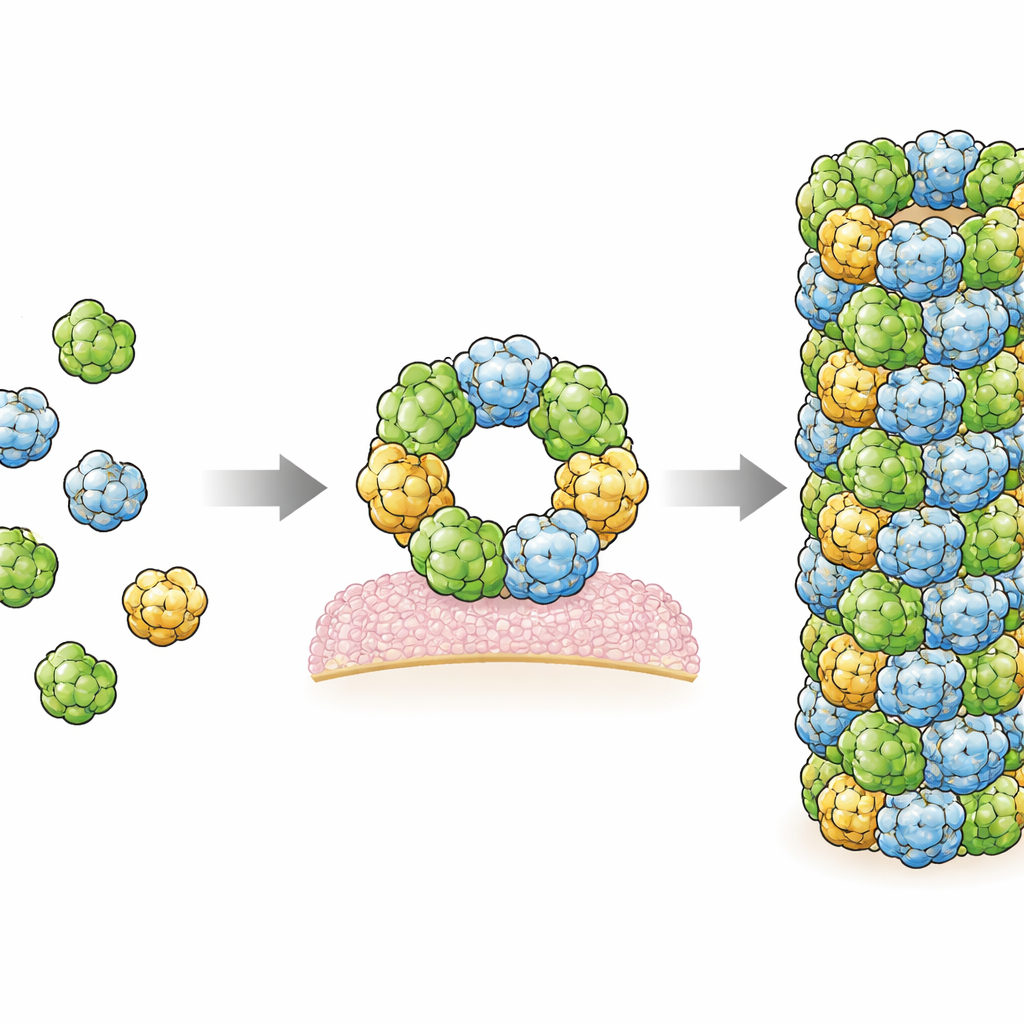
W tym badaniu autorzy wytworzyli ludzki RegIIIα w bakteriach, a następnie sprowokowali jego samorzutne składanie się w filamenty w kontrolowanych warunkach. Użyli potężnej metody obrazowania zwanej kriomikroskopią elektronową, która pozwala zobaczyć molekuły biologiczne zamrożone w cienkiej warstwie lodu z niemal atomową rozdzielczością. Odkryli, że filamenty zbudowane są z powtarzających się zestawów trzech identycznych jednostek RegIIIα, zwanych trimerami, które układają się w regularny, spiralny wzór. Każda pojedyncza cząsteczka RegIIIα wygląda bardzo podobnie do wcześniej opisanych struktur krystalicznych, ale jej orientacja w filamentach różni się od wcześniejszego, niżej rozdzielczego modelu. Ta skorygowana orientacja zmienia sposób, w jaki naukowcy rozumieją interakcję białka z błonami bakteryjnymi i z jego własnym segmentem regulacyjnym.
Jak białka łączą się i dlaczego lipidy mają znaczenie
Analiza struktury pozwoliła badaczom zidentyfikować dwa główne regiony kontaktowe, czyli interfejsy, gdzie sąsiadujące cząsteczki RegIIIα stykają się i utrzymują filament. Następnie zmienili konkretne aminokwasy w tych miejscach i pokazali, że te modyfikacje zapobiegają tworzeniu filamentów, potwierdzając, że te punkty kontaktowe są niezbędne. Co ciekawe, w obu interfejsach mapy kri-EM ujawniły dodatkowe nieostre obszary, które prawdopodobnie reprezentują małe, wydłużone cząsteczki wciśnięte między powierzchnie białek. Ich kształt i środowisko chemiczne sugerują, że mogą to być lipidy — te same rodzaje oleistych cząsteczek, które tworzą błony komórkowe. To wspiera wcześniejsze wskazówki, że lipidy pomagają w montażu RegIIIα, być może działając jak molekularne spoiwo stabilizujące połączenia między podjednostkami.
Włącznik i wyłącznik: pH i ukryty segment
Zespół badał też, co kontroluje zdolność RegIIIα do składania się. Zanim białko stanie się aktywne, niesie krótki „pro-segment”, który musi zostać odcięty przez enzymy trawienne. W ich strukturze filamentu o wysokiej rozdzielczości nie ma miejsca w centrum zespołu na zmieszczenie tego dodatkowego fragmentu, co sugeruje, że pro-segment blokuje zdolność RegIIIα do tworzenia pierścieni i filamentów od początku. Stwierdzili również, że skłonność do formowania filamentów zależy od kwasowości: filamenty powstają łatwo przy pH zbliżonym do pH jelita cienkiego, a słabo przy niższym, bardziej kwaśnym pH. Pojedynczy aminokwas, histydyna 50, wydaje się działać jak przełącznik wrażliwy na pH; gdy zostanie zastąpiona innym resztą, tworzenie filamentów staje się znacznie mniej wrażliwe na pH. Te cechy — cięcie przez enzymy, wiązanie lipidów i zależność od pH — tworzą razem wielowarstwowy system kontroli określający, kiedy i gdzie RegIIIα jest aktywny.
Co to znaczy dla zdrowia jelit
Ogólnie to badanie dostarcza najdokładniejszego jak dotąd obrazu, jak cząsteczki RegIIIα składają się w większe struktury powiązane zarówno z ich działaniem przeciwbakteryjnym, jak i z zachowaniem ograniczającym własną aktywność. Te same interfejsy, które budują filamenty, tworzą także heksamerowe pierścienie uważane za formujące pory w błonach bakteryjnych, co sugeruje delikatną równowagę między silną formą zabijającą a bezpieczniejszym, przytłumionym stanem. Mapowanie mutacji związanych z chorobami na tej strukturze pokazuje, że wiele z nich leży w kluczowych punktach kontaktowych, co sugeruje, że zaburzenia w składaniu się mogą leżeć u podstaw niektórych zaburzeń jelitowych lub trzustkowych. Wyjaśniając, jak ten naturalny antybiotyk jest aktywowany, kierowany przez lipidy i kształtowany przez lokalne pH, badanie tworzy podstawy pod przyszłe wysiłki mające na celu modulowanie naszej wrodzonej obrony — albo poprzez jej wzmocnienie przeciw infekcjom, albo jej uspokojenie, gdy ulega dysregulacji.
Cytowanie: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Słowa kluczowe: RegIIIα, odporność jelitowa, kriomikroskopia elektronowa, filamenty białkowe, peptydy przeciwbakteryjne