Clear Sky Science · pl
Azobenzenowy mostek w jonizowalnych amfifilowych glikozydach Janusa do światłowrażliwego, jednoskładnikowego i modulowalnego przez narządy dostarczania pDNA
Światło dla inteligentniejszego dostarczania genów
Terapię genową obiecują leczenie chorób u ich źródła przez dostarczanie fragmentów kodu genetycznego bezpośrednio do naszych komórek. Jednak bezpieczne przeprowadzenie tej kruchej ładunku przez krew, do właściwych narządów i do wnętrza komórek docelowych nadal stanowi poważne wyzwanie. W tej pracy wprowadzono nową klasę drobnych, cukrowych cząstek, których zachowanie można przełączać światłem jeszcze przed wprowadzeniem do organizmu, co pozwala badaczom zmieniać miejsce, w którym gen terapeutyczny się lokuje, oraz siłę jego ekspresji, przy minimalnym uszkodzeniu komórek. 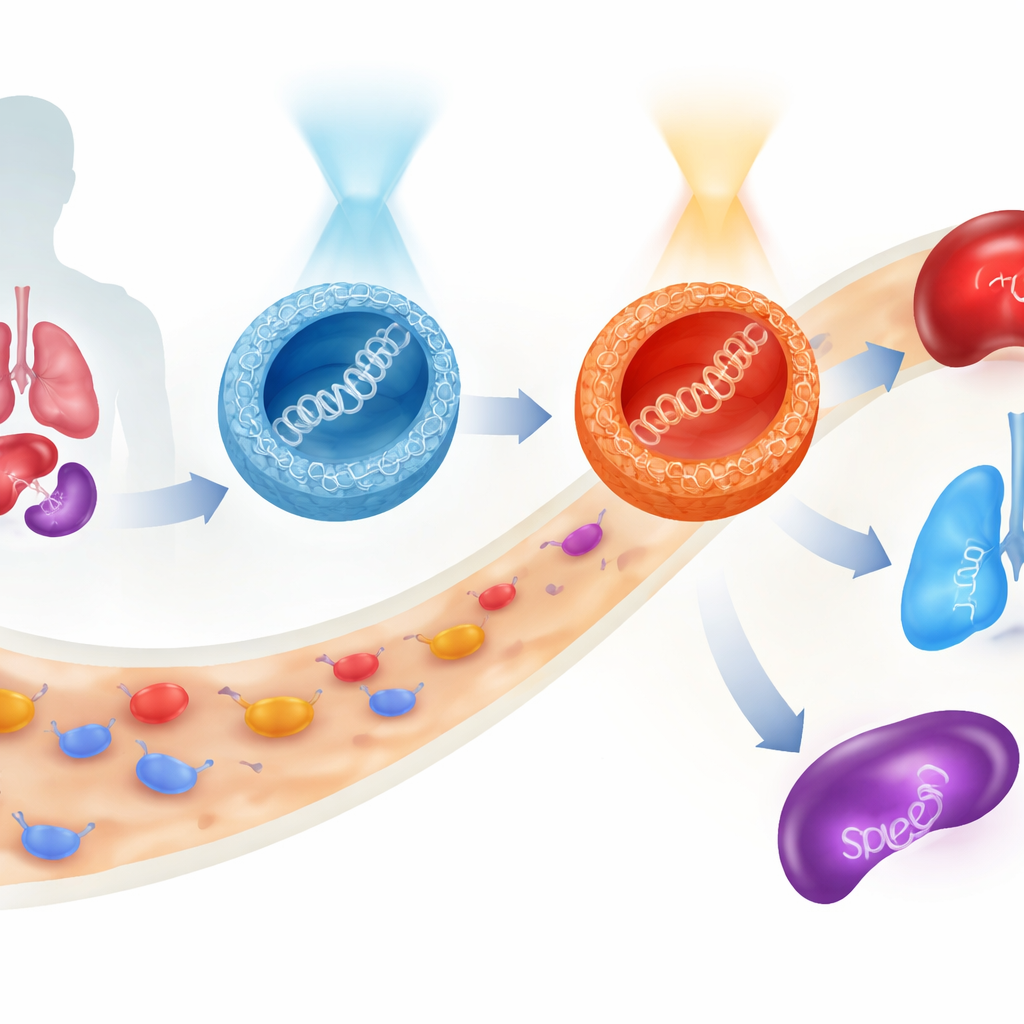
Potrzeba precyzyjnych genetycznych kurierów
Najskuteczniejsze dziś nośniki genów to nanopłatki lipidowe, które przyczyniły się do powstania szczepionek mRNA przeciw COVID‑19. Te wieloskładnikowe krople otaczają i chronią kwasy nukleinowe, lecz zwykle kumulują się głównie w wątrobie i uwalniają tylko niewielką część ładunku wewnątrz komórek. Modyfikowanie ich składu może zmieniać preferencje narządowe, jednak mieszaniny te są złożone i trudne do precyzyjnej kontroli. Zespół stojący za tym badaniem postanowił zaprojektować zamiast tego pojedyncze, dobrze zdefiniowane cząsteczki, które samoistnie tworzą nanocząstki o przewidywalnych kształtach i właściwościach — i które można aktywnie regulować z zewnątrz prostym bodźcem świetlnym.
Cząsteczkowa huśtawka kontrolowana światłem
Rdzeniem nowego systemu są podwójne glikozydy „Janusa”: cząsteczki zbudowane z dwóch jednostek glukozy, wyposażone w hydrofilowe naładowane główki i lipofilowe ogony, połączone przez centralny azobenzenowy „zawias”. Azobenzen może przełączać się między dwoma lustrzanymi kształtami, zwanymi E i Z, pod wpływem różnych barw światła. W wodzie z obecnym DNA wiele kopii tych cząsteczek samoistnie grupuje się w miękkie, warstwowe cząstki otaczające nici plazmidowego DNA. Badacze przygotowali dwie wersje — z mostkami tlenowymi i siarkowymi między cukrem a zawiasem — aby subtelnie dostroić stabilność i zachowanie biologiczne. Poprzez wstępne naświetlanie roztworów mogli wzbogacić formę E lub Z i badać, jak każdy stan wpływa na powstające cząstki dostarczające geny.
Jak zachowują się kształtozmienne cząstki
Pomiary rozmiaru cząstek, ładunku powierzchniowego i struktury wewnętrznej wykazały, że indukowane światłem przełączanie między stanami E i Z ma wyraźne konsekwencje fizyczne. Zazwyczaj forma Z dawała mniejsze, bardziej jednorodne nanocząstki o bardziej uporządkowanym, warstwowym wnętrzu niż forma E. Mikroskopia ujawniła, że te wewnętrzne ułożenia przypominają na przemian ułożone warstwy materiału lipidopodobnego i DNA. Co istotne, obydwa stany chroniły DNA przed degradacją enzymatyczną. W hodowlach komórek pochodzących z nerek, wątroby i tkanki immunologicznej różne izomery dawały wyraźnie odmienne poziomy ekspresji genu, choć podłoże DNA było identyczne. Powtarzane impulsy świetlne zastosowane po wejściu cząstek do komórek zwiększały ekspresję genu wielokrotnie, co sugeruje, że mechaniczne „kopnięcie” związane z przełączeniem pomaga cząstkom rozluźnić się i uwolnić ładunek, a także może ułatwiać ucieczkę z wewnątrzkomórkowych przedziałów. 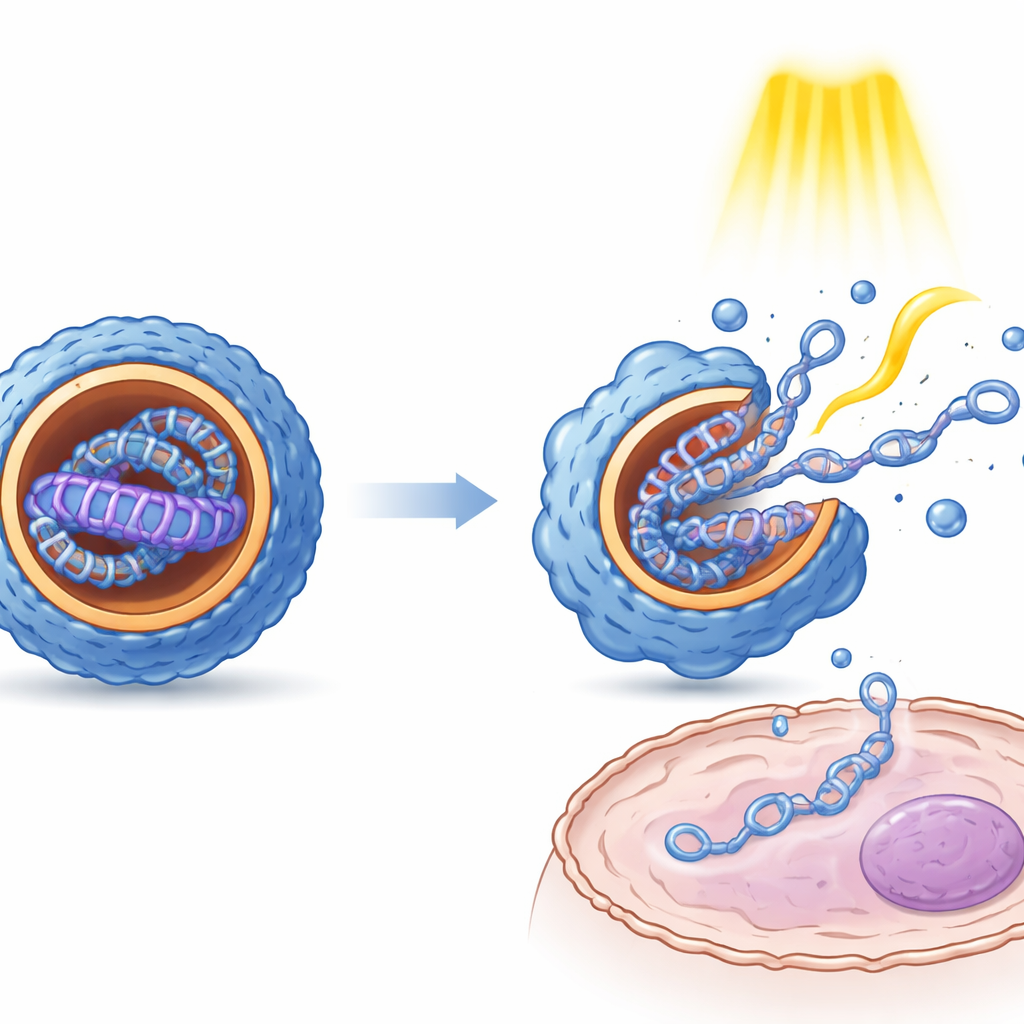
Ukierunkowywanie genów do konkretnych narządów
Najbardziej zaskakujące zachowanie zaobserwowano u myszy. Gdy cząstki z mostkiem tlenowym podano w formie bogatej w E, ekspresja genu‑markera występowała głównie w wątrobie, z pewnym udziałem w płucach. Wstępne przełączenie ich do formy Z przed wstrzyknięciem nie tylko zwiększyło całkowitą ekspresję, ale także przesunęło równowagę w kierunku płuc. Cząstki z mostkiem siarkowym zachowywały się inaczej: ich forma Z faworyzowała śledzionę, kluczowy narząd układu odpornościowego. Tak więc przy tej samej podstawowej ramie molekularnej — i bez zmiany ładunku DNA — badacze mogli skierować aktywność genu głównie do wątroby, płuc lub śledziony, po prostu wybierając typ wiązania (tlenowe lub siarkowe) oraz świetlnie aktywowany kształt (E lub Z) nośnika. W trakcie testów żywotność komórek pozostawała wysoka, co sugeruje, że system jest stosunkowo łagodny.
Świetlnie regulowana droga do przyszłych leków genowych
Mówiąc prosto, zespół zbudował maleńki, światłowłączalny prom dla DNA. Przed iniekcją krótkie naświetlenie „programuje” promy w jeden z dwóch kształtów. Każdy kształt samoistnie assembleuje się w nanocząstki o charakterystycznym rozmiarze i właściwościach powierzchniowych, co z kolei determinuje, jak silnie przylegają do różnych typów komórek i gdzie trafiają w organizmie. Ponieważ ta sama chemiczna baza może być modyfikowana na wiele drobnych sposobów, a przełączanie jest odwracalne i nie zmienia samego DNA, platforma oferuje elastyczny sposób precyzyjnego dostrajania miejsca i sposobu działania terapii genowych. Choć przed użyciem klinicznym pozostaje jeszcze dużo pracy, badanie pokazuje, że starannie zaprojektowane, jednocząsteczkowe nośniki kontrolowane światłem mogą stać się potężnym narzędziem bezpieczniejszych i bardziej precyzyjnych leków genowych.
Cytowanie: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Słowa kluczowe: dostarczanie genów, światłoczułe nanocząstki, przełączniki azobenzenowe, ukierunkowana terapia DNA, nanomedycyna