Clear Sky Science · pl
Proteaza S9 WprP2 katalizuje jednorodne cięcie peptydu prekursorowego w biosyntezie RiPP
Dlaczego małe narzędzia tnące w komórkach są ważne
W bakteriach wyspecjalizowane molekularne nożyczki przecinają długie łańcuchy aminokwasów na mniejsze, aktywne fragmenty, które często stają się antybiotykami lub innymi pożytecznymi związkami naturalnymi. W badaniu odkryto wcześniej nieznane narzędzie tnące — proteazę nazwaną WprP2 — która przycina swój peptydowy substrat z niezwykłą precyzją. Zrozumienie mechanizmu działania tej enzymu może pomóc naukowcom w projektowaniu nowych peptydów bioaktywnych i antybiotyków następnej generacji.
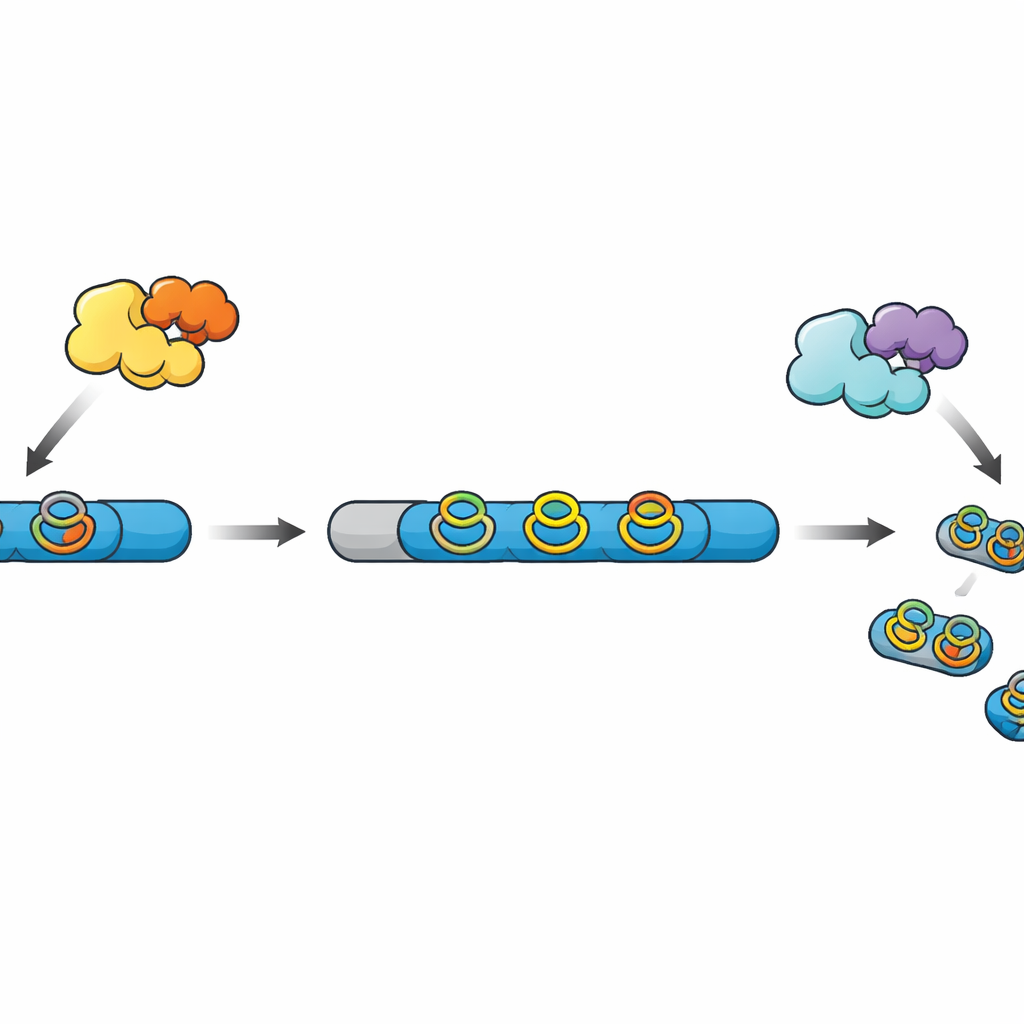
Od surowych łańcuchów do gotowych mini‑leków
Wiele współczesnych naturalnych produktów opartych na peptydach, znanych łącznie jako RiPP, zaczyna się jako proste łańcuchy syntetyzowane na rybosomie. Łańcuchy te zawierają region leadera pełniący funkcję uchwytu oraz region rdzeniowy, który po serii modyfikacji stanie się produktem końcowym. Inne enzymy wprowadzają wiązania krzyżowe i pierścienie, które zwiększają stabilność i aktywność peptydu, a ostatecznie proteaza odcina leader i uwalnia dojrzałą cząsteczkę. W niedawno odkrytej rodzinie RiPP enzymy typu radical SAM tworzą zwarte pierścienie „cyklofanowe” z udziałem aminokwasów aromatycznych, lecz w większości znanych klastrów genowych brak jest dopasowanej proteazy, co czyni końcowe etapy przetwarzania tajemniczymi.
Poszukiwanie brakującego enzymu‑partnera
Autorzy wcześniej badali enzym radical SAM nazwany WprB1, który wprowadzał identyczne wiązania krzyżowe w trzech powtarzających się segmentach WPR w peptydzie prekursorowym. W nowej pracy przeszukali genomy bakteryjne w poszukiwaniu krewnych tego enzymu i sprawdzali okoliczne geny, czy nie kodują proteazy. W Streptomyces venezuelae znaleźli obiecujący klaster zawierający podobny enzym wytwarzający wiązania krzyżowe, jego białkowego pomocnika, odpowiadający peptyd prekursorowy z trzema powtórzeniami WPR oraz kandydującą proteazę serynową z rodziny S9, którą nazwali WprP2. To uczyniło system idealnym modelem do ustalenia, w jaki sposób peptyd jest ostatecznie cięty, aby uwolnić aktywne fragmenty.
Obserwacja cięcia peptydu
Aby zbadać WprP2, zespół wyprodukował peptyd prekursorowy w bakteriach, zarówno z enzymem wprowadzającym wiązania krzyżowe, jak i bez niego, oczyścił go, a następnie wymieszał z proteazą w kontrolowanych reakcjach in vitro. Spektrometria mas wykazała, że WprP2 najpierw przecina łańcuch tuż za każdym segmentem WPR, a następnie wykonuje drugie cięcie w stałej odległości przed określonym resztą proliny dalej w sekwencji. Te dwa etapy tworzą serię mniejszych, jednakowych fragmentów. Co istotne, WprP2 przeprowadzał ten wzorzec cięć niezależnie od tego, czy enzym tworzący wiązania krzyżowe wcześniej utworzył pierścienie cyklofanowe, co pokazuje, że pierścienie nie są konieczne do rozpoznania. W porównaniu z komercyjnym trypsyną, która nie potrafi przeciąć niektórych zeskiebanych miejsc, WprP2 nadal funkcjonował, podkreślając jego niezwykłą odporność.
Odkodowywanie, co enzym rozpoznaje
Następnie badacze zapytali, jakie cechy peptydu WprP2 faktycznie odczytuje. Poprzez systematyczną zmianę pojedynczych aminokwasów wokół miejsc cięcia odkryli, że modyfikacja wielu pobliskich reszt miała niewielki wpływ, ale zmiana kluczowej argininy w segmencie WPR lub glutaminy czy proliny w drugim miejscu cięcia mogła zablokować dany etap. Eksperymenty z pokrewnym peptydem prekursora niosącym różne reszty flankingowe pokazały, że proteaza nadal ciąła po powtórzeniach WPR, lecz wykonywała drugie cięcie tylko wtedy, gdy obecna była para glutamina‑prolina. Generowane komputerowo modele strukturalne przy użyciu AlphaFold3 wspierały ten obraz: w przewidywanych kompleksach miejsca oparte na WPR i para glutamina‑prolina ustawiały się kolejno w centrum katalitycznym enzymu, co jest zgodne z dwustopniowym sekwencyjnym mechanizmem.
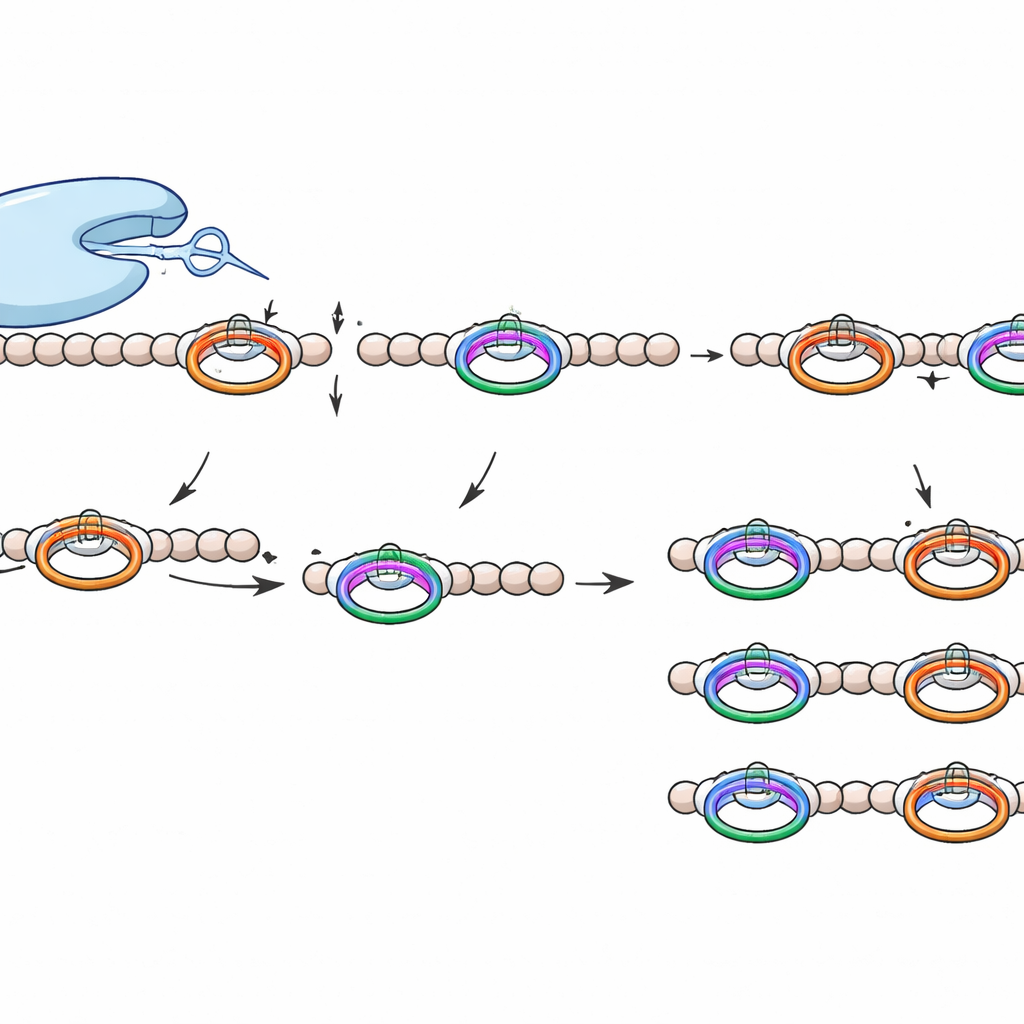
Co wyróżnia to narzędzie tnące
WprP2 należy do szerszej rodziny proteaz S9, która obejmuje już enzymy o znaczeniu medycznym, ale wyróżnia się kilkoma cechami. Przecina po stronie N‑końcowej reszty proliny, a nie po jej stronie C‑końcowej, działa na powtarzającym się motywie, generując równomiernie duże fragmenty w całym łańcuchu prekursora, i wykazuje szeroką tolerancję względem aminokwasów leżących między dwoma miejscami rozpoznawania. To połączenie precyzji i elastyczności nie było wcześniej obserwowane w proteazach związanych z RiPP.
Jak można wykorzystać to odkrycie
Odkrywając proteazę, która rozpoznaje proste wskazówki sekwencyjne i wykonuje jednorodne, powtarzalne cięcia, praca ta dodaje potężne nowe narzędzie do rosnącego zestawu metod inżynierii peptydów. W praktyce WprP2 można wykorzystać do uwalniania lub przekształcania zaprojektowanych peptydów, w tym tych z złożonymi wiązaniami krzyżowymi, które opierają się standardowym enzymom takim jak trypsyna. Dla niespecjalistów kluczowy wniosek jest następujący: naukowcy odkryli nowy rodzaj molekularnych nożyczek, które tną długie łańcuchy peptydowe na precyzyjne, równomierne kawałki, otwierając drzwi do bardziej kontrolowanej produkcji potencjalnych antybiotyków i innych molekuł bioaktywnych.
Cytowanie: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Słowa kluczowe: peptydy RiPP, proteaza serynowa, WprP2, naturalne produkty cyklofanowe, inżynieria peptydów