Clear Sky Science · pl
Probka emisji indukowanej ograniczeniami sterycznymi do monitorowania konformacji białek w żywych komórkach
Obserwowanie białek zmieniających kształt w czasie rzeczywistym
W każdej żywej komórce białka nieustannie zmieniają kształt, przekazując sygnały, wyczuwając otoczenie i wykonując kluczowe zadania. Wiele chorób wynika z zaburzeń tych zmian konformacyjnych, jednak bezpośrednie śledzenie takich ruchów w żywych komórkach — zwłaszcza zarówno w bardzo krótkich, jak i długich skalach czasowych — okazało się niezwykle trudne. W artykule przedstawiono nową sondę emitującą światło, nazwaną BIOSCE, która przekształca drobne ruchy białek w widoczne sygnały, pozwalając badaczom śledzić pojedyncze cząsteczki białek, gdy się zginają, skręcają i wchodzą w interakcje w czasie rzeczywistym wewnątrz żywych komórek. 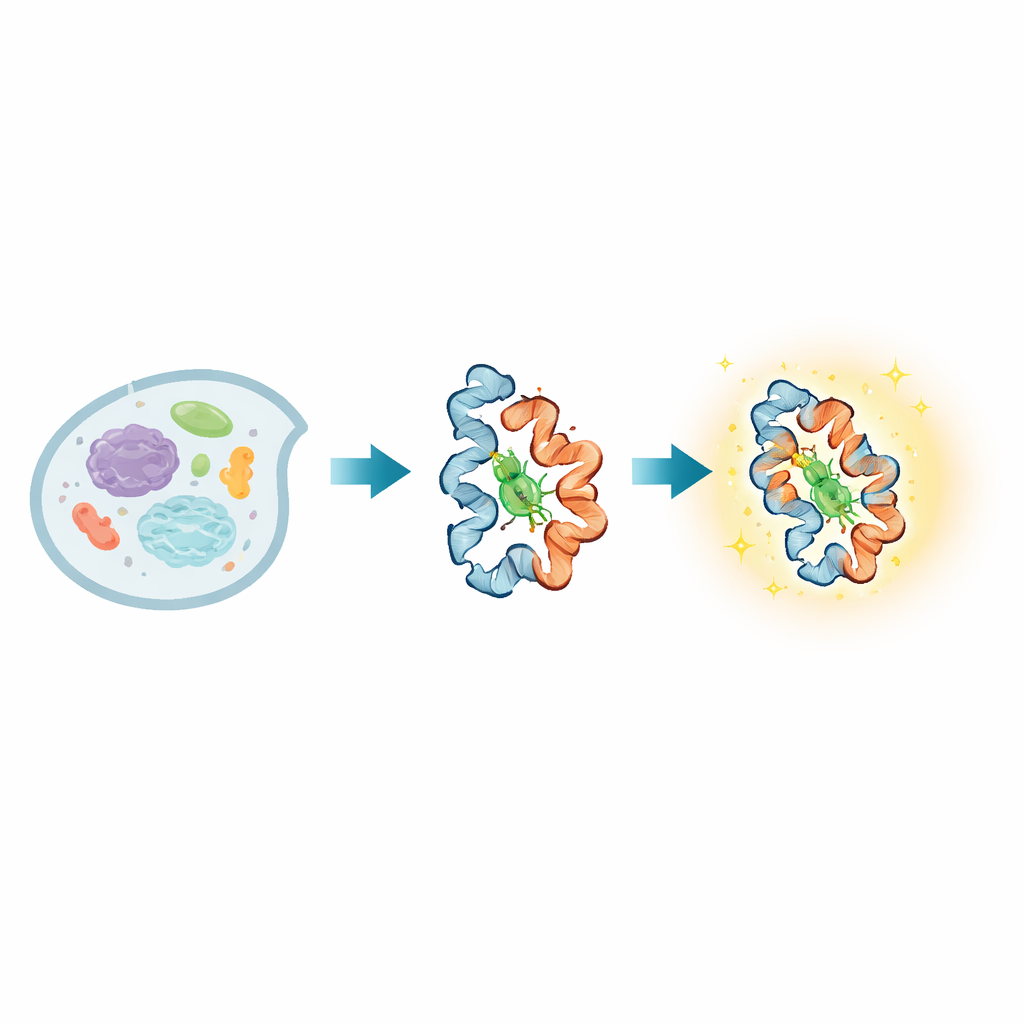
Nowy przełącznik świetlny dla poruszających się białek
U podstaw BIOSCE leży mała cząsteczka barwnika, MTPABP-Cl, która staje się jaśniejsza, gdy jest ściśnięta. Badacze przyłączają ten barwnik do powszechnie używanego taga białkowego, HaloTag, który można genetycznie zespolić praktycznie z dowolnym białkiem zainteresowania. Gdy znakowane białko zmienia kształt lub ciasniej pakuje się z sąsiadami, zmienia się „przestrzeń”, w której barwnik może się poruszać. W luźnym otoczeniu wewnętrzne części barwnika mogą obracać się swobodnie i większość pochłoniętego światła jest rozpraszana na ruch; w bardziej ciasnej kieszeni te ruchy są zablokowane, a energia zamiast tego zostaje uwolniona jako światło. Ta „emisja indukowana ograniczeniem sterycznym” przekształca subtelne zmiany lokalnego zagęszczenia wokół pojedynczego białka w płynną zmianę jasności, zamiast prostego sygnału włącz/wyłącz, dzięki czemu sonda jest wysoce czuła na niewielkie zmiany konformacyjne.
Tworzenie i testowanie barwnika wrażliwego na ściskanie
Zespół najpierw zaprojektował i zsyntetyzował MTPABP-Cl tak, by był przygaszony w roztworze, a rozjaśniał, gdy jest trzymany na miejscu przez HaloTag lub przez bardziej kompaktowe białkowe fuzy. Dokładne pomiary wykazały, że barwnik absorbuje niebieskie światło i emituje w dalekiej czerwieni, co sprzyja obrazowaniu na większych głębokościach komórek i dłuższym obserwacjom. Po związaniu jedynie z HaloTag jego emisja wzrastała; gdy HaloTag był zestrojony z białkowym partnerem, który owijał się wokół barwnika, jasność rosła jeszcze bardziej. Symulacje komputerowe potwierdziły, że w bardziej zwartych układach białkowych barwnik doświadcza silniejszego zagęszczenia, mniejszej odsłoniętej powierzchni i większej liczby stabilizujących kontaktów, które wszystkie ograniczają ruch i zwiększają emisję. Barwnik wiąże się też szybko i specyficznie z HaloTag, wykazuje bardzo niskie tło w komórkach pozbawionych taga i pozostaje nietoksyczny w stosowanych stężeniach, co wspiera jego użycie w eksperymentach na żywych komórkach. 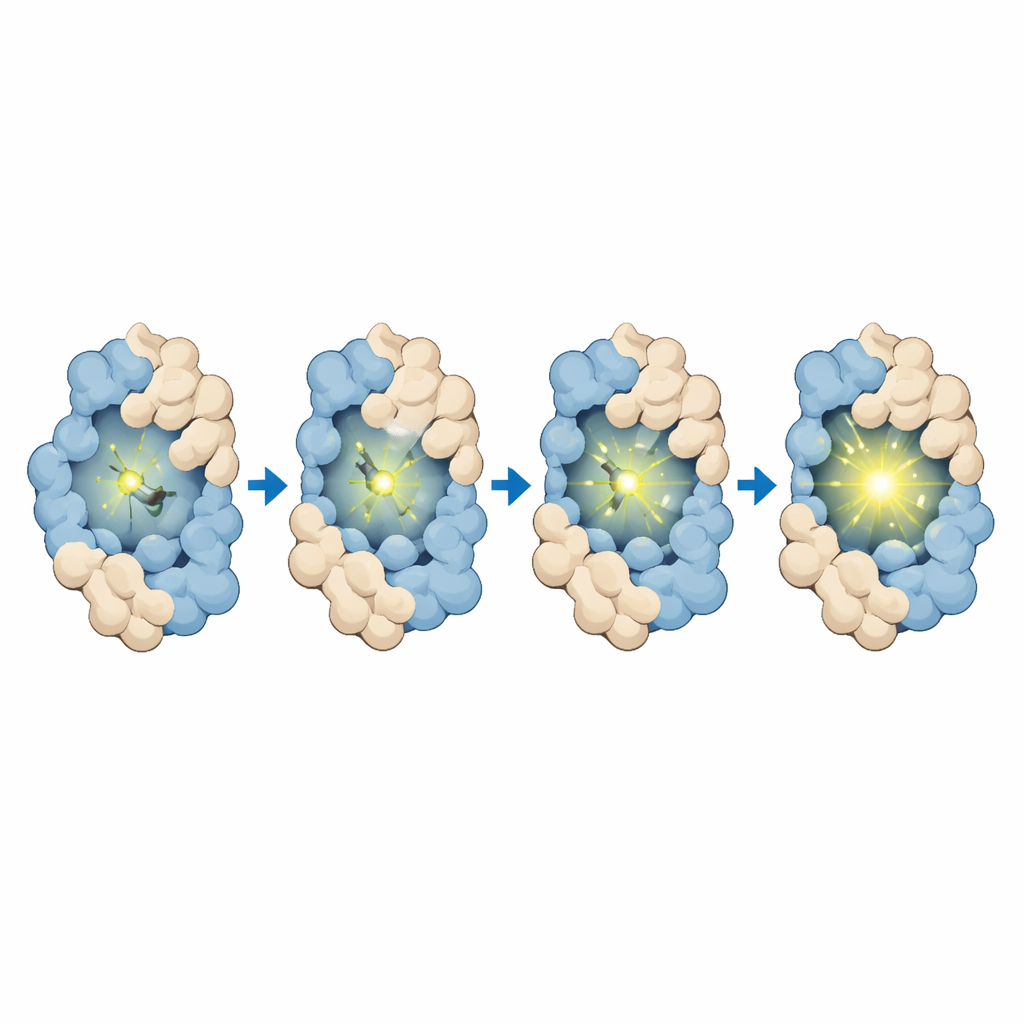
Śledzenie szybkich sygnałów i spotkań białek
Aby zademonstrować możliwości BIOSCE, autorzy zastosowali ją w kilku dobrze znanych procesach komórkowych. Najpierw zaadaptowali sensor wapnia oparty na kalmodulinie — białku zmieniającym kształt po związaniu jonów wapnia, które są centralnymi przekaźnikami przy wyładowaniach nerwowych i wielu innych zdarzeniach komórkowych. Poprzez zespolenie kalmoduliny z HaloTag i znakowanie MTPABP-Cl stworzyli chemigenetyczny wskaźnik nazwany SCECaMP. W komórkach ludzkich i komórkach podobnych do neuronów wskaźnik ten rozjaśniał się i przygasał synchronicznie ze skokami wapnia wywołanymi stymulacją potasem, z szybkościami reakcji porównywalnymi do szeroko stosowanych białek fluorescencyjnych GCaMP. Ponieważ sygnał BIOSCE zależy bezpośrednio od lokalnego zagęszczenia wokół barwnika, może wiernie odzwierciedlać strukturalne zmiany kalmoduliny, zapewniając jednocześnie stabilną, długotrwałą fluorescencję odpowiednią do przedłużonego obrazowania.
Widzenie interakcji wywołanych lekami i uszkodzeń przez toksyny
Następnie badacze sprawdzili, czy BIOSCE potrafi śledzić, kiedy dwa białka są zbliżane przez lek. Użyli klasycznego systemu, w którym rapamycyna ściąga razem dwóch partnerów, FKBP i FRB, w kluczowej ścieżce kontroli wzrostu. Przyłączając HaloTag do FKBP lub FRB i znakując MTPABP-Cl, zaobserwowali szybkie, milisekundowe wzrosty fluorescencji, gdy rapamycyna powodowała zbliżenie i przestawienie tych białek. Wzrost jasności odzwierciedlał ciasniejsze mikrośrodowisko wokół barwnika w miarę zbliżania się partnerów. W bardziej złożonym teście badali SNAP25, białko terminali nerwowych kluczowe dla uwalniania neuroprzekaźników i główny cel toksyny botulinowej A. Umieszczając HaloTag po obu stronach miejsca przecięcia przez toksynę i znakując barwnikiem, mogli oddzielnie śledzić ruchy fragmentów N- i C-końcowych po przecięciu. Śledzenie pojedynczych cząstek ujawniło, że jeden fragment pozostawał zakotwiczony w pobliżu błony komórkowej, podczas gdy drugi swobodniej dyfundował w cytoplazmie, a dokładny wzorzec zależał od tego, czy znakowanie nastąpiło przed czy po ekspozycji na toksynę. Sonda raportowała nawet szybkie, cynkowo-wywołane korekty konformacyjne w SNAP25 w tym procesie.
Co to znaczy dla biologii i medycyny
Razem wyniki te pokazują, że BIOSCE to wszechstronna nowa metoda wizualizacji tego, jak pojedyncze białka poruszają się, fałdują i wchodzą w interakcje wewnątrz żywych komórek na szerokim zakresie skal czasowych. Ponieważ metoda opiera się na ogólnym zespoleniu z HaloTag i pojedynczej małocząsteczkowej sondzie, można ją w zasadzie zastosować do wielu różnych białek bez konieczności projektowania całego sensora od nowa dla każdego przypadku. Ciągła, od zgęszczenia zależna zmiana jasności pozwala badaczom wykrywać subtelne przesunięcia strukturalne, zamiast tylko duże, binarne zdarzenia. Patrząc w przyszłość, autorzy planują ulepszyć dostarczanie sondy i głębokość obrazowania, aby BIOSCE mogła być używana w tkankach i całych zwierzętach. Jeśli się to powiedzie, podejście to może stać się potężnym narzędziem łączącym miejsce występowania białek, ich ruchy i funkcje w zdrowiu i chorobie, i ostatecznie zasilić szczegółowe modele komputerowe zachowań komórkowych.
Cytowanie: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Słowa kluczowe: dynamika konformacyjna białek, obrazowanie w żywych komórkach, fluorescencyjne biosensory, probki HaloTag, toksyna botulinowa