Clear Sky Science · pl
Zminimalizowane zużycie próbki w czasowo-rozwiązanej krystalografii seryjnej zastosowanej do cyklu redoksowego ludzkiej NQO1
Obserwowanie enzymów w działaniu przy mniejszym zużyciu cennych próbek
Współczesna biologia często korzysta z potężnych laserów rentgenowskich, aby zobaczyć, jak molekuły życia poruszają się i zmieniają kształt, ale takie eksperymenty zwykle pochłaniają ogromne ilości starannie przygotowanego białka. To badanie przedstawia nowy sposób „karmienia” drobnych kryształów białka do wolnoelektronowego lasera rentgenowskiego znacznie bardziej efektywnie, zmniejszając potrzebny materiał nawet o 97%. Pokazuje też, że ta oszczędniejsza metoda wciąż potrafi uchwycić wczesne etapy aktywności medycznie istotnego enzymu, otwierając drogę do bardziej rutynowych „filmów” pokazujących pracujące białka. 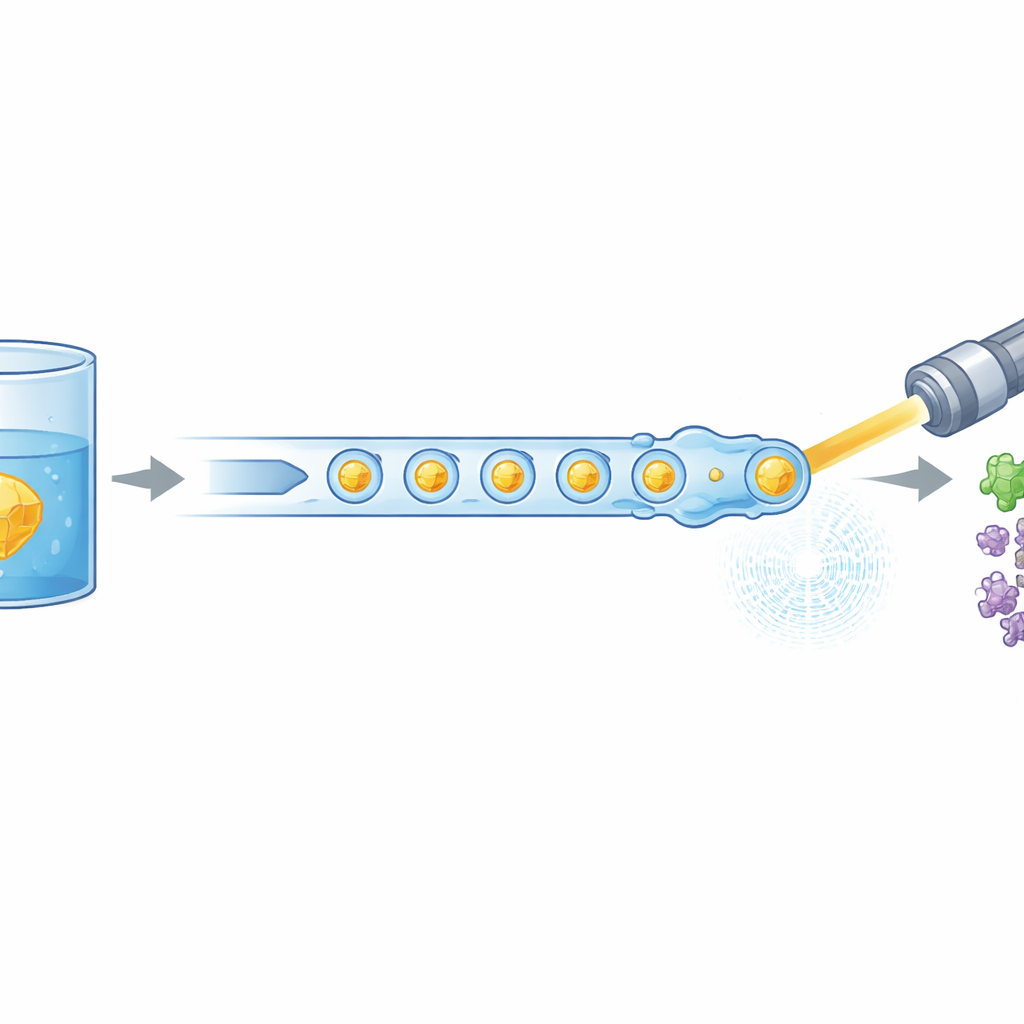
Dlaczego robienie molekularnych filmów jest tak kosztowne
Aby zrozumieć, jak białka wykonują swoje zadania, naukowcy coraz częściej przechodzą od statycznych zdjęć do sekwencji czasowych — „filmów”, które śledzą reakcje w czasie rzeczywistym. Jednym z wiodących podejść jest czasowo-rozwiązana krystalografia seryjna, która rozpyla miliony mikroskopijnych kryształów białka przez ultrajasną wiązkę rentgenowską. Każdy kryształ jest naświetlany tylko raz, co daje obraz wolny od uszkodzeń, a tysiące takich obrazów łączy się w pełny obraz struktury. Problem polega na tym, że każdy moment reakcji — jedna dziesiąta sekundy, pełna sekunda itd. — wymaga nowej partii kryształów. Ponieważ przygotowanie białka może być powolne i kosztowne, zużycie próbek stało się wąskim gardłem, szczególnie w najnowocześniejszych ośrodkach, takich jak European XFEL, gdzie impulsy rentgenowskie nadchodzą w szybkich pociągach z częstotliwością megahercową.
Nowy sposób dostarczania maleńkich kropli na żądanie
Naukowcy rozwiązali ten problem, przeprojektowując sposób dostarczania kryształów do wiązki rentgenowskiej. Zamiast ciągłego strumienia cieczy generują starannie odstępowany pociąg mikroskopijnych kropli, z których każda zawiera kryształy białka, oddzielonych fazą olejową. Miniaturowe, drukowane w 3D urządzenie łączy dwa strumienie — kryształy białka i rozpuszczonego partnera reakcji — w małe objętości mieszane, które następnie są odcinane jako krople. Krople te są kierowane przez dyszę skoncentrowaną gazem, która formuje wąski strumień zgodny z próżnią i prędkością XFEL. Kluczowe jest to, że produkcja kropli jest elektrycznie synchronizowana z rytmem pociągów impulsów rentgenowskich, dzięki czemu niemal każdy użyteczny impuls trafia w kroplę, zamiast w pustą ciecz. 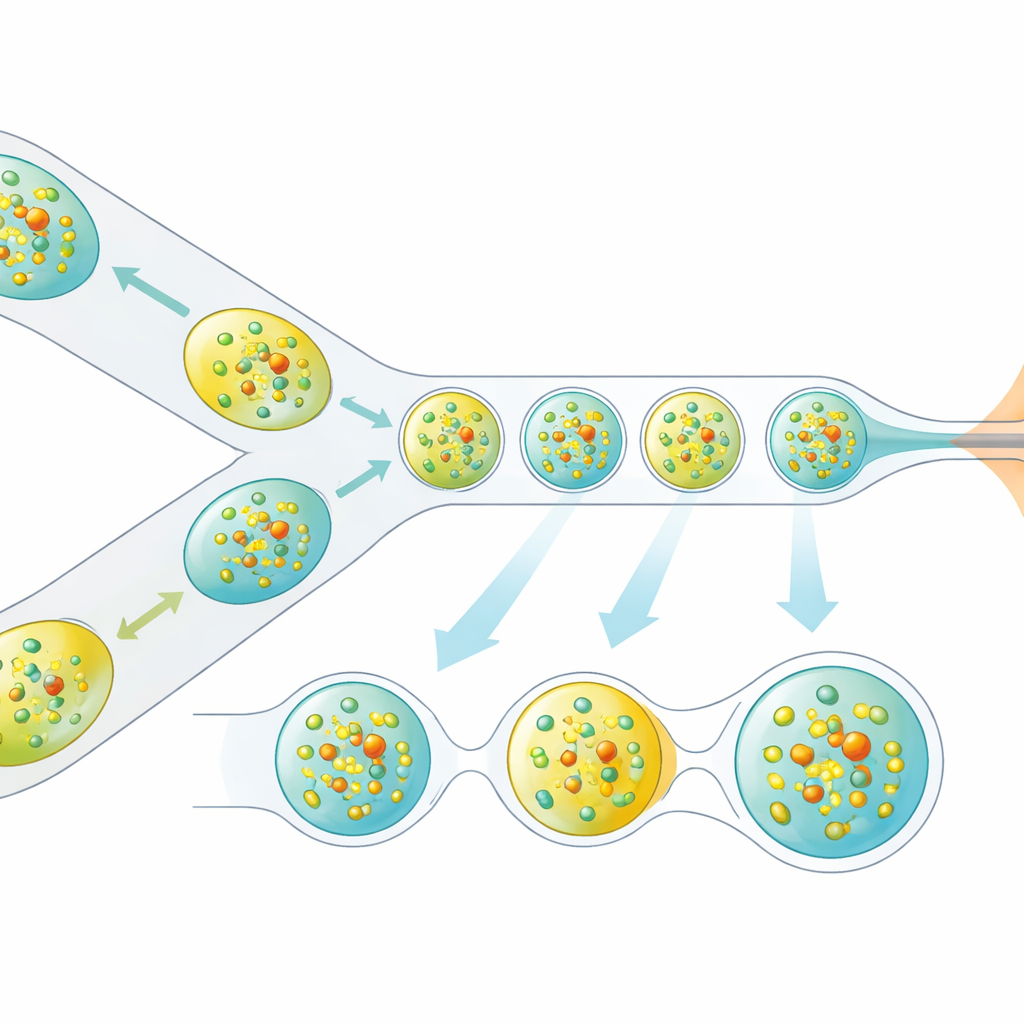
Weryfikacja metody na ludzkim enzymie
Aby udowodnić, że podejście oparte na kroplach działa w realnych zagadnieniach biologicznych, zespół przebadał NAD(P)H:chinon reduktazę 1 (NQO1), ludzki enzym zaangażowany w utrzymanie równowagi redoks w komórce i powiązany z chorobami. Wymieszali mikrokryształy NQO1 z jej naturalnym kofaktorem, NADH, i sondowali układ w dwóch wczesnych punktach czasowych: 0,3 sekundy i 1,2 sekundy po zmieszaniu. Analizując powstałe wzory dyfrakcyjne rentgenowskie, odtworzyli trójwymiarowe struktury enzymu dla każdego opóźnienia. Pomimo użycia dramatycznie mniejszej ilości białka niż w konwencjonalnych eksperymentach z ciągłym przepływem, jakość danych była wystarczająca, by ujawnić subtelne cechy gęstości elektronowej w miejscach aktywnych enzymu, zgodne z zaczynającym się wiązaniem NADH przy niskim zajęciu miejsc.
Co ujawniają wczesne strukturalne migawki
Struktury pokazują, że krótko po zmieszaniu nie wszystkie miejsca aktywne w krysztale zachowują się tak samo. W 0,3 sekundy oznaki obecności NADH pojawiają się wyraźnie w trzech z czterech miejsc aktywnych w komórce elementarnej i często w więcej niż jednym kształcie, co sugeruje, że kofaktor eksploruje kilka pozycji zanim ustabilizuje się. Po 1,2 sekundy niektóre z tych cech wyostrzają się do dominującego trybu wiązania, ale ogólny obraz pozostaje elastyczny i częściowo zajęty. To nierównomierne, zmienne zachowanie jest zgodne z wcześniejszymi dowodami biochemicznymi, że dwie jednostki partnera w dimerze NQO1 nie działają idealnie synchronicznie, lecz wykazują aktywność „połowy miejsc”, gdzie jedna strona pary angażuje się pierwsza, podczas gdy druga pozostaje w tyle. Dane czasowo-rozwiązane dają zatem wczesny strukturalny wgląd w to, jak ta asymetria realizuje się w przestrzeni rzeczywistej.
Oszczędzanie próbek przy zachowaniu wartości naukowej
Z praktycznego punktu widzenia metoda segmentowanych kropli zmniejszyła zużycie białka około sześciokrotnie dla pomiarów 0,3 sekundy i nawet do 97% dla eksperymentów 1,2 sekundy, w porównaniu z tradycyjnymi ciągłymi dyszami w podobnych warunkach. Mimo to dostarczyła wiarygodnych informacji strukturalnych w temperaturze pokojowej, zgodnych z wymagającą strukturą impulsów European XFEL. Dla osób niebędących specjalistami kluczowy wniosek jest taki, że badacze mogą teraz obserwować, jak enzymy takie jak NQO1 rozpoczynają swoją pracę w niemal rzeczywistym czasie, używając jedynie miligramów cennych próbek na punkt czasowy. Umożliwia to znacznie realniejsze badanie wielu czasów reakcji i wielu różnych białek, co ostatecznie pomaga wyjaśnić, jak medycznie istotne enzymy poruszają się, wyginają i współpracują wykonując chemię życia.
Cytowanie: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Słowa kluczowe: krystalografia seryjna, wolnoelektronowe lasery rentgenowskie, mikrofluidyka kroplowa, dynamika enzymów, NQO1