Clear Sky Science · pl
Warianty onkogennego PI3Kα ujawniają stopniowane spektrum konformacyjne z mutacjom- -specyficznymi ukrytymi kieszeniami
Kiedy jedna zmiana w DNA to za mało
Nowotwór bywa opisywany jako choroba mutacji, ale to badanie pokazuje, że nie wszystkie mutacje działają w pojedynkę. Naukowcy przeanalizowali kluczowy enzym kontrolujący wzrost, PI3Kα, i stwierdzili, że gdy dwie specyficzne zmiany w DNA występują razem w tej samej kopii genu, mogą przesunąć białko w kierunku bardziej aktywnych konformacji niż każda zmiana osobno. Ma to znaczenie, ponieważ nadaktywność PI3Kα napędza nowotwory, bierze też udział w łagodnych zespołach przerostowych i zaburzeniach rozwoju mózgu — oraz pomaga wyjaśnić, dlaczego niektóre guzy słabo reagują na dostępne leki.
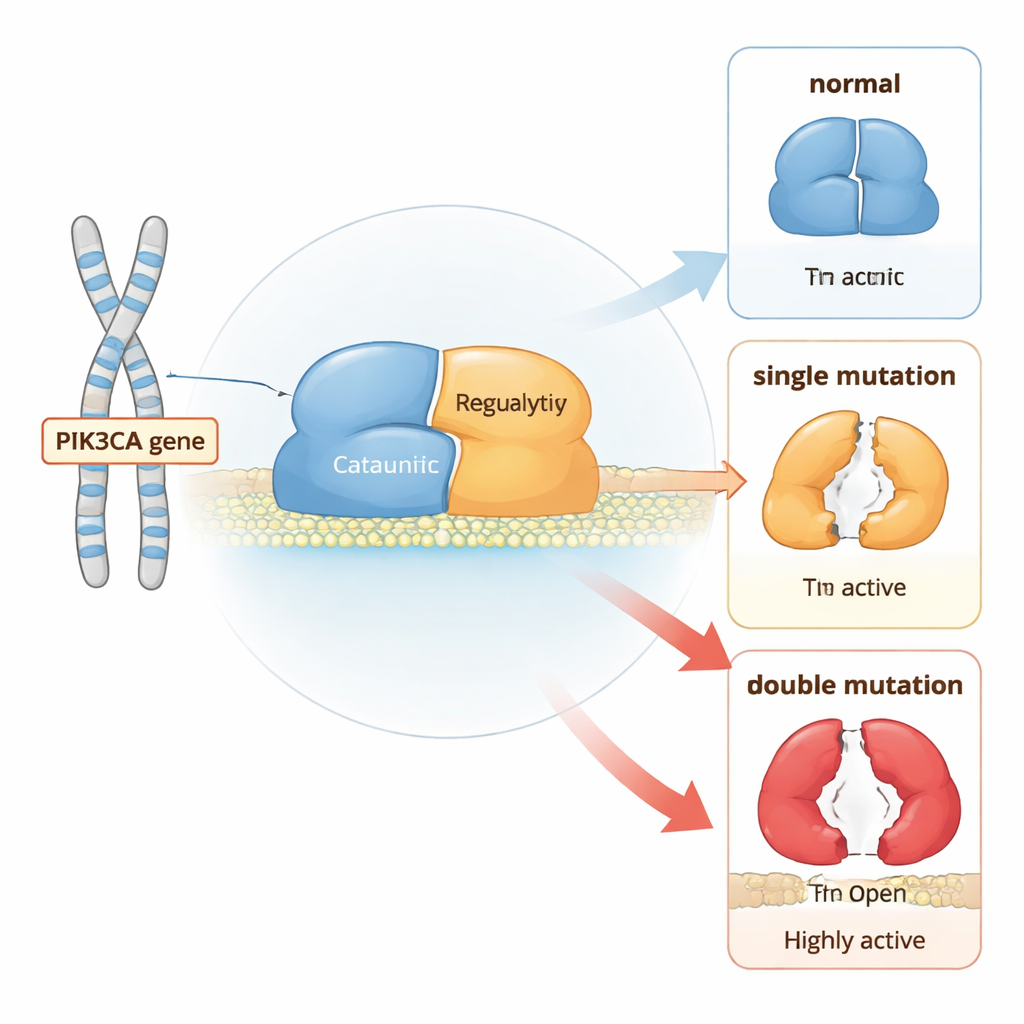
Cząsteczkowy przełącznik wzrostu komórki
PI3Kα to białko złożone z dwóch części, które lokalizuje się przy błonie komórkowej i przekazuje sygnały wzrostowe. W normalnych warunkach pozostaje przeważnie w pozycji „wyłączonej”, dopóki receptory na powierzchni komórki nie zostaną pobudzone. Wtedy PI3Kα przemieszcza się do błony i konwertuje lipid PIP2 do PIP3, co sygnalizuje komórce, by rosła i się dzieliła. Aby zapobiec niekontrolowanemu wzrostowi, kilka elementów białka działa jak wbudowane hamulce: jedna część zaciska rdzeń katalityczny, inna trzyma elastyczną pętlę aktywacyjną blisko, a podjednostka partnerska pomaga utrzymać cały kompleks w ryzach.
Jak pojedyncze i podwójne mutacje przechylają równowagę
Wykorzystując długie symulacje na poziomie atomowym, autorzy porównali normalne PI3Kα z wersjami zawierającymi pojedyncze „hotspotowe” mutacje związane z rakiem oraz kombinacje hotspotu z słabszą mutacją w tej samej cząsteczce. Stwierdzili, że każda mutacja zmienia częstotliwość występowania bardziej otwartych, aktywnych kształtów białka, ale mutacje podwójne przesuwają tę równowagę znacznie dalej niż pojedyncze. W szczególności niektóre pary mutacji współdziałają, rozluźniając kontakty utrzymujące element regulacyjny (zwany nSH2) na miejscu oraz przesuwając inny segment (iSH2) z jego miejsca dokowania. Ta skoordynowana ruchomość odblokowuje rdzeń katalityczny, ułatwiając białku przejście do błony i rozpoczęcie sygnalizacji.
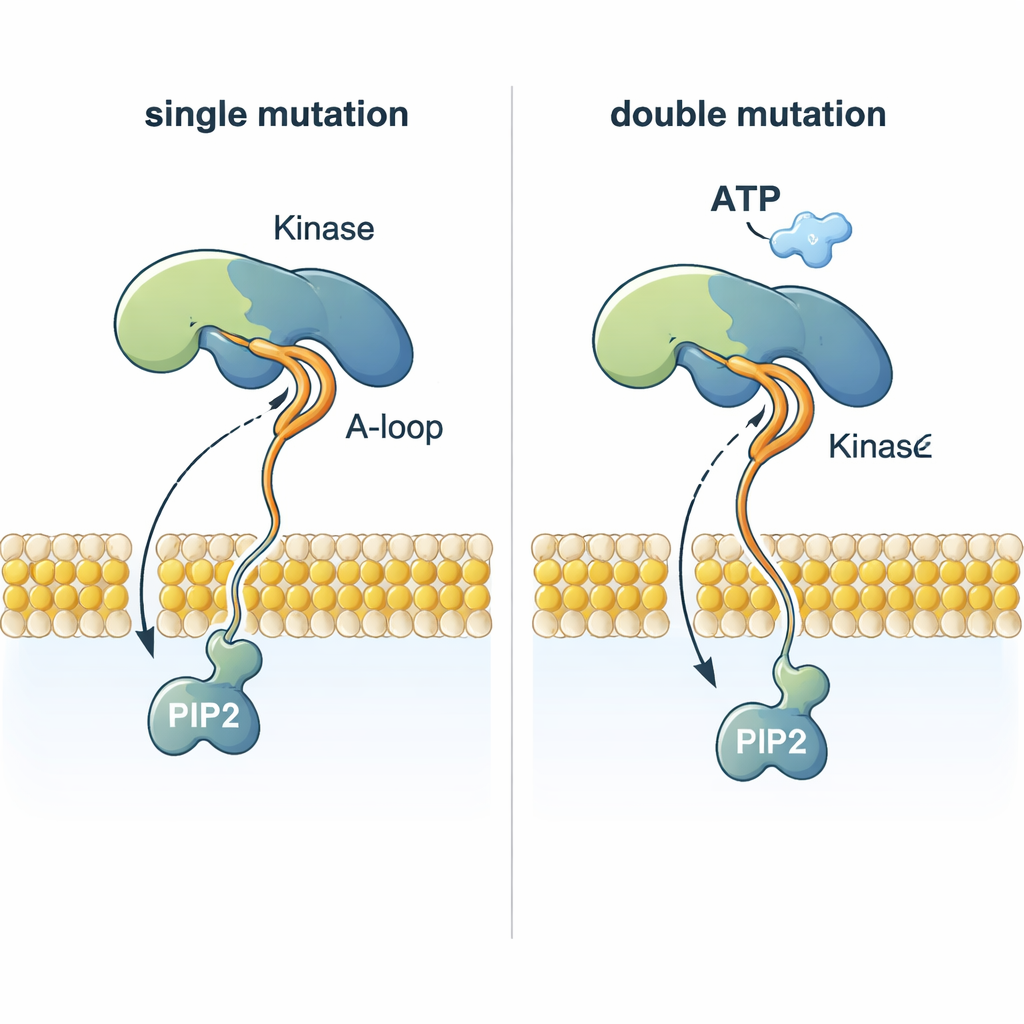
Ułatwianie dojścia substratu do miejsca reakcji
Zagadką jest, jak PI3Kα może przenieść grupę fosforanową z ATP — które leży niemal 2 nanometry nad błoną — na PIP2, osadzony w błonie. Symulacje pokazują, że pewne mutacje przebudowują elastyczną pętlę aktywacyjną tak, że silnie dodatnio naładowany fragment wyciąga się w stronę błony. Ta pętla może chwycić ujemnie naładowaną główkę PIP2, wyciągnąć ją z warstwy lipidowej i poprowadzić ku ATP. Mutacje podwójne, łączące zmianę kotwiczącą przy błonie z taką, która modyfikuje tę pętlę, koordynują PIP2 znacznie efektywniej niż normalne PI3Kα czy mutacje pojedyncze, dając strukturalne wyjaśnienie, dlaczego guzy z dwiema mutacjami PI3Kα mogą być szczególnie agresywne.
Ukryte miejsca na leki ujawnione przez ruch
Ponieważ PI3Kα jest duży i elastyczny, pojedynczy lek skierowany na jego miejsce aktywne często ma trudności z działaniem na wszystkie formy mutacyjne i może powodować efekty uboczne, takie jak poważne zaburzenia poziomu cukru we krwi. Śledząc, jak białko „oddycha” i ugina się w czasie, badacze odkryli «kryptyczne» kieszenie — tymczasowe rowki, które otwierają się tylko w określonych konformacjach mutantów i są niewidoczne w statycznych strukturach krystalicznych. Kieszenie te pojawiają się w lokalizacjach specyficznych dla mutacji, na przykład w pobliżu regionów wykazujących najsilniejsze ruchy w określonych mutantach podwójnych. Sugeruje to, że starannie zaprojektowane leki allosteryczne, które wiążą się z dala od miejsca aktywnego, mogłyby być dopasowane do blokowania poszczególnych wariantów mutantów w bezpieczniejszych, mniej aktywnych konformacjach.
W stronę mądrzejszych terapii kombinowanych
Podsumowując, praca wspiera pogląd „uderzenia dwoma pięściami” w genetyce nowotworów: silna mutacja hotspotowa wraz ze słabszym partnerem w tej samej cząsteczce PI3Kα może stworzyć stopniowane spektrum bardziej aktywnych form, często związanych z poważniejszymi wynikami klinicznymi. W terapii autorzy argumentują, że zamiast polegać na jednym inhibitorze, skuteczniejsze może być łączenie leków celujących w różne kieszenie — jednej w miejscu aktywnym i jednej lub więcej allosterycznych, które istnieją tylko w określonych mutantach. Takie koktajle mogłyby teoretycznie precyzyjniej wyciszyć aktywność PI3Kα, zmniejszyć toksyczne skutki uboczne i lepiej dopasować leczenie do dokładnego wzoru mutacji stwierdzonego w guzie pacjenta.
Cytowanie: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Słowa kluczowe: PI3K alfa, mutacje onkogenne, inhibitory allosteryczne, dynamika molekularna, transdukcja sygnału