Clear Sky Science · pl
Dynamika kondensatów biologicznych silnie zależna od sekwencji i skali długości w białkach nieuporządkowanych o dużym ładunku
Dlaczego małe krople białek mają znaczenie
W naszych komórkach wiele kluczowych reakcji zachodzi w miękkich, kroplopodobnych strukturach pozbawionych otaczającej ich błony. Te „kondensaty biomolekularne” zachowują się jak maleńkie ciekłe przedziały i często zbudowane są z giętkich, silnie naładowanych białek. Eksperymenty wykazały, że cząsteczki wewnątrz niektórych z tych kropli mogą poruszać się zaskakująco szybko, choć same krople bywają dość gęste i lepki. W artykule postawiono proste, lecz istotne pytanie: jak dokładny układ ładunków dodatnich i ujemnych wzdłuż tych białek kontroluje szybkość ruchu wewnątrz takich kropli?
Budowanie kropli z giętkich łańcuchów ładunkowych
Autorzy koncentrują się na białkach wewnętrznie nieuporządkowanych — długich, elastycznych łańcuchach, które nie składają się w sztywne kształty. Wiele z tych łańcuchów niesie zarówno ładunki dodatnie, jak i ujemne, ułożone w różne wzory wzdłuż długości. Wykorzystując wielkoskalowe symulacje komputerowe, zespół stworzył modele kropli złożonych z wielu kopii takich białek, wraz z wodą i małymi jonami, aby odzwierciedlić zatłoczone wnętrze rzeczywistych kondensatów. Systematycznie zmieniali stopień „blokowości” wzoru ładunków — od sekwencji, w których ładunki dodatnie i ujemne naprzemiennie występują, po sekwencje, w których wszystkie ładunki dodatnie są zgrupowane razem, a ujemne tworzą odrębny blok.
Udział wody i przepływ kształtują ruch
Symulacje ujawniły, że te krople mogą nadal zachowywać się jak prawdziwe ciecze o bardzo wysokiej zawartości wody — między około 55% a 84%, w zależności od układu ładunków. Taka ilość wody oznacza, że przepływ płynu, czyli hydrodynamika, nie jest całkowicie stłumiony, jak sugerowałyby liczne teorie dotyczące gęstych roztworów polimerów. Śledząc, jak segmenty białek przemieszczają się w czasie, autorzy wykryli wzory ruchu charakterystyczne dla łańcuchów, których ruch jest wspomagany przez otaczający płyn, zamiast być hamowany wyłącznie przez tarcie. Ten hydrodynamiczny wpływ utrzymuje się do rozmiaru, a nawet powyżej rozmiaru całego łańcucha białkowego, szczególnie w kroplach z sekwencji o bardziej wymieszanych ładunkach, a więc zawierających więcej wody.
Lokalne wzory ładunków sterują mikroelastycznością
Patrząc dokładniej, autorzy zbadali, jak krótkie odcinki każdego łańcucha relaksują się i reorganizują wewnątrz kropli. Różne części tego samego białka, zawierające taką samą liczbę jednostek budulcowych, mogły poruszać się w bardzo różnym tempie w zależności od lokalnego stosunku ładunków dodatnich i ujemnych. Odcinki o bardziej zrównoważonym ładunku relaksowały się szybciej, podczas gdy fragmenty zdominowane przez jeden rodzaj ładunku poruszały się powoli. Co zaskakujące, różnice te pozostawały silne, mimo że proste argumenty o ekranowaniu sugerowałyby, że efekty elektrostatyczne powinny być krótkozasięgowe w takich słonych, zatłoczonych warunkach. Praca pokazuje, że fakt związania ładunków wzdłuż łańcucha zachowuje dalekosiężne korelacje elektryczne, które mocno wpływają na lokalny ruch.
Lepkość zależy od rozmiaru sondy
Zespół następnie zapytał, jak „gęste” wydają się te krople na różnych skalach długości. Używając metody łączącej drobne fale pędu płynu z jego odpornością na przepływ, obliczyli lepkość zależną od długości pomiarowej. Dla wszystkich sekwencji ciecz wydaje się rzadsza przy badaniu bardzo małych skal i gęstsza przy badaniu w skali całej kropli. Ta zależność od rozmiaru jest szczególnie dramatyczna dla sekwencji o blokowych ładunkach: dla najbardziej segregowanego wzoru lepkość makroskopowa jest ponad dwadzieścia razy większa niż lepkość lokalna na poziomie monomeru. Dla porównania, krople z dobrze wymieszanymi sekwencjami wykazują znacznie mniejszą różnicę. Ogólnie lepkość makroskopowa rośnie stromo wraz ze stężeniem białka, zgodnie z zachowaniem gęstych roztworów neutralnych polimerów, mimo że same białka są silnie naładowane.
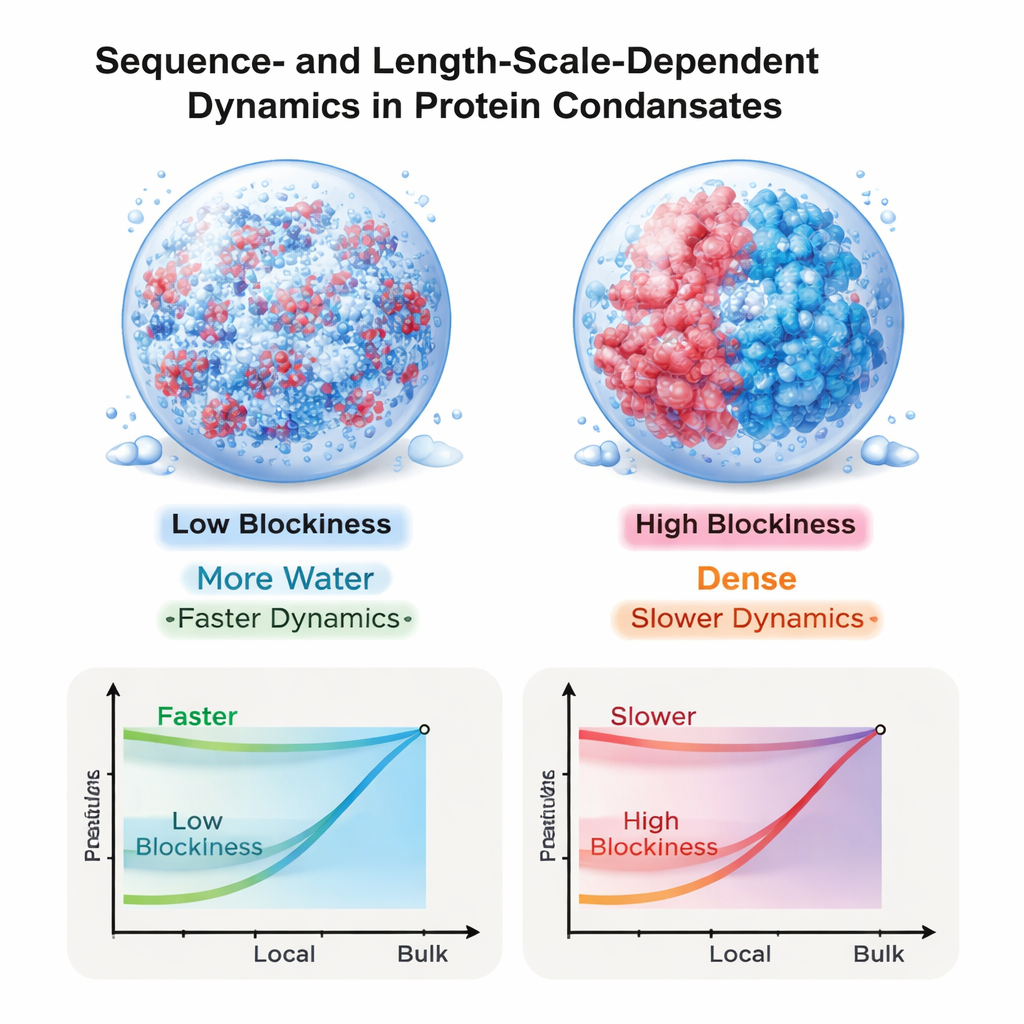
Łączenie symulacji z intrygującymi eksperymentami
Wyniki te pomagają rozwiązać widoczny paradoks z ostatnich eksperymentów: jak małe molekuły i odcinki białek mogą dyfundować tak szybko wewnątrz kondensatów, które mierząc jako całość wydają się wyjątkowo lepkie? Odpowiedź, jaka wyłania się z tej pracy, jest taka, że zarówno przepływ wody, jak i dalekosiężne interakcje elektrostatyczne pozostają istotne w tych kroplach, a ich wpływ jest ściśle kontrolowany przez to, jak ładunki są uporządkowane wzdłuż każdego łańcucha. Sekwencje z blokowymi wzorami ładunków tworzą gęste, bardzo lepkie krople, które mimo to pozostają stosunkowo płynne na skali mikroskopowej, podczas gdy bardziej wymieszane sekwencje dają środowiska ogólnie bardziej ruchliwe. Pokazując, że sekwencja ładunków może regulować ruch różnie na różnych skalach długości, badanie dostarcza zasady projektowej dla inżynierii syntetycznych materiałów białkowych i wyjaśnia, jak komórki mogą programować zachowanie kondensatów przez szczegółową sekwencję swoich białek nieuporządkowanych.
Cytowanie: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Słowa kluczowe: kondensaty biomolekularne, białka wewnętrznie nieuporządkowane, układanie ładunków, dynamika białek, lepkość