Clear Sky Science · pl
Zintegrowany proces badawczy do ustalania struktury nanokrystalicznych proszków
Dlaczego małe kryształy mają znaczenie
Wiele współczesnych leków i zaawansowanych materiałów wytwarza się w postaci drobnych proszków, a nie pięknych, błyszczących kryształów. To problem dla naukowców, ponieważ nasze najlepsze narzędzie do ustalania rozmieszczenia atomów w ciele stałym — krystalografia rentgenowska — wymaga dużych, niemal doskonałych kryształów. W artykule przedstawiono nową, krok po kroku strategię ustalania pełnej struktury atomowej opornych proszków w rozmiarze nano, takich jakie często powstają przy bardziej ekologicznym, oszczędzającym rozpuszczalniki sposobie produkcji. Zrozumienie tych struktur może pomóc poprawić rozpuszczalność leków, ich stabilność i niezawodność działania w organizmie.
Wyzwanie niewidocznych atomów
Metody mechanochemiczne, takie jak mielenie składników w młynie zamiast rozpuszczania ich w dużych objętościach rozpuszczalnika, zyskują na popularności zgodnie z zasadami zielonej chemii. Mogą tworzyć nowe formy stałe leków — na przykład sole i kocrystaly — które dostrajają właściwości takie jak rozpuszczalność i trwałość. Jednak te same cechy, które czynią te metody atrakcyjnymi, utrudniają pracę krystalografom: zazwyczaj dają one tylko kryształy w rozmiarze nano- lub mikro-, czasem zmieszane z materiałem amorficznym. Tradycyjna dyfrakcja rentgenowska na pojedynczych kryształach nie radzi sobie z tak drobnymi ziarniami, natomiast proszkowa dyfrakcja rentgenowska często ma trudności z złożonością współczesnych stałych form farmaceutycznych.
Zestaw narzędzi do zobaczenia niewidzialnego
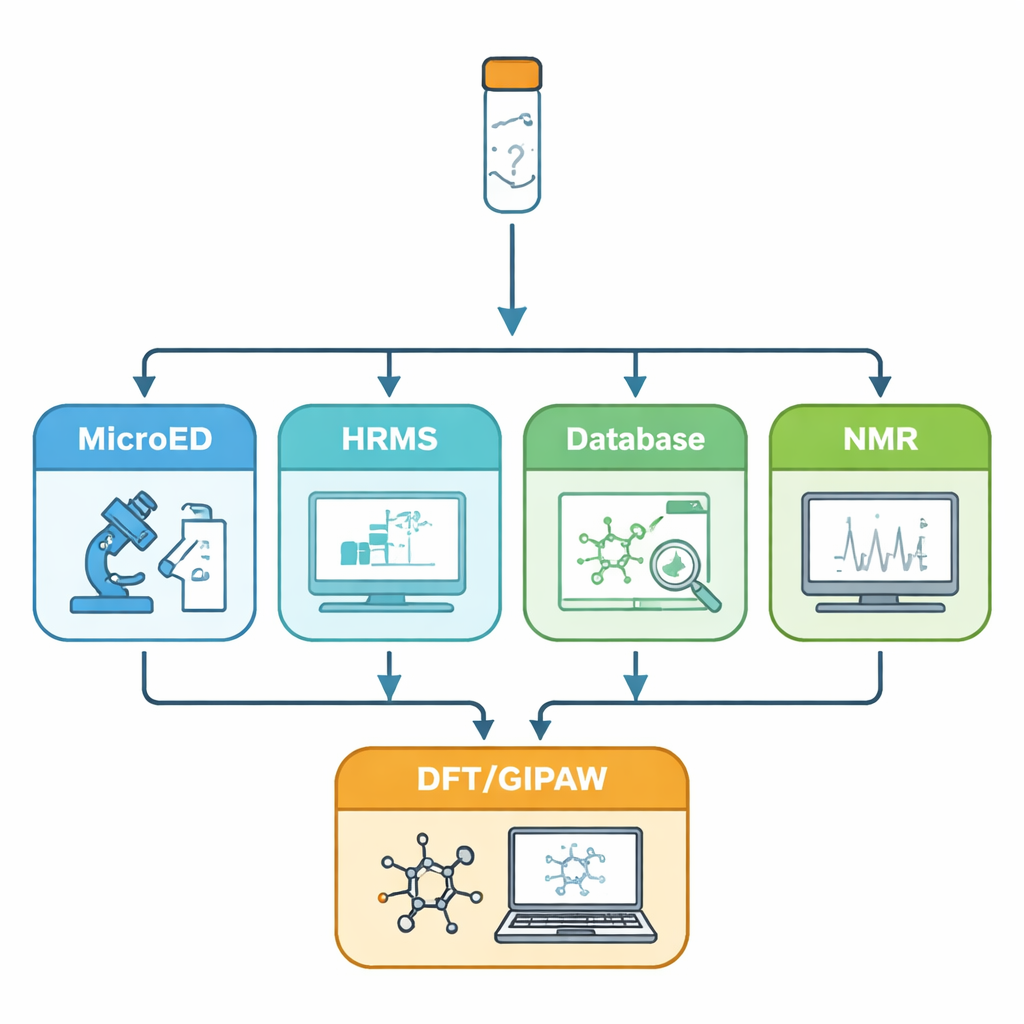
W ostatnich latach mikrokryształowa dyfrakcja elektronowa (MicroED) wyłoniła się jako potężny sposób uzyskiwania informacji na poziomie atomowym z kryształów liczących zaledwie kilkaset nanometrów. Elektrony oddziałują z materią silniej niż promieniowanie rentgenowskie, więc nawet te niewielkie kryształy mogą dawać ostre wzory dyfrakcyjne. MicroED może ujawnić podstawowy układ — „szkielet” — cząsteczek w ciele stałym. Ma jednak dwa istotne słabe punkty: atomy wodoru są bardzo trudne do zobaczenia, a atomy takie jak węgiel, azot i tlen bywają trudne do rozróżnienia. Autorzy rozwiązują te ograniczenia, łącząc MicroED z szeregiem narzędzi uzupełniających: wysokorozdzielczą spektrometrią mas do ustalenia dokładnej formuły molekularnej, przeszukiwaniem baz danych w celu zaproponowania prawdopodobnych tożsamości cząsteczkowych, spektroskopią NMR w roztworze i w stanie stałym dla potwierdzenia obecnych cząsteczek i ich wzajemnych oddziaływań oraz obliczeniami kwantowomechanicznymi do dopracowania i walidacji końcowej struktury.
Rozwiązanie dwóch rzeczywistych zagadek
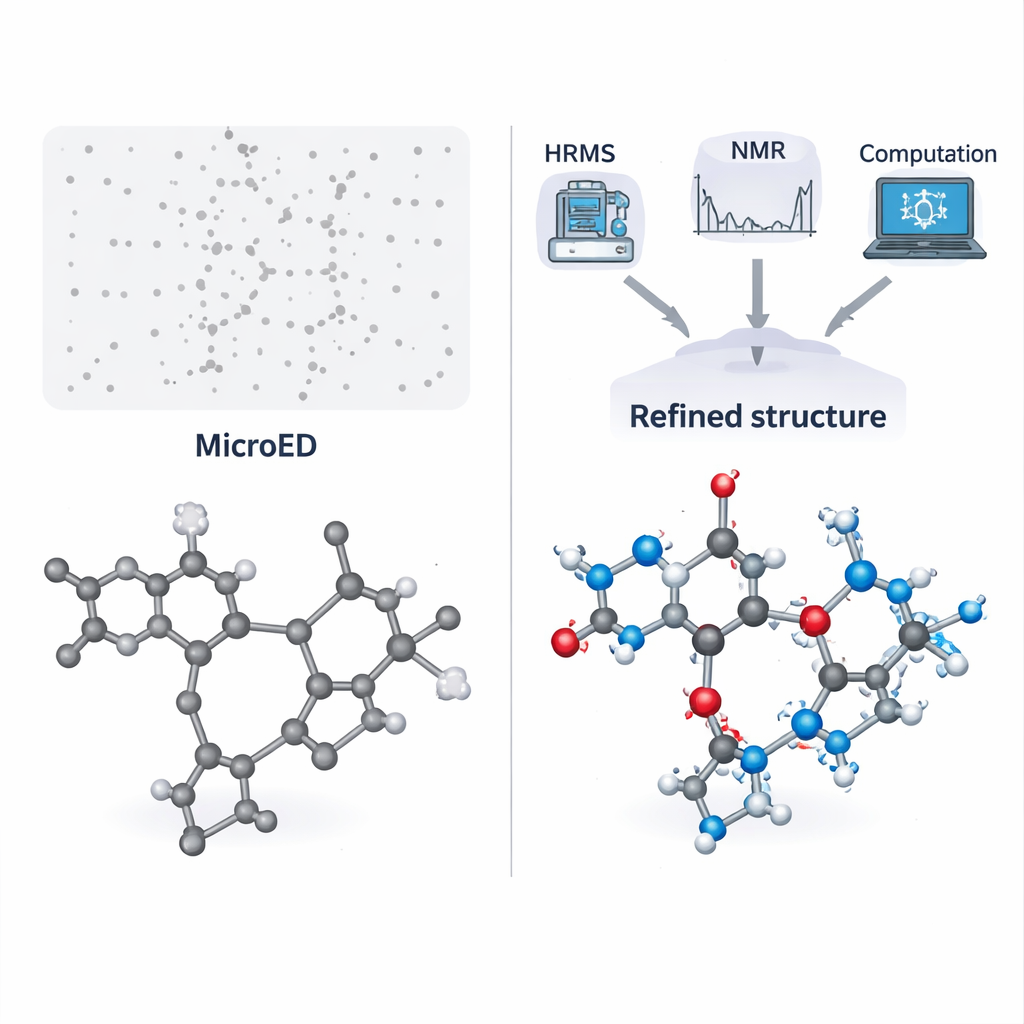
Zespół najpierw zastosował ten obieg badawczy do trudnej soli powstałej z pirydoksyny (formy witaminy B6) i przeciwutleniacza N‑acetyl‑L‑cysteiny. Materiał ten można otrzymać tylko przez suche mielenie, a wielokrotne próby wyhodowania odpowiednich pojedynczych kryształów nie powiodły się, ponieważ produkt jest lepki. MicroED wykazał, że proszek zawierał dwa różne składniki molekularne i zasugerował obecność atomu siarki, ale nie był w stanie wiarygodnie przypisać wszystkich pozostałych atomów ani atomów wodoru. Wysokorozdzielcza spektrometria mas ujawniła dwa precyzyjne masy molowe, które następnie użyto do przeszukania baz danych chemicznych w poszukiwaniu pasujących struktur. Porównując te kandydatury ze szkieletem MicroED i sprawdzając kluczowe cechy za pomocą NMR roztworowego, autorzy zawęzili możliwości i z pewnością zidentyfikowali dwie cząsteczki jako pirydoksynę i N‑acetyl‑L‑cysteinę.
Od szkicu do gotowego obrazu
Gdy tożsamości molekularne zostały ustalone, obliczenia kwantowochemiczne na komputerze posłużyły do delikatnego zrelaksowania struktury pochodzącej z MicroED i przewidzenia przesunięć chemicznych w NMR. Te obliczone sygnały NMR porównano następnie z danymi NMR w stanie stałym uzyskanymi z rzeczywistego proszku. Doskonałe dopasowanie potwierdziło, że pozycje atomów, łącznie z większością wodorów, były poprawne. Dodatkowe eksperymenty NMR skoncentrowały się na jednym kluczowym atomie wodoru współdzielonym między dwiema cząsteczkami, co pozwoliło zespołowi bardzo precyzyjnie zmierzyć jego odległość do atomu azotu. Wykazało to, że para tworzy prawdziwą sól, a nie neutralny kocrystal — ważne rozróżnienie dla właściwości leku i klasyfikacji regulacyjnej. Ten sam obieg badawczy przetestowano następnie na drugim, zupełnie innym związku: małym tripeptydzie zwanym fMLF, powszechnie używanym jako system modelowy w badaniach NMR, którego struktura w stanie stałym nigdy wcześniej nie była zgłaszana. Ponownie, zintegrowane podejście dostarczyło w pełni zwalidowaną strukturę i nawet rzuciło światło na szybkie ruchy pierścienia aromatycznego.
Jak to pomaga nauce i medycynie
Traktując każdy nieznany proszek jak „test ślepy”, autorzy pokazują, że ich modułowy proces może zaczynać od bardzo ograniczonych informacji, a mimo to dojść do kompletnej, godnej zaufania struktury atomowej. MicroED dostarcza pierwszego szkicu, spektrometria mas i bazy danych identyfikują kandydatów molekularnych, NMR wyjaśnia, ile jest komponentów i gdzie znajdują się wodory, a obliczenia kwantowe spajają całość. Dla chemików i naukowców farmaceutycznych oznacza to, że złożone, nanokrystaliczne proszki powstające w ekologicznych procesach produkcyjnych nie muszą pozostawać zagadką strukturalną. Metoda otwiera drogę do rutynowej, szczegółowej charakterystyki proszków — od pigmentów po formulacje leków — nawet gdy tradycyjne hodowle kryształów zawodzą, pomagając projektować bezpieczniejsze i bardziej efektywne materiały od podstaw.
Cytowanie: Sabena, C., Bravetti, F., Miyauchi, N. et al. An integrated workflow for the structure elucidation of nanocrystalline powders. Commun Chem 9, 97 (2026). https://doi.org/10.1038/s42004-026-01902-1
Słowa kluczowe: MicroED, magnetyczny rezonans jądrowy w stanie stałym, nanokrystaliczne proszki, synteza mechanochemiczna, sole farmaceutyczne