Clear Sky Science · pl
Dynamika foto-utleniania CO do CO2 na rutylówym (110)
Dlaczego obserwowanie molekuł w trylionowej części sekundy ma znaczenie
Współczesne życie opiera się na reakcjach chemicznych, które oczyszczają powietrze i wodę oraz przekształcają światło słoneczne w użyteczną energię. Wiele z tych reakcji zachodzi na powierzchniach stałych materiałów zwanych fotokatalizatorami, napędzanych światłem. W tym badaniu przyglądamy się jednej z takich reakcji — jak trujący tlenek węgla (CO) przekształcany jest w dwutlenek węgla (CO2) na powierzchni tlenku tytanu — na skalach czasowych rzędu zaledwie biliardowych części sekundy. Zrozumienie tych ultraszybkich etapów może pomóc naukowcom projektować lepsze materiały do kontroli zanieczyszczeń, powierzchni samoczyszczących się i technologii energetyki słonecznej.
Załoga sprzątająca napędzana światłem
Tlenek tytanu to wszechstronny materiał stosowany w samoczyszczących się oknach, powłokach oczyszczających powietrze i eksperymentalnych urządzeniach do produkcji paliw słonecznych. Jest tani, stabilny i potrafi wykorzystać światło do wywoływania silnych reakcji czyszczących na swojej powierzchni. Nie wszystkie jednak formy tlenku tytanu zachowują się tak samo. Dwie powszechne formy, zwane anatazem i rutylem, różnią się wydajnością w napędzaniu reakcji, takich jak przekształcanie CO w CO2. Choć anataz zwykle jest bardziej aktywny globalnie, szczegóły czasowe poszczególnych etapów reakcji — zwłaszcza aktywacji tlenu z powietrza — pozostawały niejasne. To badanie koncentruje się na formie rutylówiej o określonej orientacji powierzchniowej, oznaczonej jako (110), aby zobaczyć, jak szybko CO jest utleniany po naświetleniu materiału.
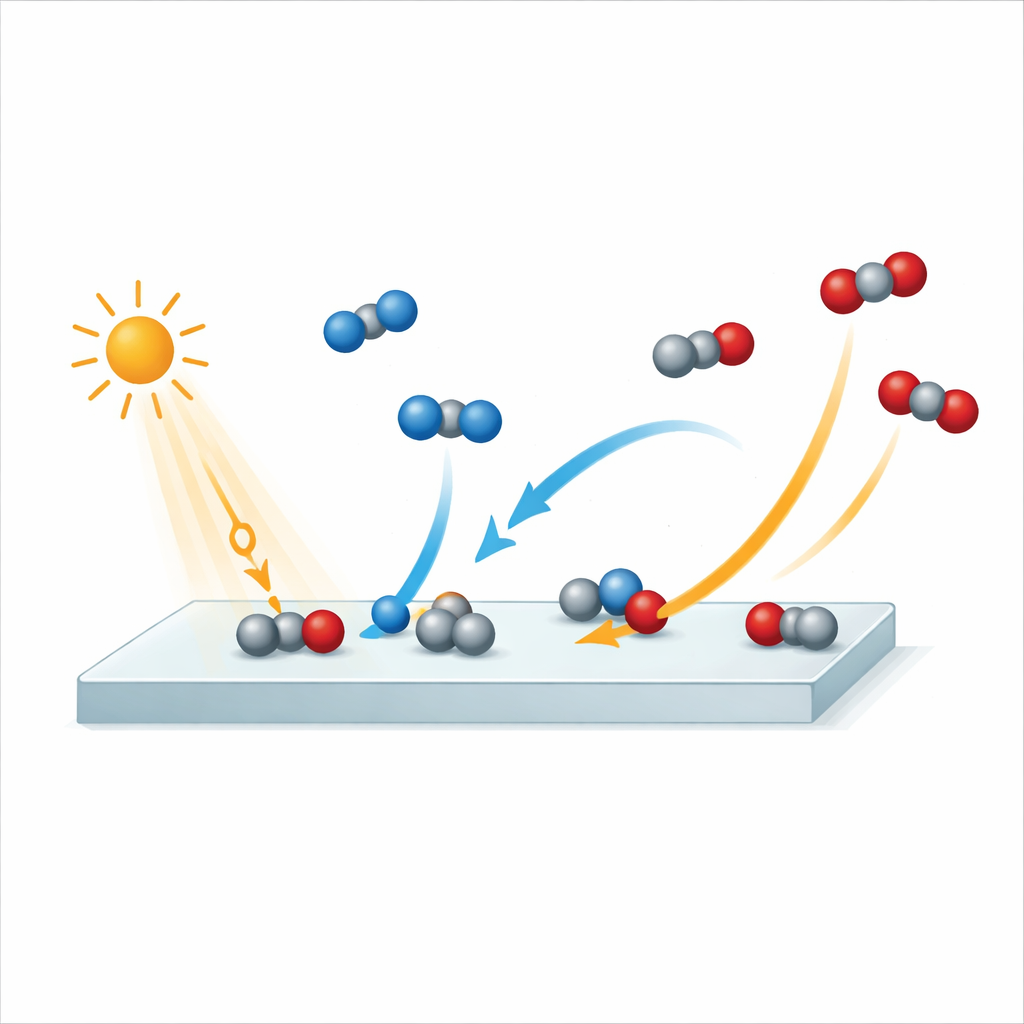
Nagrywając reakcję z ekstremalną prędkością
Aby uchwycić ten proces, badacze użyli lasera swobodnych elektronów w Hamburgu, który generuje niezwykle krótkie błyski promieniowania rentgenowskiego. Najpierw powierzchnię rutylu uderzono impulsem światła podczerwonego, pełniącym rolę małego flesza rozpoczynającego reakcję. Starannie zsynchronizowany impuls rentgenowski następnie sondował, jak zmieniają się atomy i elektrony na powierzchni. Powtarzając tę sekwencję przy różnych opóźnieniach między impulsami świetlnymi i rentgenowskimi, zbudowano rodzaj „molekularnego filmu” reakcji z rozdzielczością czasową około 250 femtosekund — jedna femtosekunda to milionowa część miliardowej części sekundy. Zespół monitorował sygnały pochodzące od atomów tlenu na powierzchni i w cząsteczkach gazu, co pozwoliło rozróżnić CO, CO2, wodę oraz sam tlenek podczas rozwijania się reakcji.
Uchwycenie CO2 w czasie krótszym niż trylionowa część sekundy
Kluczowa obserwacja to pojawienie się nowego CO2 na powierzchni rutylu już w ciągu 200 do 800 femtosekund po impulsie świetlnym. Oznacza to, że tlen z pobliskich cząsteczek O2 zostaje aktywowany, wiązania się zrywane, a CO przekształcone w CO2 w czasie krótszym niż jedna trylionowa część sekundy. Po około 0,8 pikosekundy świeży sygnał CO2 zanika, gdy produkt odczepia się od powierzchni. Co ciekawe, cała ta sekwencja zachodzi szybciej na rutylu niż na anatazie, gdzie wcześniejsze badania wykazały pojawienie się pierwszego CO2 dopiero po około 1,2–2,8 pikosekundy przy podobnych warunkach. Mimo że anataz wytwarza ogólnie więcej CO2 i uważa się go za silniejszy fotokatalizator, rutyl przeprowadza kluczowy krok utleniania szybciej.
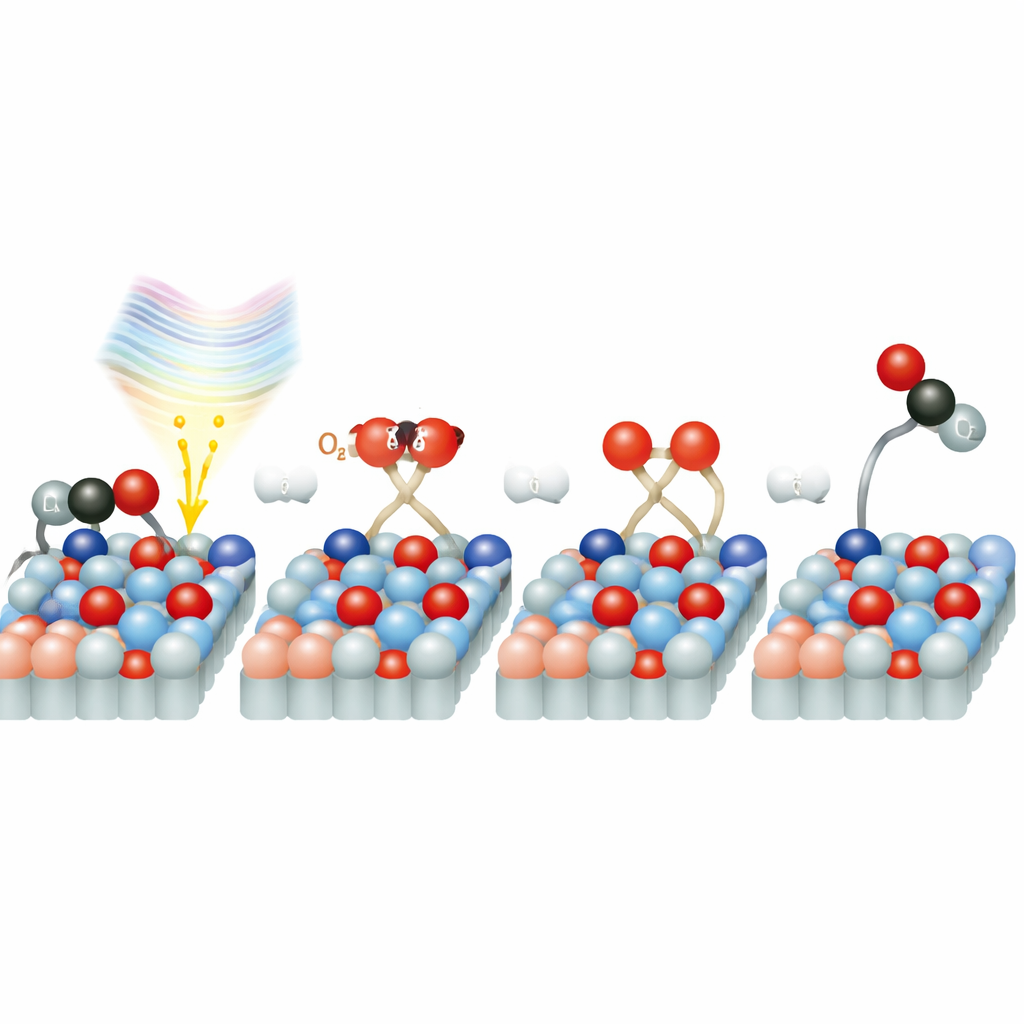
Skrócona ścieżka dla tlenu
Dlaczego reakcja jest tak szybka na rutylu? Szczegółowe symulacje komputerowe sugerują, że cząsteczki tlenu siedzące na powierzchni tworzą specjalne stany elektroniczne, które działają jak pomost między ciałem stałym a O2. Gdy absorbowane jest światło laserowe o długości fali 770 nanometrów, może ono bezpośrednio przemieścić elektron z tlenku tytanu do cząsteczki tlenu, tworząc naładowane, aktywowane gatunki tlenowe. Ten „skrót” omija wolniejszą drogę, w której elektrony najpierw przemieszczają się przez objętość ciała stałego, a dopiero potem docierają do powierzchni. Po aktywacji tlen szybko rozpada się, a jeden atom tlenu łączy się z CO, tworząc CO2. Badanie wykazuje także, że śladowe ilości wody na powierzchni mogą zarówno blokować miejsca reakcyjne, jak i przy niskich stężeniach potencjalnie wspomagać transfer ładunku i aktywację tlenu, dodając kolejną warstwę złożoności.
Łączenie struktury elektronowej z wydajnością w praktyce
Ogólnie rzecz biorąc, praca pokazuje, że drobne szczegóły dotyczące poruszania się elektronów między powierzchnią a pobliskimi cząsteczkami mogą dramatycznie zmieniać szybkość reakcji, nawet między dwoma blisko spokrewnionymi materiałami. Choć anataz nadal wygrywa pod względem całkowitej wydajności fotokatalitycznej, rutyl wykazuje szybszy etap aktywacji tlenu powiązany z tą szczególną ścieżką transferu ładunku. Łącząc ultraszybkie pomiary z zaawansowanymi symulacjami, badanie dostarcza wskazówek, jak modyfikować powierzchnie, aby reakcje wywoływane światłem przebiegały wydajniej. W dłuższej perspektywie takie wnioski mogą pomóc inżynierom zaprojektować lepsze powłoki do oczyszczania powietrza, skuteczniejsze powierzchnie antybakteryjne oraz ulepszone materiały do produkcji paliw napędzanych światłem i rozszczepiania wody.
Cytowanie: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Słowa kluczowe: fotokataliza, dioxyd tytanu, ultraszybka spektroskopia, chemia powierzchni, utlenianie tlenku węgla