Clear Sky Science · pl
Opracowanie nanomodelu z czterokrotnym sprzężeniem kropek węglowych do celowanej terapii glejaka
Nowa nadzieja dla opornych guzów mózgu
Guz wysokiego stopnia, taki jak glejak wielopostaciowy, należy do najtrudniejszych nowotworów w leczeniu. Wiele leków skutecznych w innych częściach ciała albo nie przechodzi przez ochronną barierę krew–mózg, albo po drodze uszkadza zdrowe tkanki. W tym badaniu opisano laboratoryjnie zbudowaną „inteligentną” nanocząstkę, która ma trafiać do guzów mózgu z większą precyzją, przenosić silny koktajl leków i uwalniać go bezpośrednio w jądrach komórek nowotworowych — tam, gdzie może wyrządzić raka najwięcej szkody, oszczędzając przy tym komórki zdrowe.
Mały pojazd dostawczy zbudowany z węgla
Rdzeń nowego podejścia stanowią kropki węglowe — cząstki w nanometrowej skali wykonane z węgla, tanie w produkcji, dobrze mieszające się z wodą i wykazujące fotoluminescencję pod określonym światłem. Ponieważ ich powierzchnia jest bogata w chemiczne „haczyk”, można jednocześnie przyłączać do nich liczne składniki biologiczne. W tej pracy badacze stworzyli nanomodel „czterokrotnie sprzężony”: każda kropka węglowa została chemicznie połączona, w jednym etapie reakcji, z dwoma różnymi peptydami celującymi i dwoma ładunkami przeciwnowotworowymi. Ta modułowa konstrukcja zamienia każdą kropkę w mały pojazd dostawczy, który potrafi rozpoznawać komórki nowotworowe, przenikać przez bariery komórkowe i dostarczać leki pod właściwy wewnątrzkomórkowy adres.
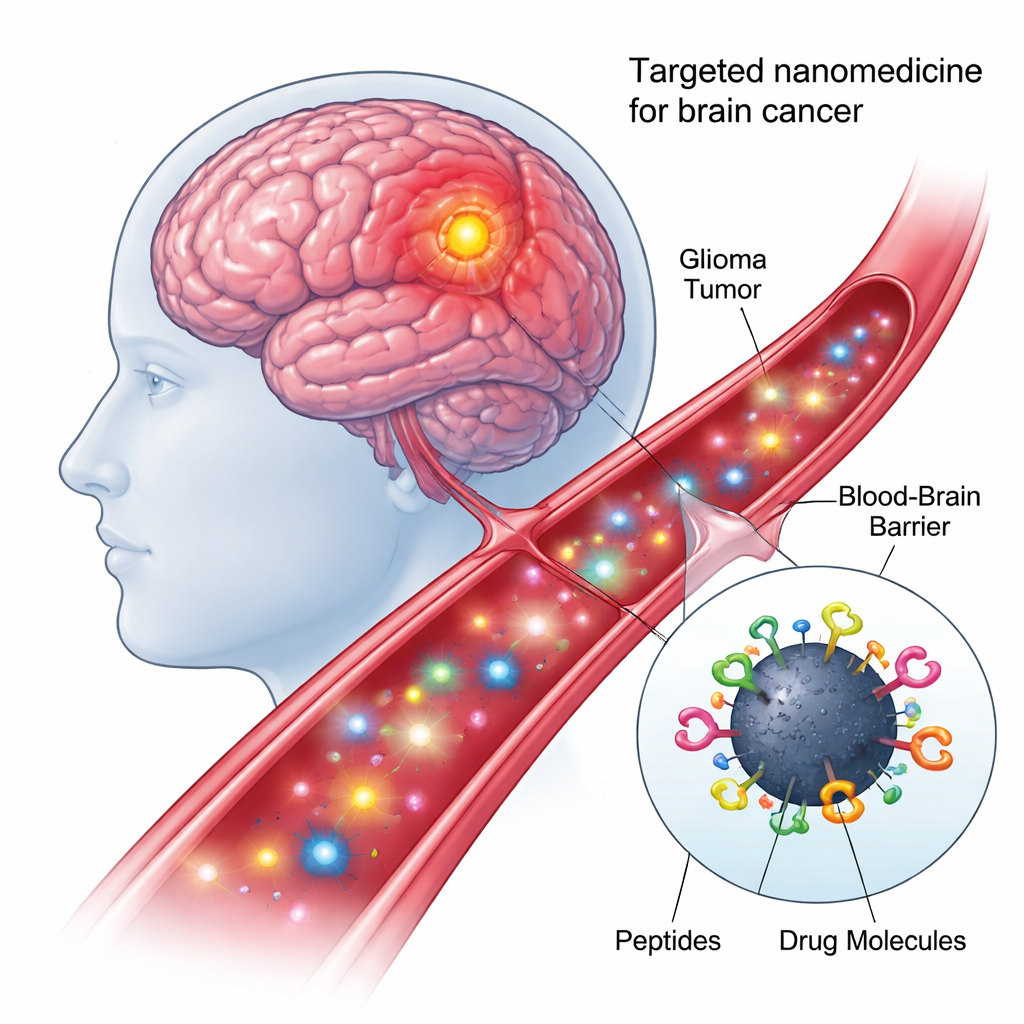
Odnajdywanie i wchodzenie do właściwych komórek mózgu
Pierwszy peptyd na nanocząstce, nazwany shPep-1, zaprojektowano tak, by rozpoznawał receptor IL13Rα2. Receptor ten występuje na wysokim poziomie w wielu agresywnych guzach mózgu — w tym w glejakach dorosłych i dziecięcych oraz w rozlanym wewnątrzrdzeniowym glejaku pnia mózgu — a na komórkach normalnych mózgu występuje słabo. Poprzez wiązanie IL13Rα2, shPep-1 pomaga kropkom węglowym koncentrować się na komórkach nowotworowych i wchodzić do nich drogą endocytozy zależnej od receptora. Drugi, dłuższy peptyd, lnPep-1, zawiera sygnał lokalizacji jądrowej: krótką sekwencję ułatwiającą przejście ładunku przez błonę jądrową i dotarcie do centrum kontrolnego komórki, gdzie przechowywane jest DNA. Razem te dwa peptydy nadają nanocząstce zarówno swoistość wobec guza, jak i zdolność dotarcia do jądra po wejściu do komórki.
Dostarczanie skoordynowanego ataku lekowego
Terapeutyczny ładunek składa się z dwóch małych cząsteczek. Pierwsza to epirubicyna, znany lek chemioterapeutyczny, który zabija komórki nowotworowe, wczepiając się w DNA i blokując enzymy potrzebne do naprawy pęknięć dwuniciowych. Druga to metabolit zwany 5-aminoimidazol-4-karboksamidem (AIC), powstający z leku przeciwguzowego temozolomidu w pH fizjologicznym. W wcześniejszych pracach ta sama grupa wykazała, że skojarzenie epirubicyny i AIC na kropce węglowej zwiększało zabijanie komórek nowotworowych w porównaniu z każdym z leków osobno. W nowym projekcie obie substancje są współdostarczane na nanocząstce z dwoma peptydami, z zamiarem uzyskania efektu synergicznego bezpośrednio w jądrze komórki nowotworowej.
Silne działanie w komórkach guza, łagodniejsze wobec komórek zdrowych
Aby sprawdzić skuteczność nanomodelu, zespół wystawił kilka linii komórkowych wysokiego stopnia glejaka — glejaka dorosłych, glejaka dziecięcego i model rozlanego glejaka pnia mózgu — na działanie czterokrotnie sprzężonych kropek węglowych. Nawet przy bardzo niskich stężeniach (już od 50 nanomoli) żywotność komórek nowotworowych spadła do około połowy w porównaniu z nieleczonymi kontrolami, a przy wyższych dawkach wszystkie testowane koniugaty zabiły większość komórek guza. Co ważne, nanomodel czterokrotnie sprzężony przewyższał prostsze wersje „z jednym peptydem”, mimo że zawierał ogólnie mniej epirubicyny. Testy na niekancerogennych komórkach mięśni gładkich naczyń wykazały znacznie niższą toksyczność: te komórki wymagały około 25–40 razy większej ilości nanocząstek, aby zaobserwować podobny spadek żywotności, co sugeruje użyteczne okno bezpieczeństwa wynikające z celowania w guz zamiast jedynie wysokiego dawkowania.
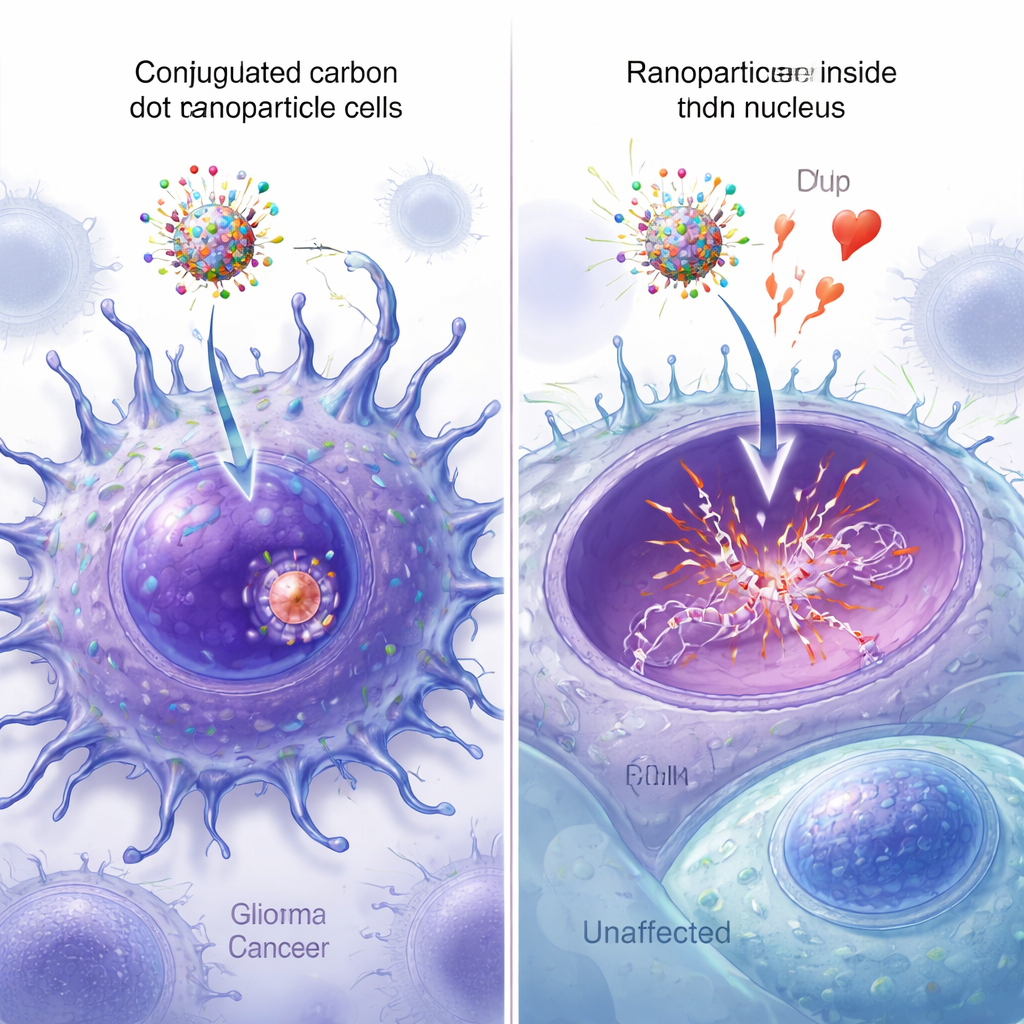
Widoczne dotarcie nanocząstek do jądra
Fluorescencyjne wersje nanocząstek pozwoliły badaczom obserwować, jak dobrze każdy projekt wchodzi do komórek i dociera do jądra. Pod mikroskopem kropki węglowe wyposażone w oba peptydy wykazywały najsilniejszy sygnał rozciągający się po całych komórkach nowotworowych, z wyraźnym nakładaniem się zielonej fluorescencji nanocząstek i niebieskiego barwienia jądra. Ilościowa analiza obrazów potwierdziła, że cząstki z dwoma peptydami miały najwyższą kolokalizację jądrową, znacząco przewyższającą cząstki niosące tylko jeden peptyd lub żaden. Dodatkowe pomiary spektroskopowe, spektrometrii mas i mikroskopii sił atomowych potwierdziły, że wszystkie cztery składniki zostały pomyślnie przyłączone do kropek węglowych i nieznacznie zwiększyły ich rozmiar, nie zakłócając przy tym kluczowej zdolności epirubicyny do wiązania DNA.
Co to może oznaczać dla przyszłej opieki nad nowotworami mózgu
Dla pacjentów te wyniki to wciąż wczesny, in vitro pokaz koncepcji, a nie gotowa terapia. Pokazują jednak obiecujący pomysł: niewielką, stabilną i stosunkowo łatwą do wytworzenia nanocząstkę węglową, którą można szybko modyfikować peptydami celującymi i kombinacjami leków. Dzięki kierowaniu leków konkretnie do komórek guza nadprodukujących IL13Rα2 i koncentracji ich w jądrze, takie nanomedycyny mogłyby pewnego dnia umożliwić stosowanie niższych dawek, mniejszą liczbę działań niepożądanych oraz bardziej spersonalizowane strategie leczenia wysoce śmiertelnych nowotworów mózgu, takich jak glejak wielopostaciowy i rozlany glejak pnia mózgu.
Cytowanie: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Słowa kluczowe: glejak wielopostaciowy, nanomedycyna, kropki węglowe, celowane dostarczanie leków, nowotwory mózgu