Clear Sky Science · pl
Kontrolowany wzrost sferulitycznych kryształów z mieszanin soli
Dlaczego kryształy soli mogą wyglądać jak kwiaty
Większość z nas wyobraża sobie kryształy jako ostre, fasetowane kształty, ale w przyrodzie często rosną one w spektakularne sfery przypominające kwiaty lub śnieżne kulki. Te „sferulity” pojawiają się w skałach wulkanicznych, kamieniach nerkowych, a nawet w niektórych chorobach związanych z nieprawidłowo sfałdowanymi białkami. Artykuł omawia, jak powszechny minerał, siarczan sodu — ta sama sól występująca w detergentach i niektórych materiałach budowlanych — może tworzyć tak misternie ukształtowane sferyczne kryształy oraz co to mówi o tym, jak z prostych składników samoorganizują się złożone struktury.
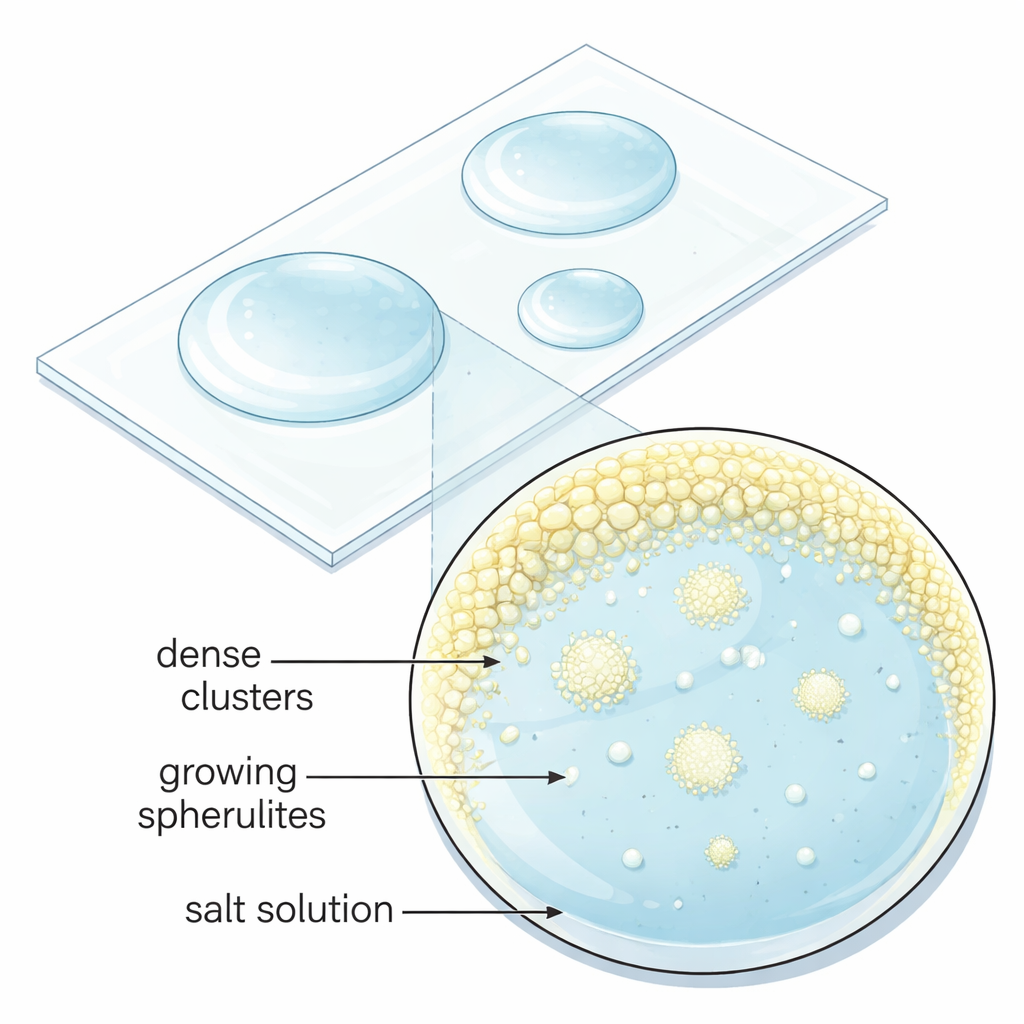
Od prostych soli do rzeźbionych sfer
Naukowcy postanowili zrozumieć, kiedy i w jaki sposób siarczan sodu rośnie jako sferulity zamiast zwykłych, kanciastych kryształów. Przygotowali maleńkie krople wody z mieszaninami siarczanu sodu i innych siarczanów, których jony metali niosą dwa ładunki dodatnie, takich jak magnez czy żelazo. Gdy te pikolitr- do mikrolitrowe krople powoli odparowywały na szklanych szalkach w temperaturze pokojowej, rozpuszczone sole stawały się coraz bardziej skoncentrowane, aż zaczynały formować się kryształy. Systematycznie zmieniając stosunek mieszaniny, znaleźli określone „słodkie punkty” składu, w których siarczan sodu konsekwentnie tworzył sferyczne, promieniście teksturowane kryształy. Poza tymi zakresami ta sama ciecz dawała albo regularne, fasetowane ziarna, albo bezpostaciowy, żelowaty stały produkt, co pokazuje, że powstawanie sfer wymaga precyzyjnie dostrojonych warunków.
Maleńkie ciekłe kieszonki, które zapładniają sfery krystaliczne
Pod mikroskopem zespół zaobserwował, że sferulity nie pojawiały się bezpośrednio z przejrzystego roztworu. Zamiast tego parowanie najpierw tworzyło małe, gęste skupiska ciekłe wzbogacone w rozpuszczone jony w pobliżu krawędzi kropli. Te mikronowe kieszonki trwały przez minuty, zanim nagle wyrósł z nich równocześnie duży zbiór sferulitów. Obrazy o wysokiej rozdzielczości z mikroskopu elektronowego suchych struktur ujawniły, że każda sferulita zbudowana jest z niezliczonych nanometrowych kryształków siarczanu sodu skierowanych mniej więcej na zewnątrz, które później się zespalają. To zachowanie stoi w sprzeczności z podręcznikowym obrazem wzrostu kryształów, w którym pojedyncze stabilne ziarno rośnie gładko, i zamiast tego wskazuje na wieloetapową, „nieklasyczną” ścieżkę, w której gęste kropelki i nanocząstki montują się i reorganizują w drodze do ostatecznego stałego kształtu.
Kiedy słona woda robi się jak masło orzechowe
Kluczowym elementem tej historii jest to, jak gęsty, czyli lepki, staje się roztwór w miarę utraty wody. Śledząc szybkość, z jaką sferulity się rozszerzały, i bezpośrednio mierząc właściwości płynięcia pokrewnych roztworów soli, autorzy wykazali, że mieszaniny sodowo–magnezowe lub sodowo–żelazowe stają się niezwykle lepkie — do około 100 razy gęstsze niż miód — dokładnie w momencie, gdy zaczynają się tworzyć sferulity. Ta niemal „masłowo-orzechowa” konsystencja spowalnia ruch jonów tak bardzo, że dyfuzja, a nie chemia powierzchni, ogranicza szybkość wzrostu kryształów. W tym ospałym środowisku powstaje niezliczona liczba małych skupisk i nanokrystalików, które mają czas, by złączyć się w sferyczne agregaty zamiast rosnąć w kilka dużych, dobrze ukształtowanych kryształów. Kationy dwuwartościowe odgrywają tu kluczową rolę: silnie wiążą wodę i łączą się w krótkie łańcuchy lub sieci, co zarówno zwiększa lepkość, jak i pomaga wytworzyć amorficzne, żelopodobne otoczenie wokół rosnących sferulitów.
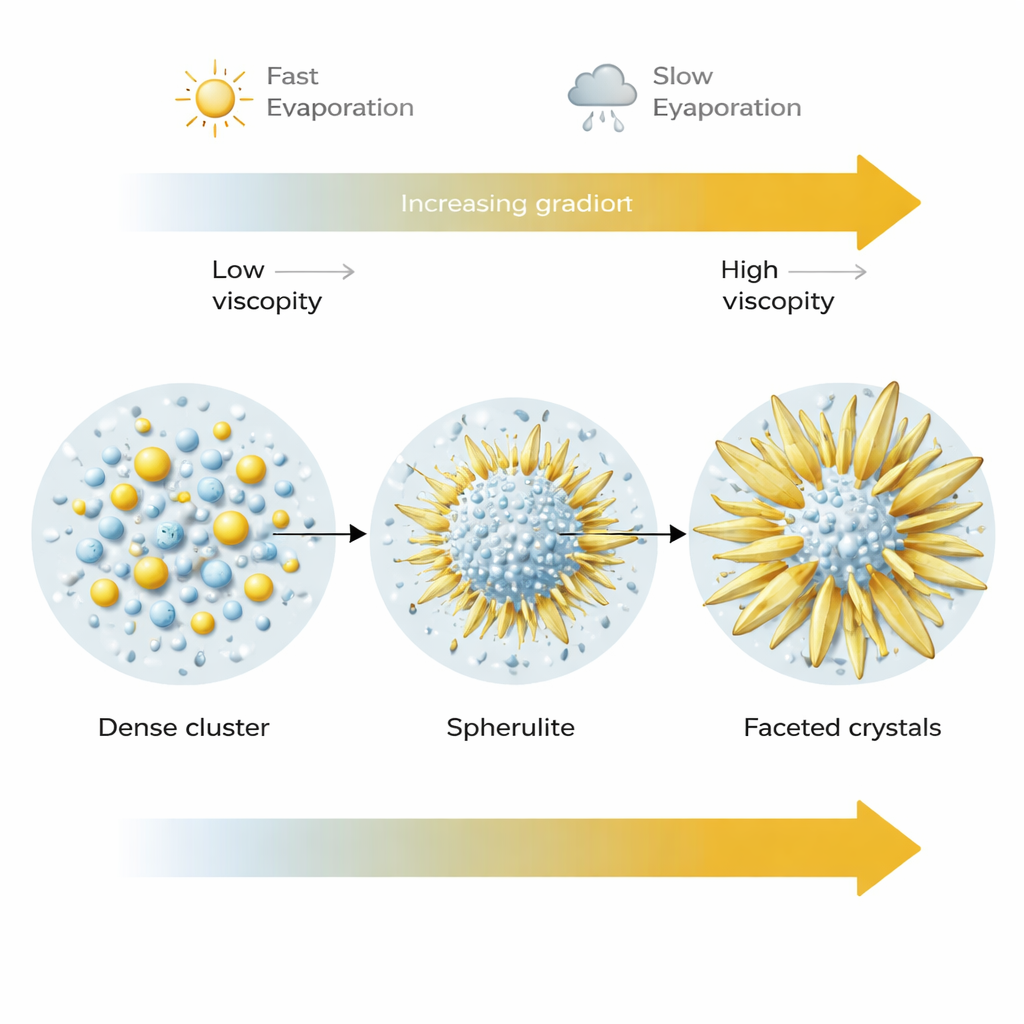
Jak prędkość wysychania przekształca ostateczne kryształy
Szybkość parowania okazała się kolejnym potężnym pokrętłem sterującym. Przy szybszym wysychaniu (niższej wilgotności) zainicjowało się wiele sferulitów, ale pozostały one stosunkowo małe, zablokowane w swojej metastabilnej sferycznej postaci, gdy otaczający płyn szybko zgęstniał. Przy wolniejszym wysychaniu (wyższej wilgotności) te same początkowe kule miały więcej czasu i dostęp do rozpuszczonych jonów. Ich drobne cegiełki mogły się przearanżować i połączyć w większe, gładsze i bardziej fasetowane kryształy, często wyrastające w ostrza przypominające łopatki, które ostatecznie przechodziły w termodynamicznie stabilną formę siarczanu sodu. Innymi słowy, struktury sferyczne działają jako etap przejściowy w podróży wzrostu, która może zakończyć się bardzo różnymi kształtami, w zależności od tego, jak szybko roztwór wysycha i jak łatwo materiał w nim jeszcze się przemieszcza.
Dlaczego to ma znaczenie poza ładnymi kryształami
Mówiąc prosto, badanie pokazuje, że piękne, kwiatopodobne kule soli powstają, gdy skoncentrowane mieszaniny prostych soli stają się na tyle gęste, że wszystko się spowalnia, ale nie tak gęste, by wzrost całkowicie ustawał. W tych „właśnie właściwych” warunkach gęste ciekłe kieszonki i roje małych kryształków samoorganizują się w sferyczne skupiska, które później mogą ewoluować w bardziej stabilne, fasetowane ziarna. Zrozumienie i kontrola tej delikatnej równowagi między składem, lepkością i parowaniem otwiera drogę do projektowania niestandardowych tekstur kryształów dla zastosowań od mocniejszych materiałów budowlanych i ulepszonych farmaceutyków po lepsze modele formowania kryształów geologicznych i biologicznych.
Cytowanie: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Słowa kluczowe: sferulity, siarczan sodu, wzrost kryształów, nukleacja nieklasyczna, roztwory soli