Clear Sky Science · pl
Pierwsza struktura krystaliczna adduktu powstałego w reakcji związku wanadu z ludzką transferyną surowicy
Dlaczego białko krwi i metaliczny lek mają znaczenie
Wiele eksperymentalnych leków zawiera atomy metali, które mogą pomagać w leczeniu chorób od cukrzycy po nowotwory. Gdy te leki oparte na metalach trafiają do krwiobiegu, muszą jednak wsiąść do „transportu” na naturalnych białkach przenoszących organizmu. W tym badaniu przyjrzano się, jak jedno z takich białek — ludzka transferyna surowicy, główny nośnik żelaza we krwi — oddziałuje z obiecującym związkiem wanadu, rzucając światło na to, jak leki metaliczne są przewożone po organizmie i jak można je dopracować, by były bezpieczniejsze i skuteczniejsze.
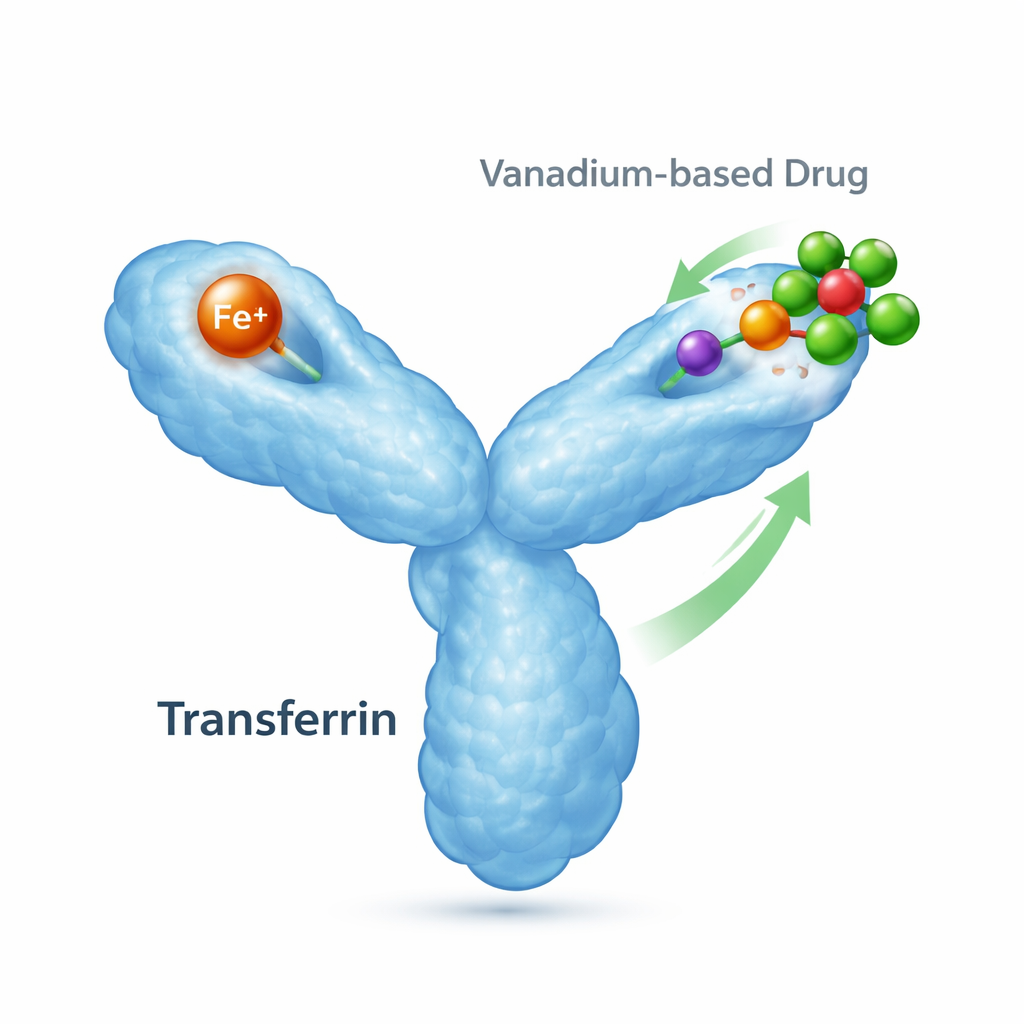
Kurier żelaza w organizmie i jego dodatkowe role
Transferyna to białko o masie ~80 kDa, którego podstawową funkcją jest chwytać żelazo i dostarczać je do komórek, które go potrzebują. Ma dwie „płatowe” domeny, z których każda może związać jeden jon żelaza, i zmienia kształt w zależności od obecności żelaza. Gdy żelazo wiąże się, domena zamyka się; bez żelaza pozostaje otwarta. Specjalne receptory na powierzchni komórek rozpoznają te załadowane żelazem formy i internalizują je, co sprawia, że transferyna jest kluczowa dla równowagi żelaza i zdrowia komórek. Jednak transferyna może też wiązać inne metale, w tym pochodzące z terapii, co oznacza, że może wpływać na to, dokąd przemieszczają się leki metaliczne i jak działają.
Snapshot kształtu wanadu na transferynie
Naukowcy skupili się na dobrze zbadanym kandydacie na lek z wanadem, nazwanym bis(acetylacetonato)oksowanadem(IV), zapisywanym często jako [VIVO(acac)₂]. Wcześniejsze prace wskazywały, że związek ten, lub powstające z niego w wodzie gatunki, mogą przyłączać się do transferyny, ale nikt nie widział tego dokładnie. Korzystając z krystalografii rentgenowskiej, zespół uzyskał struktury transferyny o wysokiej rozdzielczości, zawierającej żelazo tylko w C‑terminalnej domenie (forma „FeC”), zarówno przed, jak i po ekspozycji na związek wanadu. W kryształach traktowanych wanadem nie zaobserwowano oryginalnego leku, lecz przekształcony klaster tlenowo‑wanadowy związany w żelazowym, pustym N‑płatku. Dało to pierwsze bezpośrednie strukturalne wyobrażenie fragmentu wanadu przyłączonego do ludzkiej transferyny.
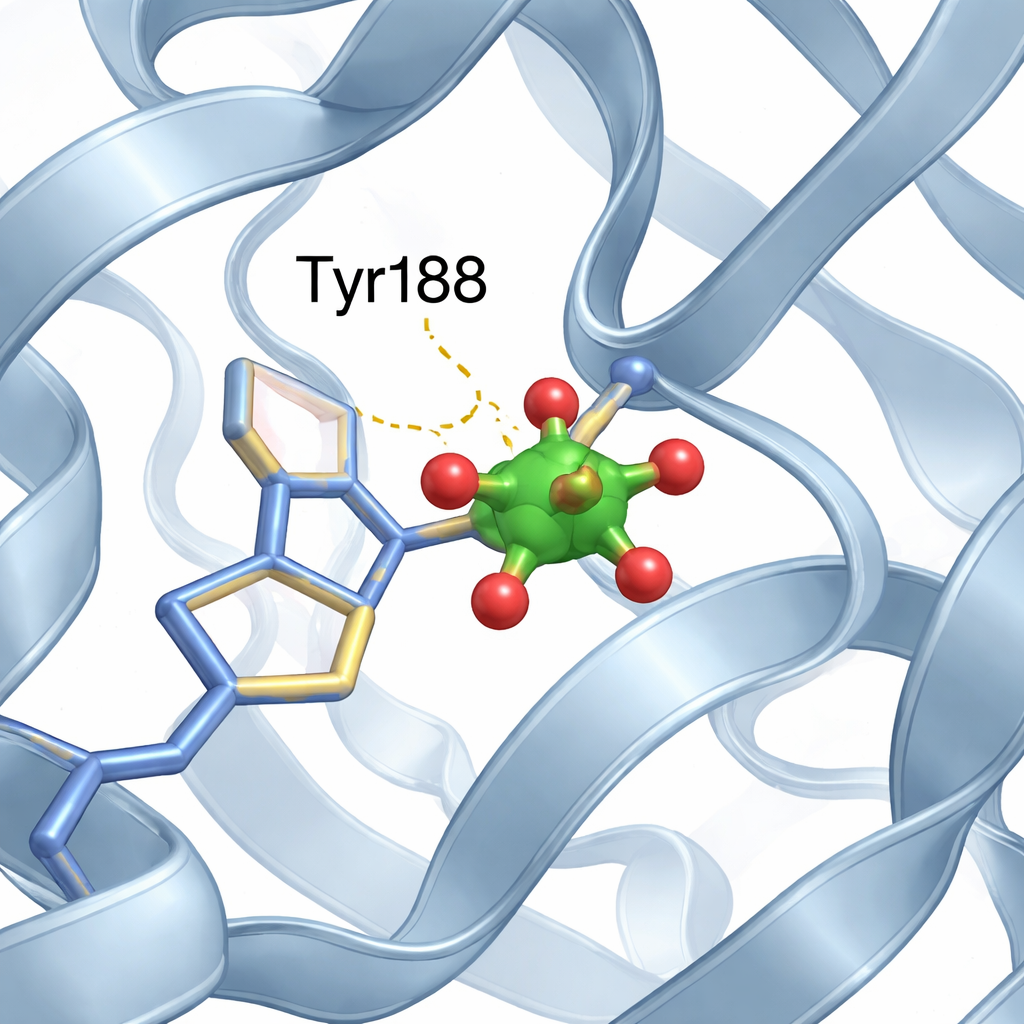
Mały klaster wanadu znajduje swoje miejsce
W miejscu wiązania żelaza w N‑płatku zespół zidentyfikował niewielki klaster złożony z dwóch atomów wanadu i atomów tlenu, najlepiej opisany jako zmodyfikowana jednostka „divanadanu”. Jedno z miejsc tlenowych klastra zajmuje tlen z określonego aminokwasu — tyrozyny 188 (Tyr188), tworząc bezpośrednie wiązanie między białkiem a klastrem metalu. Dodatkowe łagodne interakcje, takie jak wiązania wodorowe od pobliskich fragmentów białka, dodatkowo stabilizują klaster na miejscu. Co ważne, pomimo obecności tego nowego metalicznego gościa w kieszeni wiążącej żelazo, całe białko zachowuje zwykłe ustawienie z otwartym N‑płatkiem i zamkniętym C‑płatkiem, niemal identyczne z strukturą wolną od wanadu.
W jaki sposób transferyna przekształca chemię wanadu
W roztworze przy pH i stężeniu użytym do krystalizacji, dwuwanadowy gatunek widziany w krysztale jest zazwyczaj tylko małym udziałowcem; dominują większe klastry tlenowo‑wanadowe. Pomiar spektroskopowy i teoretyczne obliczenia specjacji sugerują, że pierwotny związek wanadu powoli ulega utlenieniu i rozpadowi w wodzie, tworząc proste jony wanadanu, które następnie składają się w różne klastry. Struktura krystaliczna wskazuje, że transferyna wybiórczo stabilizuje ten mały, przypominający divanadan fragment ponad większymi klastrami, zasadniczo „wybierając” jedną formę chemiczną z roztworowej mieszaniny poprzez zapewnienie dopasowanego miejsca wiążącego przy Tyr188 i wspierającej sieci wiązań wodorowych.
Utrzymanie uścisku z receptorem komórkowym
Ponieważ transferyna musi wiązać receptor na powierzchniach komórek, aby dostarczyć żelazo, badacze sprawdzili, czy przyłączenie tego klastra wanadu zakłóci ten kluczowy „uścisk dłoni”. Z użyciem nie-denaturującej elektroforezy żelowej i czułej techniki zwanej interferometrią warstwową (biolayer interferometry) zmierzyli, jak dobrze transferyna traktowana wanadem wiąże receptor transferynowy w porównaniu z nieleczoną formą zawierającą tylko żelazo. Obie zachowywały się niemal identycznie, wykazując bardzo silne wiązanie w zakresie niskich nanomolarów. Potwierdza to, że klaster wanadowy, choć umieszczony w N‑płatku, nie zmienia istotnie kształtu transferyny w rejonie interakcji z receptorem i w związku z tym nie powinien uniemożliwiać rozpoznania białka przez komórki.
Co to oznacza dla leków opartych na metalach
Dla osób niebędących specjalistami wniosek jest taki, że badanie dostarcza molekularnego obrazu tego, jak pochodna leku z wanadem przyłącza się do głównego nośnika żelaza organizmu, nie zaburzając jego normalnej funkcji. Transferyna może wychwycić specyficzny, mały klaster tlenowo‑wanadowy w kieszeni żelazowej, a mimo to ogólny kształt białka i jego zdolność do wiązania receptora pozostają praktycznie niezmienione. Pomaga to wyjaśnić, jak leki wanadowe mogą krążyć związane z transferyną i podkreśla, że różne białka mogą preferować różne rozmiary klastrów wanadowych. Takie spostrzeżenia są kluczowe przy projektowaniu inteligentniejszych terapii opartych na metalach, których zachowanie w krwiobiegu — jakie formy przyjmują, dokąd trafiają i jak długo tam pozostają — można przewidzieć i kontrolować.
Cytowanie: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Słowa kluczowe: leki wanadowe, ludzka transferyna surowicy, terapie oparte na metalach, wiązanie białko–metal, biologia strukturalna