Clear Sky Science · pl
Laktam umożliwia zdalne przemieszczenia boronianów do wiązań C═N
Nowy skrót do budowy molekuł przypominających leki
Chemicy nieustannie poszukują szybszych, czyściejszych sposobów na konstruowanie złożonych cząsteczek występujących w lekach i zaawansowanych materiałach. To badanie przedstawia sprytny skrót, który pozwala powszechnemu, pierścieniowemu układowi zwanemu laktamem tymczasowo kierować przebiegiem reakcji, a potem dyskretnie ustąpić—umożliwiając przekształcenie prostych, łatwo dostępnych składników w wartościowe cegiełki farmaceutyczne bez użycia drogich metali czy skomplikowanych etapów przygotowawczych.
Przekształcenie cichego pomocnika w tymczasowy przewodnik
Wiele współczesnych leków i funkcjonalnych materiałów opiera się na reakcjach kwasów boronowych, rodziny związków zawierających bor cenionych za niezawodność i łagodne warunki reakcji. Tradycyjnie, aby skłonić kwasy boronowe do tworzenia nowych wiązań z wiązaniami podwójnymi węgiel–azot (C=N), chemicy muszą wcześniej wprowadzić specjalne „grupy kierujące” na substratach. Grupy te działają jak uchwyty sterujące reakcją, ale kosztują dodatkowy czas, pieniądze i etapy—i często działają tylko z bardzo reaktywnymi partnerami. Autorzy zauważyli, że laktamy, pierścieniowe odpowiedniki dobrze znanego wiązania amidowego obecnego w białkach, mogą pełnić rolę wbudowanych, tymczasowych przewodników. Poprzez koordynację z atomem boru, tlen laktamu pomaga uformować wysoko zorganizowany, czterozłącznikowy ośrodek boru, który może przemieścić przyłączony fragment na odległe miejsce w cząsteczce, przygotowując nowe wiązania C–N bez żadnej trwałej grupy kierującej.
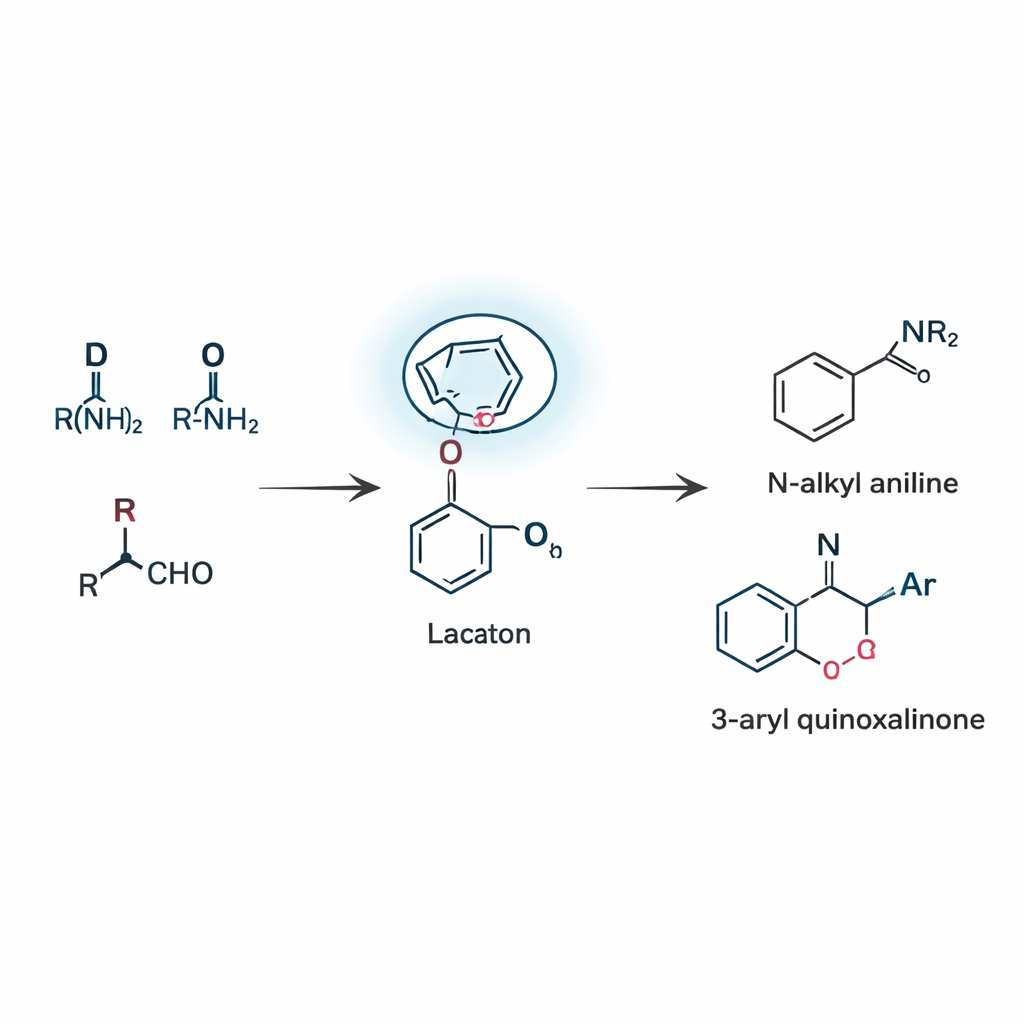
Budowa dwóch rodzin użytecznych produktów jedną strategią
Wykorzystując tę koncepcję, zespół opracował dwie powiązane reakcje, które obie polegają na tej laktamowo prowadzonej rekonfiguracji, znanej jako zdalne przemieszczenie boronianowe. W pierwszym wariancie trzy proste elementy—aldehyd, amin i kwas boronowy—łącza się, tworząc N‑alkilowane aniliny, motyw podstawowy występujący w niezliczonych kandydatach na leki i barwnikach. Reakcja przebiega przez rzadki przesuw 1,5, w którym grupa arylowa na borze przeskakuje przez pięć atomów, aby dotrzeć do wiązania C=N. Poprzez staranne dobranie katalizatora, rozpuszczalnika i temperatury, badacze uzyskali przyzwoite wydajności i wykazali, że tolerowane są różne podstawienia, w tym halogeny, grupy alkilowe i heterocykle. W drugim trybie reakcji ta sama idea przewodnia jest zastosowana do chinoksalinonów, klasy pierścieni bogatych w azot powszechnych w chemii medycznej. Tutaj reakcja nie wymaga dodatku metalu jako katalizatora i mimo to dostarcza 3‑arylowe chinoksalinony wydajnie, dzięki zdolności laktamu do współdziałania z borem i stabilizacji kluczowego pośrednika.
Warunki przyjazne środowisku i późne edytowanie leków
Poza wykazaniem szerokiego zakresu, autorzy pokazują, że strategia jest praktyczna dla rzeczywistych cząsteczek. Ponieważ przemieszczenie 1,4 w przypadku chinoksalinonów przebiega w warunkach bezmetaliowych w specjalnym alkoholu, unika potrzeby użycia drogich lub toksycznych metali przejściowych. Zespół zastosował metodę do złożonych fragmentów pochodzących z dopuszczonych do obrotu leków, takich jak ibuprofen, oraz innych związków terapeutycznych zawierających szkielet chinoksalinonu. W każdym przypadku reakcja wprowadzała nowe grupy arylowe w określone miejsce, nie naruszając jednocześnie innych wrażliwych funkcji. Tego rodzaju „późna funkcjonalizacja” pozwala chemikom szybko dekorować istniejące rdzenie lekowe nowymi łańcuchami bocznymi, przyspieszając poszukiwanie poprawy mocy, bezpieczeństwa lub właściwości fizycznych.
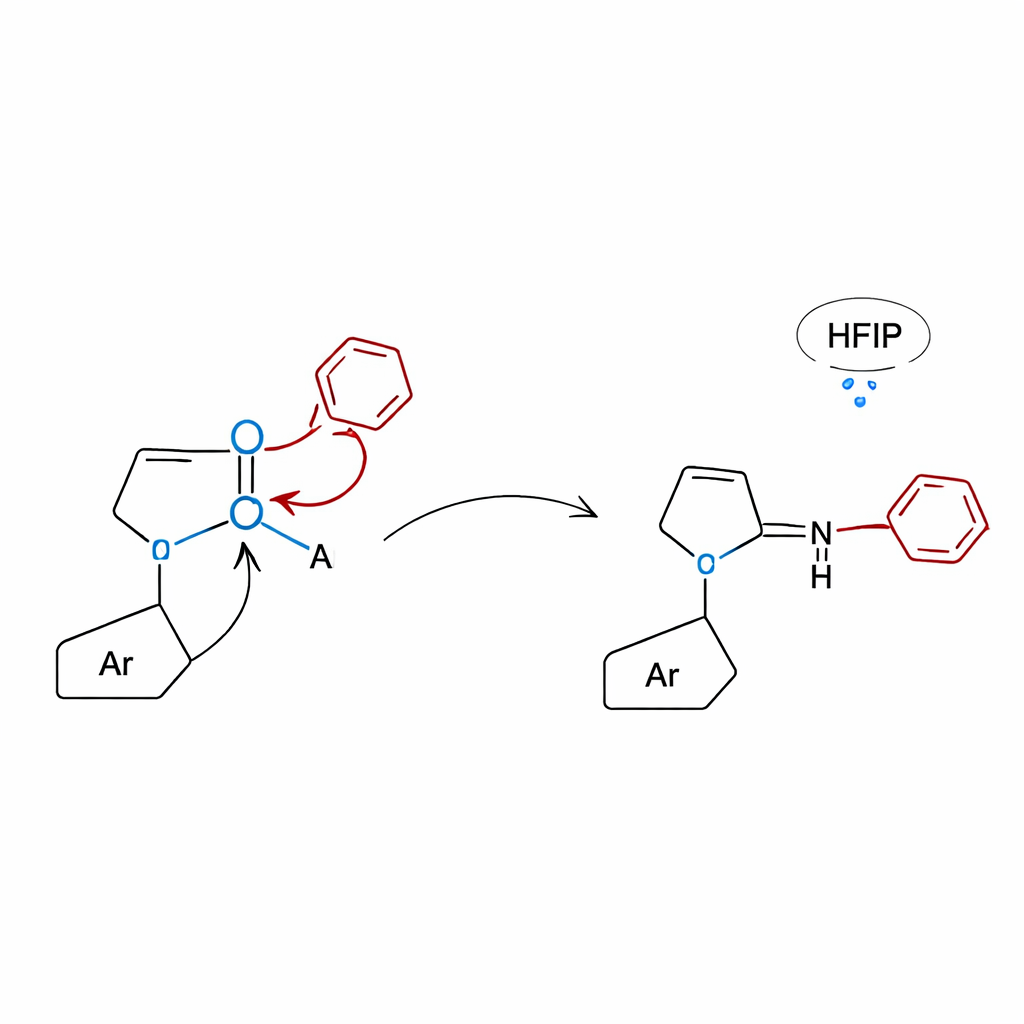
Zajrzeć pod maskę dzięki teorii i testom kontrolnym
Aby zrozumieć, dlaczego podejście z laktamem działa tak dobrze, badacze połączyli starannie zaprojektowane eksperymenty kontrolne z symulacjami komputerowymi. Gdy testowano cząsteczki pozbawione fragmentu laktamowego, reakcje praktycznie ustawały, co potwierdziło, że pierścień laktamu jest niezbędny do aktywacji kwasu boronowego i nakierowania przemieszczenia. Obliczenia chemii kwantowej wykazały, że tlen laktamu wiąże się z borem, tworząc zwarty, czterozłącznikowy układ, z którego grupa arylowa może migrować albo przez pięć atomów (przesuw 1,5), dając N‑alkilowane aniliny, albo przez cztery atomy (przesuw 1,4), dając 3‑arylowe chinoksalinony. W przypadku chinoksalinonów sieć wiązań wodorowych zapewniana przez rozpuszczalnik HFIP dodatkowo obniża barierę energetyczną, pomagając reakcji przebiegać w stosunkowo łagodnych warunkach termicznych bez dodatku jakiegokolwiek katalizatora.
Dlaczego to ma znaczenie dla przyszłych leków
Podsumowując, praca pokazuje, że prosty pierścień laktamowy może działać jako dynamiczny, możliwy do recyclingu przewodnik, który odblokowuje wcześniej niedostępne wzorce tworzenia wiązań w chemii kwasów boronowych. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że chemicy zyskują teraz bardziej bezpośredni, wydajny sposób przekształcania podstawowych cegiełek w dwie ważne klasy związków zawierających azot, które stanowią podstawę wielu leków. Ponieważ metoda unika cennych metali, toleruje szerokie spektrum grup funkcyjnych i sprawdza się w zaawansowanych strukturach przypominających leki, może uprościć projektowanie i optymalizację przyszłych farmaceutyków, a potencjalnie także nowych środków ochrony roślin.
Cytowanie: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Słowa kluczowe: kwasy boronowe, chemia laktamów, formowanie wiązań C–N, chinoksaliny, chemia medyczna