Clear Sky Science · pl
Wykrywanie enzymów na podstawie ortologii w celu urozmaicenia szkieletu przeciwnowotworowego evodiaminy
Przekształcanie związków roślinnych w lepsze leki
Wiele współczesnych leków zaczynało życie jako ochronne związki chemiczne w roślinach. Te naturalne molekuły często wykazują silne działanie przeciw nowotworom, infekcjom czy bólowi, lecz rzadko są „idealnymi” lekami. Chemicy chcieliby precyzyjnie modyfikować ich struktury, by uczynić je bezpieczniejszymi i skuteczniejszymi, jednak te cząsteczki bywają tak złożone, że nawet drobne zmiany są trudne. W tym badaniu pokazano, jak naukowcy mogą wykorzystać enzymy roślinne jako małe narzędzia molekularne do dokonywania ukierunkowanych zmian w związku przeciwnowotworowym zwanym evodiaminą, co może otworzyć nowe drogi do lepszych terapii.
Dlaczego ta roślinna molekuła ma znaczenie
Evodiamina to naturalny związek występujący w owocach drzewa wykorzystywanego w tradycyjnej medycynie chińskiej. Należy do rodziny pierścieniowych molekuł, które stanowią podstawę ważnych leków na raka, nadciśnienie i infekcje. Sama evodiamina wykazała działanie przeciwnowotworowe, przeciwzapalne, przeciwbólowe i przeciwdrobnoustrojowe, a niektóre jej zmodyfikowane wersje wydają się szczególnie obiecujące jako wielocelowe prowadzące związki przeciwnowotworowe. Problem polega na tym, jak przyłączyć nowe „uchwyty” chemiczne, na przykład grupy zawierające tlen, w bardzo konkretnych miejscach na tym zatłoczonym szkielecie, bez użycia agresywnych reagentów czy wielostopniowych syntez.
Pozwólmy enzymom wykonać trudną chemię
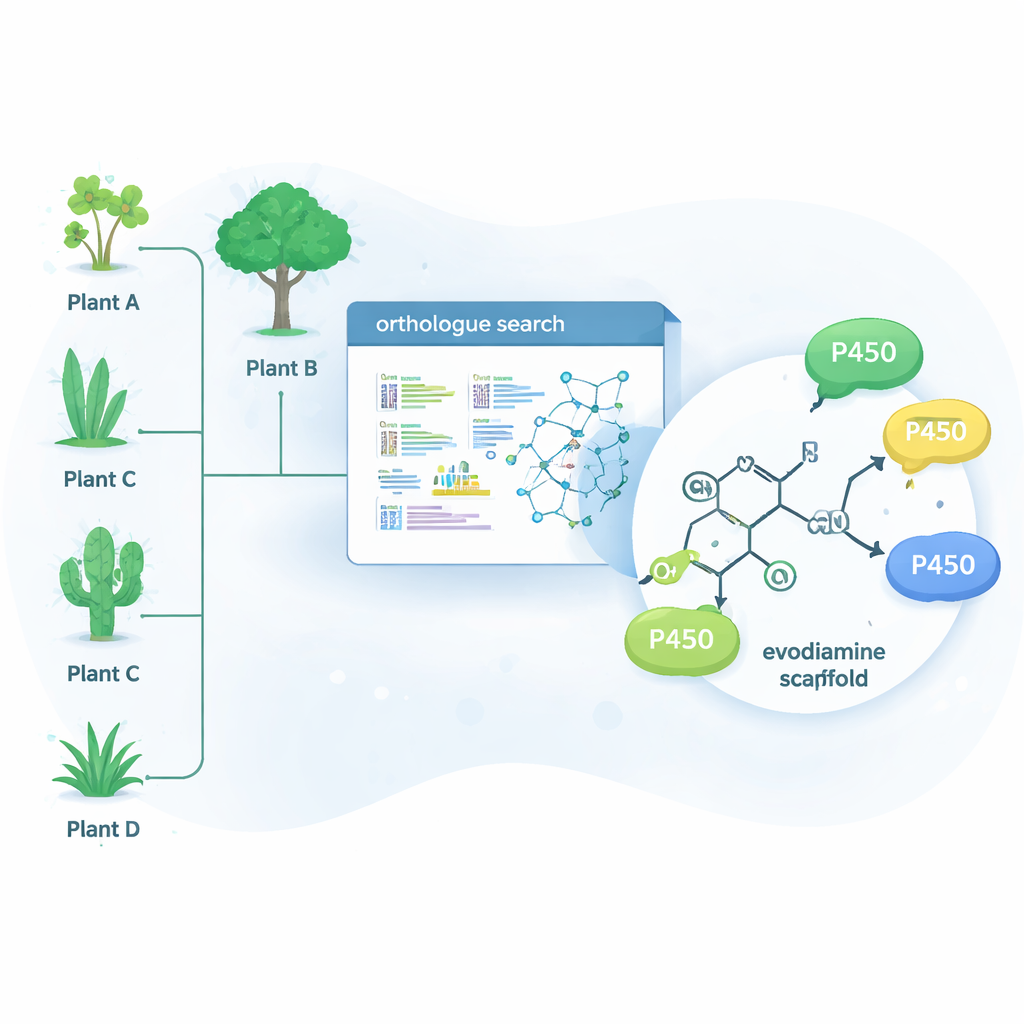
Przyroda rozwiązała już wiele takich trudnych problemów chemicznych za pomocą enzymów — białek katalizujących określone reakcje. Jedna duża rodzina enzymów, zwana cytochromami P450, szczególnie dobrze radzi sobie z wprowadzaniem tlenu do względnie nieaktywnego wiązania węgiel‑wodór. Ten pojedynczy krok może dramatycznie zmienić zachowanie cząsteczki w organizmie i może też stworzyć punkt wyjścia do dalszych modyfikacji chemicznych. Zamiast przeszukiwać tylko rośliny naturalnie produkujące evodiaminę, badacze użyli narzędzia bioinformatycznego OrthoFinder do przebadania danych genetycznych z 15 różnych roślin produkujących alkaloidy. Szukali enzymów P450 będących bliskimi „ortologami” znanych enzymów modyfikujących alkaloidy, zakładając, że krewni tych enzymów także mogą potrafić precyzyjnie dopracować pokrewne molekuły o właściwościach lekopodobnych.
Odkrywanie nowych enzymów w niespodziewanych roślinach
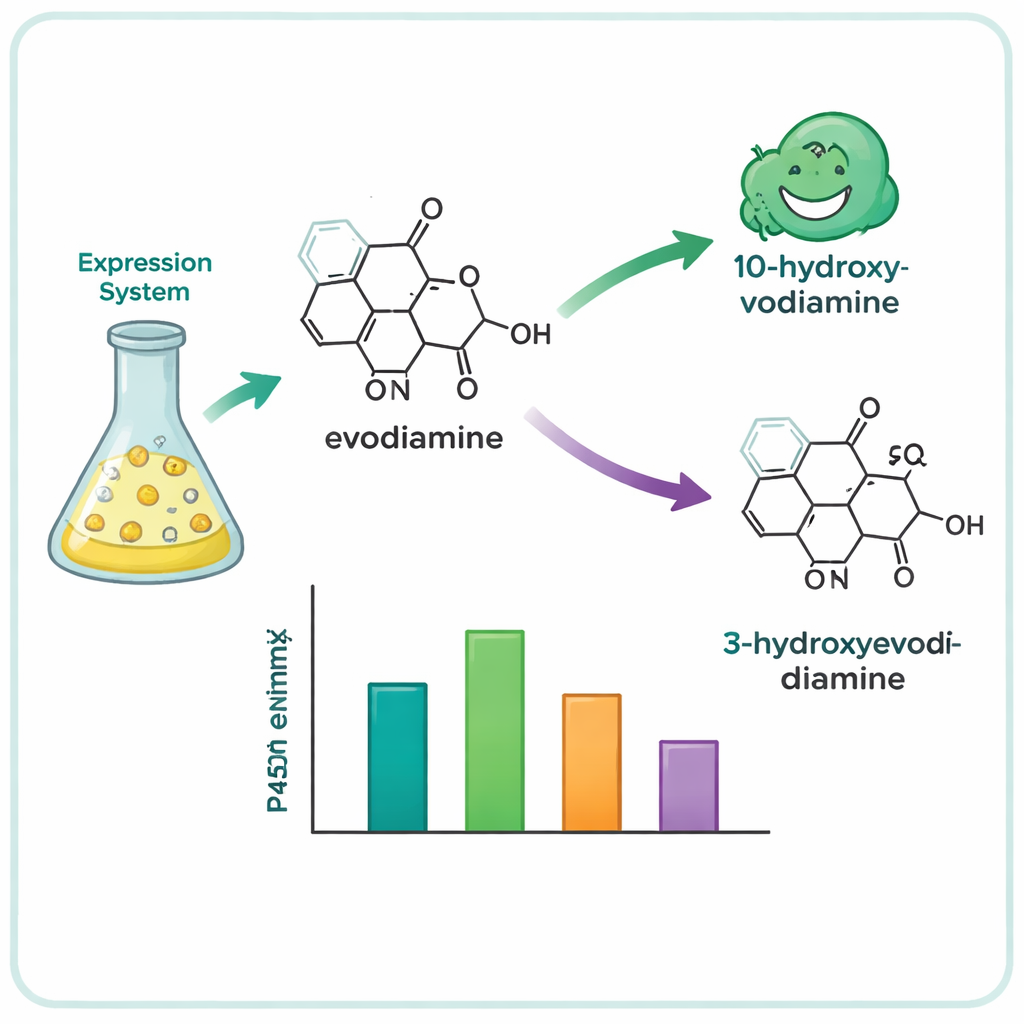
Z setek kandydatów zespół zawęził listę do 15 obiecujących P450 i wyraził je w komórkach drożdży, które posłużyły jako miniaturowe fabryki enzymów. Następnie podawano tym drożdżom kolekcję złożonych związków roślinnych i analizowano, które z nich uległy chemicznej przemianie. Cztery enzymy — trzy z drzewa Camptotheca acuminata i jeden z krzewu Tabernaemontana elegans — okazały się działać na evodiaminę, mimo że żadna z tych roślin nie jest znana z produkcji tego związku. Enzymy te selektywnie wprowadzały atom tlenu w jedno z dwóch miejsc w systemie pierścieni evodiaminy, generując dwa główne produkty: 10‑hydroksyevodiaminę i 3‑hydroksyevodiaminę. Takie utlenione wersje łatwiej poddać dalszym przekształceniom w związki rozpuszczalne w wodzie lub w silniejsze kandydaty na leki, wykorzystując łagodniejszą chemię niż tradycyjne drogi syntetyczne.
Zaglądając do zestawu narzędzi molekularnych
Aby zrozumieć, dlaczego te blisko spokrewnione enzymy zachowywały się inaczej, badacze zbudowali trójwymiarowe modele najbardziej aktywnego enzymu i jego krewniaków z użyciem nowoczesnych narzędzi do przewidywania struktur białkowych. Potem zastosowali dokowanie komputerowe, by zobaczyć, jak evodiamina może układać się w aktywnych kieszeniach enzymów, w pobliżu żelazowego centrum P450, gdzie zachodzi reakcja. Modele uwydatniły kilka dużych, odpychających wobec wody aminokwasów — szczególnie reszty fenyloalaniny — umieszczonych blisko aromatycznych pierścieni evodiaminy. Poprzez precyzyjne mutacje tych pozycji zespół pokazał, że zmiana rozmiaru i kształtu tej kieszeni może osłabić aktywność, zmienić dopasowanie substratu, a nawet przełączyć preferowane miejsce oksygenacji z jednego pierścienia cząsteczki na drugi. W jednym przypadku pojedyncza mutacja odwróciła preferencję enzymu z produkcji 10‑hydroksy na 3‑hydroksy.
Co to oznacza dla przyszłych leków
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że autorzy przedstawili praktyczną mapę drogową do odkrywania i strojeniia enzymów roślinnych, które mogą wykonać precyzyjne, „chirurgiczne” modyfikacje złożonych molekuł o właściwościach lekopodobnych. Łącząc szeroko zakrojone poszukiwania genetyczne z testowaniem enzymów i modelowaniem strukturalnym, odkryli zestaw biokatalizatorów, które selektywnie przeprojektowują szkielet evodiaminy w pozycjach trudnych do osiągnięcia standardową chemią. To nie tylko oferuje czystszy, bardziej zrównoważony sposób tworzenia zaawansowanych wersji evodiaminy — na przykład rozpuszczalnych w wodzie kandydatów przeciwnowotworowych — lecz także pokazuje, że użyteczne enzymy można znaleźć w roślinach, które same nigdy nie wytwarzają danego związku. Tę samą strategię można teraz zastosować do wielu innych naturalnych produktów, przyspieszając projektowanie kolejnej generacji leków pochodzenia roślinnego.
Cytowanie: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Słowa kluczowe: evodiamina, enzymy roślinne, cytochrom P450, biokataliza, poszukiwanie leków