Clear Sky Science · pl
Mutacja w zespole PACS1 zakłóca transport ładunków zależny od dyneiny przez HDAC6 i BICD2
Dlaczego to ma znaczenie dla rozwoju mózgu
Zespół PACS1 to rzadkie schorzenie genetyczne powodujące niepełnosprawność intelektualną, padaczkę i charakterystyczne rysy twarzy. Rodziny i klinicyści znają objawy, ale aż do niedawna nie było jasne, co dokładnie szwankuje wewnątrz komórek pacjentów. To badanie odsłania tę tajemnicę, pokazując, jak jednonukleotydowa zmiana w genie PACS1 rozregulowuje wewnętrzny system transportu komórkowego, zwłaszcza w neuronach, i jak to łączy zespół PACS1 z szerszą rodziną schorzeń „ruchu” w układzie nerwowym. 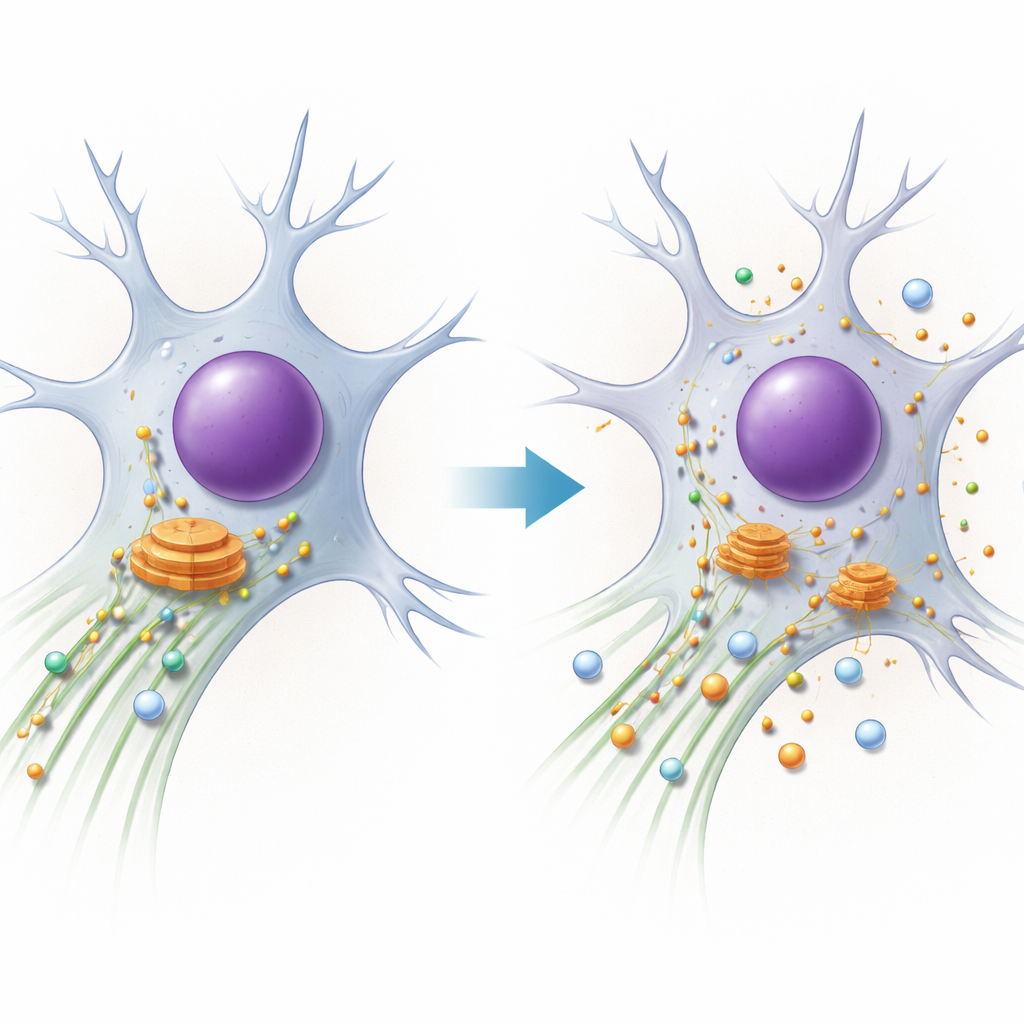
Autostrady dostawcze komórki
Każda komórka polega na mikroskopijnych „autostradach” zbudowanych z białkowych rur zwanych mikrotubulami. Molekularne silniki poruszają się po tych torach, transportując ładunki takie jak enzymy i pęcherzyki błonowe tam, gdzie są potrzebne. Jeden ze szlaków, dyneina, odpowiada za długodystansowe „trasy powrotne”, ściągając ładunki z peryferii komórki w kierunku centrum, gdzie znajduje się główny punkt sortowania — aparat Golgiego. Autorzy koncentrują się na PACS1, białku pomagającym wybierać, które ładunki trafiają na dyneinę, a także regulującym stan torów poprzez inne białko, HDAC6, które kontroluje chemiczną modyfikację (acetylację) mikrotubul. Neurony, z bardzo długimi wypustkami, są szczególnie wrażliwe na nawet drobne usterki w tym systemie.
Mutant-koordynator, który chwyta zbyt mocno
Zespół PACS1 wywołuje powtarzalna mutacja R203W w PACS1. Zespół badawczy wykazał, że zarówno normalny, jak i zmutowany PACS1 fizycznie wiążą ciężkie łańcuchy dyneiny, jednak forma zmutowana przyczepia się silniej. Na komórkach skóry pacjentów i w zmodyfikowanych liniach komórkowych pokazali, że to nadmierne zaangażowanie daje taki sam efekt, jak częściowa utrata funkcji dyneiny: aparat Golgiego rozpada się na rozproszone mini‑stosy, a ważny enzym o nazwie furyna, zwykle zlokalizowany po stronie trans Golgiego, trafia omyłkowo do innych przedziałów komórkowych. Analizując strukturę PACS1, zidentyfikowali krótki fragment beta‑struktury — „łatkę”, która bezpośrednio styka się z dyneiną. Gdy zmienili tę łatkę, nie naruszając innych funkcji PACS1, furyna ponownie straciła właściwe miejsce, co potwierdza, że uścisk dyneiny przez PACS1 jest kluczowy dla prawidłowego ustawienia ładunków. 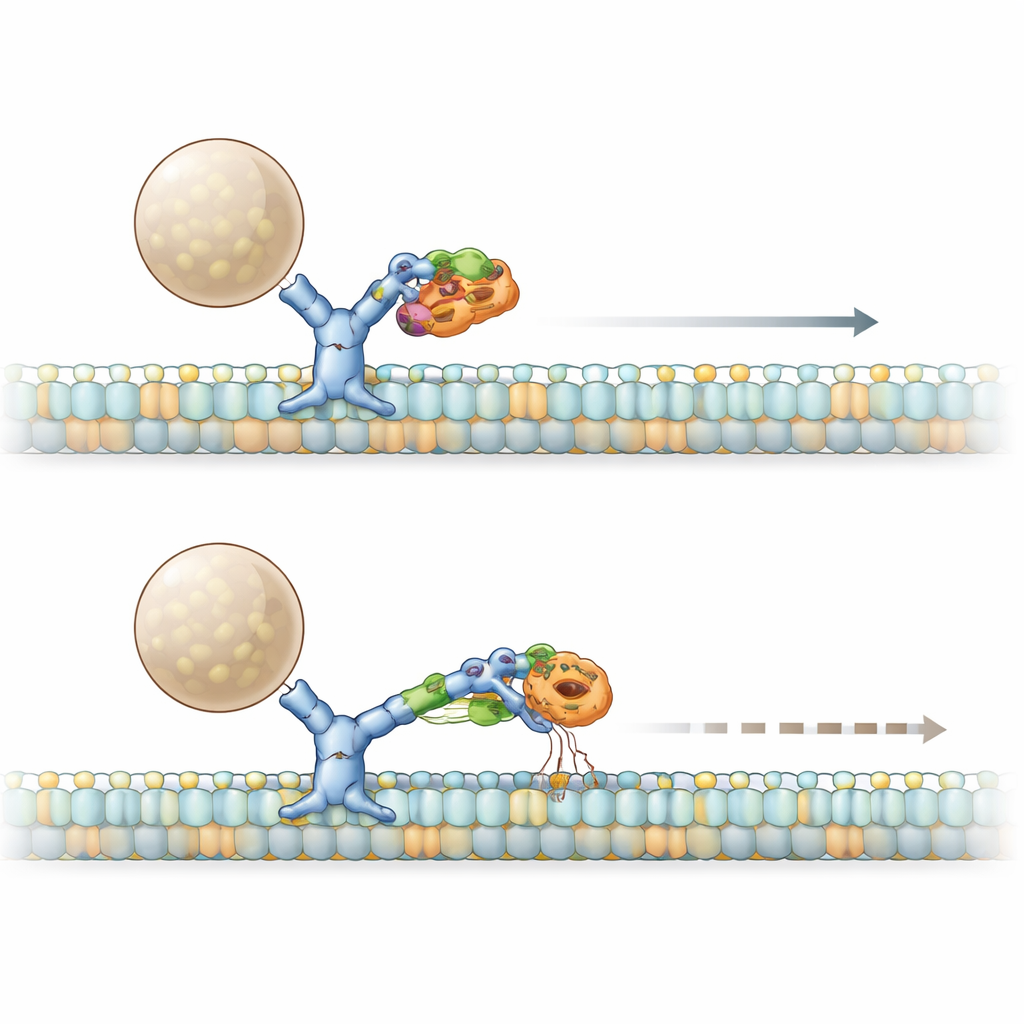
Jak sojusz trzech białek zatyka silnik
Historia komplikuje się o dwóch dodatkowych uczestników: HDAC6 oraz adaptor o nazwie BICD2, który pomaga składać aktywne kompleksy dyneiny. Zmutowany PACS1 nie tylko zwiększa aktywność HDAC6, zmniejszając acetylację mikrotubul, lecz także tworzy powiększony kompleks z HDAC6 i BICD2. Testy biochemiczne wykazały, że mutant PACS1 i HDAC6 razem odciągają BICD2 od dyneiny, pozostawiając jednocześnie jego związek z poruszającym się do przodu silnikiem (kinezyną) nienaruszonym. W żywych komórkach sztuczny ładunek, który zwykle gna szybko dzięki dyneinie, zwolnił, a mniej ładunków w ogóle się poruszało, gdy obecny był zmutowany PACS1. Zablokowanie aktywności HDAC6 przywróciło zarówno prędkość, jak i liczbę poruszających się cząstek, pokazując, że kompleks mutanta PACS1–HDAC6–BICD2 działa jak hamulec uniemożliwiający dyneinie inicjację i podtrzymanie transportu.
Ratowanie ruchu naturalnym wspomagaczem dyneiny
Następnie badacze sprawdzili, czy dyneinę można „reaktywować” pomimo obecności zmutowanego kompleksu. Sięgnęli po Lis1, znanego pomocnika dyneiny, który stabilizuje aktywne zespoły motorowe. W komórkach pacjentów poziomy Lis1 były nieco obniżone. Gdy dodali dodatkowy Lis1, dwie rzeczy uległy poprawie: aparat Golgiego ponownie skupił się w pobliżu centrum komórki, a lizosomy — inna grupa organelli, które przesunęły się na zewnątrz — wróciły na miejsce. W tym samym teście ruchliwości Lis1 zwiększył zarówno częstotliwość, jak i prędkość transportu napędzanego przez dyneinę w obecności zmutowanego PACS1. Wyniki te pokazują, że problem nie polega na braku dyneiny, ale na tym, iż ulega ona uwięzieniu w słabo aktywnym stanie — stanie, który można częściowo skorygować poprzez osłabienie HDAC6 lub wzmocnienie aktywacji dyneiny.
Powiązanie rzadkiego zespołu z szerszym zestawem zaburzeń
Łącząc analizę strukturalną, biologię komórki i obrazowanie na żywo, autorzy proponują spójny model: PACS1 normalnie łączy wybrane ładunki z dyneiną i stroi wydajność silnika poprzez HDAC6 i acetylację mikrotubul. Mutacja R203W odsłania powierzchnię interakcyjną PACS1, nadmiernie rekrutując HDAC6 i BICD2 do kompleksu, który osłabia zdolność dyneiny do chwytania mikrotubul i efektywnego przemieszczania się. W efekcie dochodzi do szerokiego niewłaściwego rozmieszczenia Golgiego, lizosomów i innych ładunków, szczególnie w neuronach, gdzie transport na długich dystansach ma kluczowe znaczenie. Mechanizm ten pomaga wyjaśnić, dlaczego obniżenie poziomu PACS1 lub HDAC6 za pomocą terapii antysensownych koryguje defekty mózgowe w modelach mysich i jest obecnie badane u pacjentów. Szerzej rzecz biorąc, umieszcza zespół PACS1 w rosnącym spektrum zaburzeń związanych z ruchem po mikrotubulach, obok chorób wywołanych mutacjami w dyneinie, BICD2 i pokrewnych czynnikach transportu.
Cytowanie: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Słowa kluczowe: zespół PACS1, transport dyneinowy, ruch wzdłuż mikrotubul, organizacja aparatu Golgiego, rozwój neuronów