Clear Sky Science · pl
Białko sekrecyjne CLCF1 poprawia przebieg cholestatycznej choroby wątroby poprzez hamowanie syntezy kwasów żółciowych w wątrobie i wspieranie ich wydalania
Dlaczego to badanie ma znaczenie dla zdrowia wątroby
Cholestatyczne choroby wątroby to stany, w których żółć — płyn trawienny wytwarzany przez wątrobę — przestaje prawidłowo odpływać i zamiast tego gromadzi się, stopniowo zatruwając wątrobę od środka. Dostępne leki pomagają tylko części pacjentów, a wielu z nich ostatecznie wymaga przeszczepu wątroby. To badanie odsłania naturalnie produkowane białko, nazwane CLCF1, które organizm wydaje się włączać jako system obronny podczas cholestazy. Zrozumienie mechanizmów jego działania może wskazać drogę do nowych terapii chroniących wątrobę zarówno przez zmniejszenie produkcji szkodliwych składników żółci, jak i przez ułatwienie ich wydalania.
Ukryty pomocnik w chorującej wątrobie
Naukowcy zaczęli od badania tkanki wątrobowej pacjentów z pierwotnym zapaleniem dróg żółciowych (PBC) i pierwotnym stwardniającym zapaleniem dróg żółciowych (PSC), dwoma głównymi postaciami przewlekłej cholestazy. Porównali osoby we wczesnym stadium choroby z tymi z bardziej zaawansowaną cholestazą oraz przeanalizowali dostępne publiczne zbiory danych genowych. We wszystkich tych niezależnych źródłach wyróżniało się jedno białko sekrecyjne: CLCF1 konsekwentnie znajdował się wśród najsilniej podwyższonych genów w cholestatycznych wątrobach. Wyższe poziomy CLCF1 korelowały z gorszymi markerami krwi świadczącymi o ciężkości choroby, co sugeruje, że wątroba zwiększa produkcję tego białka w miarę nasilania się stresu i nagromadzenia żółci. U pacjentów we wczesnym stadium leczeniem standardowym, kwasem ursodeoksycholowym, lepiej reagujący mieli zwykle więcej CLCF1 w wątrobie, co sugeruje, że białko to może oznaczać bardziej adaptacyjną, podatną na leczenie wątrobę.
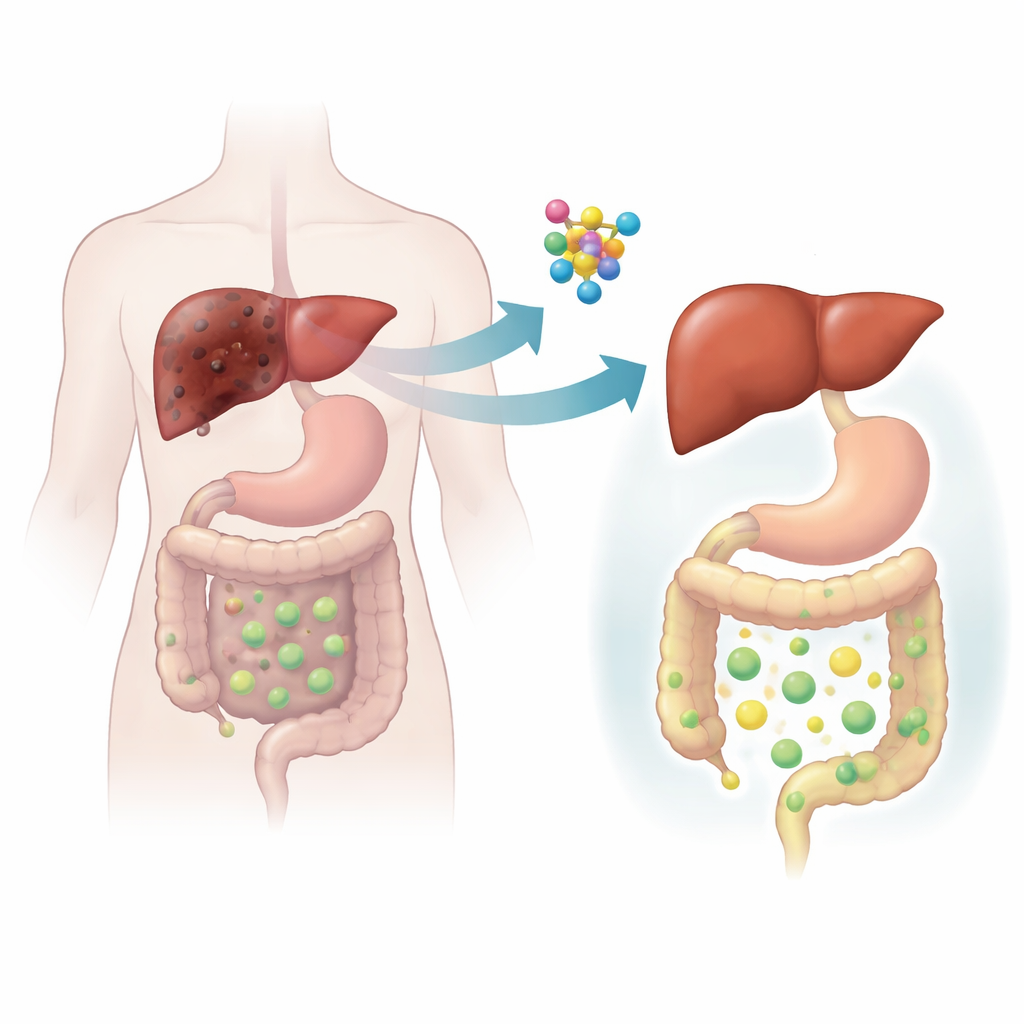
Testowanie CLCF1 w modelach zwierzęcych
Aby wyjść poza korelacje obserwowane u ludzi, zespół badawczy sięgnął po myszy i zastosował zarówno manipulacje genetyczne, jak i dietetyczne, by naśladować cholestatyczną chorobę wątroby. W dwóch różnych modelach mysich cholestaza silnie zwiększała produkcję Clcf1 w wątrobie, co odzwierciedla obserwacje u ludzi. Gdy naukowcy specyficznie usunęli receptor dla CLCF1 z komórek wątrobowych, uraz cholestatyczny znacząco się pogorszył: przewody żółciowe nadmiernie rozrosły się, występowała martwica tkanki wątrobowej, nasiliło się zapalenie, nagromadziła się blizna, a toksyczne kwasy żółciowe kumulowały się. Odwrotne eksperymenty przyniosły bardziej optymistyczne wyniki. Kiedy zespół użył bezpiecznego wirusa do zwiększenia poziomu Clcf1 wyłącznie w wątrobie, myszy były chronione. Ich wątroby miały zdrowszy wygląd, wyniki badań krwi się poprawiły, włóknienie zmalało, a ilość kwasów żółciowych zalegających w wątrobie znacznie spadła.
Zakrananie strumienia i otwieranie odpływu
Jak CLCF1 tak skutecznie redukuje przeciążenie kwasami żółciowymi? Naukowcy wykryli dwa uzupełniające się mechanizmy. Po pierwsze, CLCF1 bezpośrednio uspokaja maszynerię wątroby produkującą żółć. W wielu modelach mysich i w hodowanych komórkach wątrobowych dodatkowy CLCF1 konsekwentnie wyłączał kluczowe enzymy konwertujące cholesterol do kwasów żółciowych, skutecznie zakręcając kran syntezy nowej żółci. Działo się to bez aktywacji zwykłego wątrobowego przełącznika kontroli żółci — jądrowego receptora FXR — co sugeruje, że CLCF1 wykorzystuje alternatywną drogę wewnątrzkomórkową do spowolnienia syntezy żółci. Po drugie, CLCF1 wpływał na dalsze losy żółci w organizmie. Przekształcał skład mikrobioty jelitowej w kierunku bakterii szczególnie efektywnych w przetwarzaniu kwasów żółciowych i zwiększał ilość kwasów żółciowych usuwanych z organizmu w kale, działając niczym silniejszy odpływ.
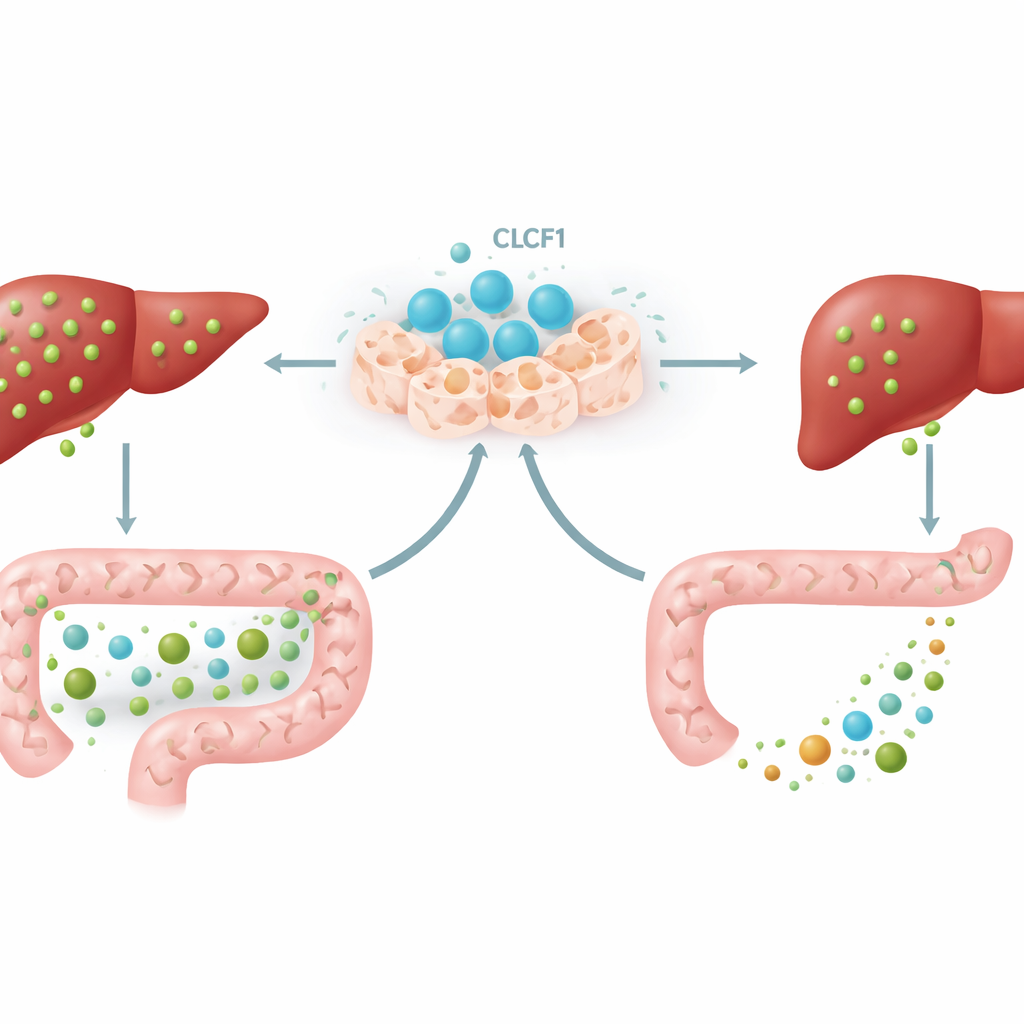
Rozmowa jelito–wątroba
Kluczowy element układanki stanowiła pętla sygnałowa między jelitem a wątrobą. Niektóre kwasy żółciowe w jelicie aktywują czujnik o nazwie FXR w komórkach jelitowych, które następnie wydzielają hormon przekaźnikowy zwany FGF15 u myszy. Hormon ten podróżuje krwią do wątroby i nakazuje jej ograniczyć produkcję kwasów żółciowych. Przy dodatkowym CLCF1 myszy gromadziły w jelitach konkretne typy kwasów żółciowych — szczególnie formy znane z silnej aktywacji FXR. W rezultacie jelitowy FXR został włączony, poziomy FGF15 wzrosły zarówno w jelicie, jak i w wątrobie, a wątroba dodatkowo zmniejszyła produkcję kwasów żółciowych. Gdy naukowcy zablokowali jelitowy FXR lekiem działającym wyłącznie w światle jelita, większość ochronnego efektu CLCF1 zanikła, wykazując, że ta rozmowa jelito–wątroba jest istotną częścią działania białka.
Co to może znaczyć dla przyszłych terapii
W sumie wyniki przedstawiają CLCF1 jako wbudowany zawór bezpieczeństwa w cholestatycznej chorobie wątroby. Białko redukuje poziomy kwasów żółciowych z obu stron: spowalnia ich powstawanie w wątrobie i zachęca do ich usuwania przez jelito, przy wsparciu przyjaznych mikroorganizmów jelitowych oraz hormonalnego sprzężenia zwrotnego. W odróżnieniu od istniejących leków aktywujących FXR w całym organizmie, które mogą powodować działania niepożądane, takie jak świąd i nieprawidłowe stężenia tłuszczów we krwi, CLCF1 wydaje się kierować kontrolą żółci bardziej łagodnie i selektywnie, zwłaszcza poprzez jelito. Choć prace te opierają się wciąż na modelach mysich i próbkach laboratoryjnych, sugerują, że zwiększanie CLCF1 lub naśladowanie jego szlaków może stać się podstawą nowych terapii — oraz że pomiar tego białka, albo kwasów żółciowych, które ono wzbogaca w jelicie, mógłby pomóc zidentyfikować pacjentów, którzy skorzystaliby najbardziej.
Cytowanie: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Słowa kluczowe: cholestatyczna choroba wątroby, kwasy żółciowe, <keyword>CLCF1, mikrobiota jelitowa