Clear Sky Science · pl
System sekrecji typu VI u Acinetobacter: mechanizmy, biologia i potencjał terapeutyczny
Ukryte bronie w zarazkach szpitalnych
Wielu ludzi wie, że niektóre szczepy szpitalnych zarazków opierają się antybiotykom, ale mniej osób zdaje sobie sprawę, że te drobnoustroje toczą też zaciekłe walki między sobą. Niniejszy przegląd opisuje mikroskopijną „odciąganą lancę” w Acinetobacter — grupie bakterii obejmującej słynny patogen szpitalny Acinetobacter baumannii. Zrozumienie, jak działa ta wbudowana broń, kiedy jest uruchamiana i jak pomaga osiedlać się infekcjom, może otworzyć nowe drogi do diagnozowania i unieszkodliwiania zagrażających życiu, opornych na leki zakażeń.
Maszyna przetrwania, nie tylko zatruty grot
Gatunki Acinetobacter żyją w glebie, wodzie i na naszej skórze, ale niektóre stały się wyjątkowo skutecznymi patogenami szpitalnymi. Kluczowym narzędziem w ich arsenale jest system sekrecji typu VI, w skrócie T6SS — maleńka kurczliwa maszyna zakotwiczona w otoczce komórkowej. Po uruchomieniu wystrzeliwuje kolczasty grot naładowany toksycznymi białkami w kierunku sąsiednich komórek, często zabijając konkurencyjne bakterie przy zetknięciu. W przeciwieństwie do niektórych innych drobnoustrojów posiadających kilka wariantów tego systemu, patogeniczne Acinetobacter zwykle mają tylko jeden T6SS, lecz przebudowały tę pojedynczą platformę tak, by służyła wielu celom — od odpierania rywali po kształtowanie przebiegu zakażeń.
Przebudowany mechanizm: nietypowa platforma startowa
Większość bakterii buduje T6SS w oparciu o standardowy zestaw części, ale Acinetobacter przeprojektowały kilka kluczowych elementów. Brakuje tu powszechnego kotwiczenia w zewnętrznej błonie zwanego TssJ; zamiast tego system polega na trzech wyspecjalizowanych pomocnikach: TsmK tworzy fundament w błonie wewnętrznej, TslA stabilizuje długie „tubularne” białko (TssM) przechodzące przez ścianę komórkową, a TagX lokalnie przecina ścianę, robiąc miejsce dla broni. Ponadto szczególne białko grotu, VgrG1, musi mieć niemal idealny kształt, żeby system w ogóle zadziałał — pojedyncze zmiany aminokwasowe mogą go unieruchomić. Razem te modyfikacje pokazują, jak ewolucja potrafi zastąpić brakujące elementy nowymi rozwiązaniami, zachowując podstawową zasadę wystrzału.
Inteligentne sterowanie: kiedy warto przejść do ataku
Budowa i wystrzelenie tej nanomaszyny są kosztowne energetycznie, więc Acinetobacter trzyma ją pod ścisłą kontrolą. Globalne białko wiążące DNA (H‑NS) oraz specjalne represory przenoszone na plazmidach wielolekowych mogą zablokować system w pozycji „wyłączonej”, zwłaszcza gdy geny oporności są wymieniane między komórkami. Przy dużym zagęszczeniu komórek chemiczne sygnały „kworum” mogą go włączyć, przygotowując bakterie do rywalizacji w bliskim kontakcie. Jony metali też odgrywają rolę: pod stresem oksydacyjnym importowany mangan aktywuje małe RNA, które powoduje degradację kluczowych komunikatów T6SS, wygaszając broń, by sprzyjać przeżyciu wewnątrz gospodarza. Nawet otoczka — cukrowe pokrycie zewnętrzne — działa równocześnie jako tarcza i hamulec, blokując nadchodzące ataki, ale też mechanicznie tłumiąc własne wystrzały Acinetobacter.
Różnorodne narzędzia do mikroskopijnych ciosów
Gdy Acinetobacter pociągnie za spust, może dostarczyć szeroki wachlarz toksyn. Niektóre enzymy rozkładają twardą ścianę komórkową rywali; inne stopniowo uszkadzają błony komórkowe, a jeszcze inne rozcinają DNA wewnątrz komórek docelowych. Każda toksyna jest sparowana z odpowiadającym jej białkiem „odpornościowym”, które chroni atakującego przed przyjaznym ogniem. Jedna toksyna tnąca DNA, obecnie nazwana TafE, potrafi nawet zabić grzyby, sugerując potyczki między królestwami w miejscach takich jak jelito czy płuca. Badania genomowe wskazują, że Acinetobacter koduje wiele kolejnych, jeszcze nieopisanych toksyn, często zgrupowanych w dużych białkach Rhs pełniących rolę modułowych nośników. Zamiast polegać na pojedynczym ciosie, bakterie te zdają się stosować warstwowe ataki, uszkadzając jednocześnie kilka istotnych struktur.
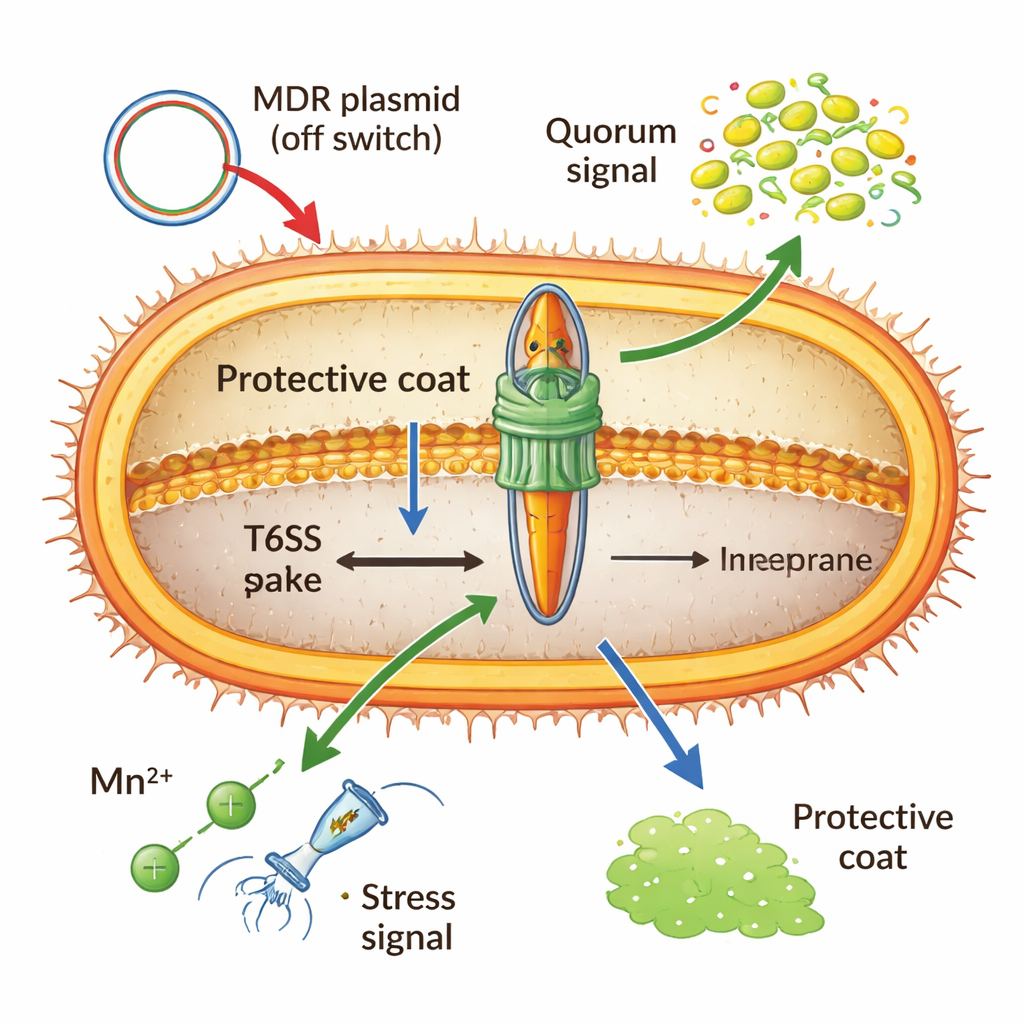
Kształtowanie zakażeń, genów i przyszłych terapii
Dane z izolatów pacjentów i modeli zwierzęcych sugerują, że aktywny T6SS często idzie w parze z cięższym przebiegiem choroby, silniejszym zapaleniem i lepszym przeżywaniem bakterii wewnątrz gospodarzy. Zabijając pobliskie mikroby, system uwalnia też DNA, które kompetentne komórki Acinetobacter mogą naturalnie pobierać, przyspieszając rozprzestrzenianie cech takich jak oporność na antybiotyki. Jednak ciągłe utrzymywanie broni w trybie aktywnym jest kosztowne, dlatego wiele skutecznych szczepów szpitalnych nosi plazmidy lub mutacje, które go wyciszają po zabezpieczeniu oporności. Autorzy argumentują, że system sekrecji powinien być postrzegany nie jako prosty czynnik wirulencji, lecz jako elastyczny „moduł sprawności”, który Acinetobacter reguluje w górę lub w dół, aby zrównoważyć agresję, przetrwanie i zużycie energii. Ta nowa perspektywa wskazuje na praktyczne zastosowania — od szczepionek skierowanych przeciw konserwowanym elementom T6SS po leki selektywnie blokujące mechanizm wystrzału — które mogą pomóc klinicystom przechytrzyć niebezpiecznego i adaptacyjnego przeciwnika szpitalnego.
Cytowanie: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Słowa kluczowe: Acinetobacter, system sekrecji typu VI, oporność na antybiotyki, konkurencja bakteryjna, zakażenia szpitalne