Clear Sky Science · pl
Glikozylacja jako dynamiczny regulator szlaków sygnalizacyjnych odporności wrodzonej RLR i cGAS-STING
Jak cukrowe znaczniki pomagają komórkom wykrywać wirusy
Nasze komórki nieustannie czuwają przed napływem wirusów, a wiele z tej obrony opiera się na drobnych cukrowych znaczkach przyłączanych do białek. Ten przegląd wyjaśnia, jak te znaczniki cukrowe, zwane glikozylacją, działają bardziej jak regulatory natężenia niż proste włączniki/wyłączniki w kluczowych szlakach przeciwwirusowych. Zrozumienie tego cukrowego dostrajania może otworzyć nowe drogi do poprawy szczepionek, leczenia infekcji wirusowych, a nawet wykorzystania układu odpornościowego przeciwko nowotworom.
Wczesny alarm komórki
Gdy wirusy wnikają do komórki, pozostawiają po sobie charakterystyczne fragmenty RNA lub DNA. Specjalistyczne systemy „alarmowe” patrolują wnętrze komórki w poszukiwaniu tych genetycznych śladów. Jeden z systemów, nazywany szlakiem receptorów podobnych do RIG-I (RLR), wykrywa wirusowe RNA. Inny, znany jako szlak cGAS–STING, rozpoznaje DNA pojawiające się w niewłaściwym miejscu wewnątrz komórki. Po aktywacji oba szlaki uruchamiają kaskady chemiczne kończące się uwolnieniem interferonów typu I i cząsteczek zapalnych — silnych sygnałów ostrzegających komórki sąsiednie i mobilizujących obronę immunologiczną. Ponieważ zbyt słaba lub zbyt silna odpowiedź może być niebezpieczna, komórka musi precyzyjnie regulować te alarmy, a glikozylacja jest jednym z kluczowych mechanizmów tej regulacji. 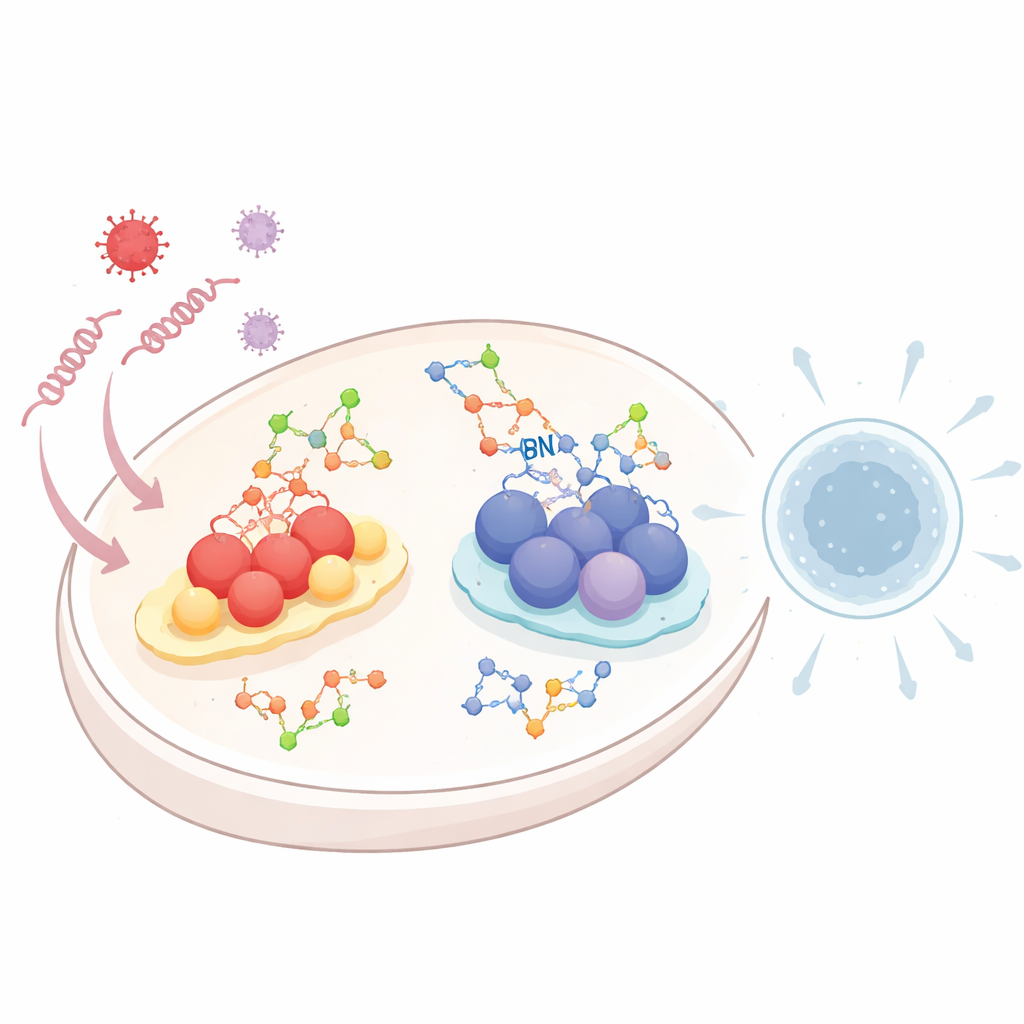
Cukrowe powłoki jako precyzyjne regulatory
Glikozylacja dodaje małe jednostki cukrowe do białek w różnych miejscach komórki. W wewnętrznej sieci transportowej komórki, w siateczce śródplazmatycznej i aparacie Golgiego, rozległe łańcuchy N-glikanów pomagają białkom prawidłowo się fałdować, pozostawać stabilnymi i trafiać do właściwych błon. Natomiast lżejsza forma, zwana O-GlcNAcylacją, przyłącza pojedynczy cukier do białek w cytoplazmie i jądrze. Ten minimalistyczny znacznik jest wysoce dynamiczny — szybko się odwraca w odpowiedzi na poziom składników odżywczych i stres dzięki dwóm enzymom dodającym lub usuwającym go. Artykuł opisuje, że różne rodzaje cukrów nie po prostu włączają lub wyłączają czujniki odpornościowe; zamiast tego regulują łatwość grupowania się czujników, ich trwałość oraz siłę sygnalizacji. W ten sposób glikozylacja łączy stan metaboliczny komórki bezpośrednio z jej gotowością do walki z infekcją.
Dostrajanie szlaku detekcji RNA
W systemie detekcji RNA RLR centralnym przekaźnikiem jest białko MAVS zlokalizowane na mitochondriach, pełniące rolę kluczowego węzła. Przegląd pokazuje, że O-GlcNAcylacja MAVS może zarówno przyspieszać, jak i hamować sygnalizację przeciwwirusową, w zależności od miejsca przyłączenia cukru. Znaczniki cukrowe w określonych miejscach sprzyjają kolejnym modyfikacjom białka, takim jak specyficzny rodzaj łańcucha ubikwitynowego, które pomagają MAVS tworzyć duże skupiska sygnałowe i napędzać silną produkcję interferonów przeciw wirusom RNA. Inne miejsca glikozylacji utrzymują MAVS rozproszony i nieaktywny w warunkach spoczynkowych, zapobiegając niepotrzebnemu zapaleniu. Infekcja wirusowa i zmiany w metabolicznej ścieżce produkcji cukrów komórkowych mogą przesunąć równowagę między tymi aktywującymi i hamującymi znacznikami. Pokrewne modyfikacje innego czynnika, IRF5, mogą skierować układ odpornościowy w stronę szkodliwych „burz cytokin”, co podkreśla, że więcej cukru nie zawsze znaczy lepiej. Równolegle wirusy potrafią wykorzystywać N-glikany na białkach powierzchniowych, takich jak receptor wzrostu EGFR, aby oznaczać górnoprzepustowe czujniki, np. RIG-I, do degradacji, osłabiając obronę przeciwwirusową.
Dostrajanie szlaku detekcji DNA
Szlak cGAS–STING wykrywający DNA również jest silnie modulowany przez glikozylację. STING, białko błonowe w siateczce śródplazmatycznej, potrzebuje łańcuchów N-glikanów, by prawidłowo się fałdować, pozostawać stabilnym i zgromadzić w klastry sygnałowe po aktywacji przez przekazniki pochodzące z DNA. Bez tych cukrów STING nie tworzy struktur wyższych rzędów ani nie przemieszcza się przez odpowiednie przedziały komórkowe niezbędne do silnego uwolnienia interferonów. Jednocześnie O-GlcNAcylacja STING w określonym miejscu wzmacnia inny zestaw chemicznych znaczników, które promują jego grupowanie i transport, potęgując sygnały przeciwwirusowe przeciw wirusom DNA. Łańcuchy cukrowe zwane siarczonymi glikoaminoglikanami, budowane w Golgi, dodatkowo pomagają, ułatwiając polimeryzację aktywowanego STING w długie struktury rekrutujące enzymy dalszego stopnia. Wirusy kontratakują, modyfikując własne glikoproteiny lub uruchamiając szlaki degradacji celujące w STING, często w tych samych przestrzeniach komórkowych, gdzie te cukrowe ozdoby są przyłączane lub przetwarzane. 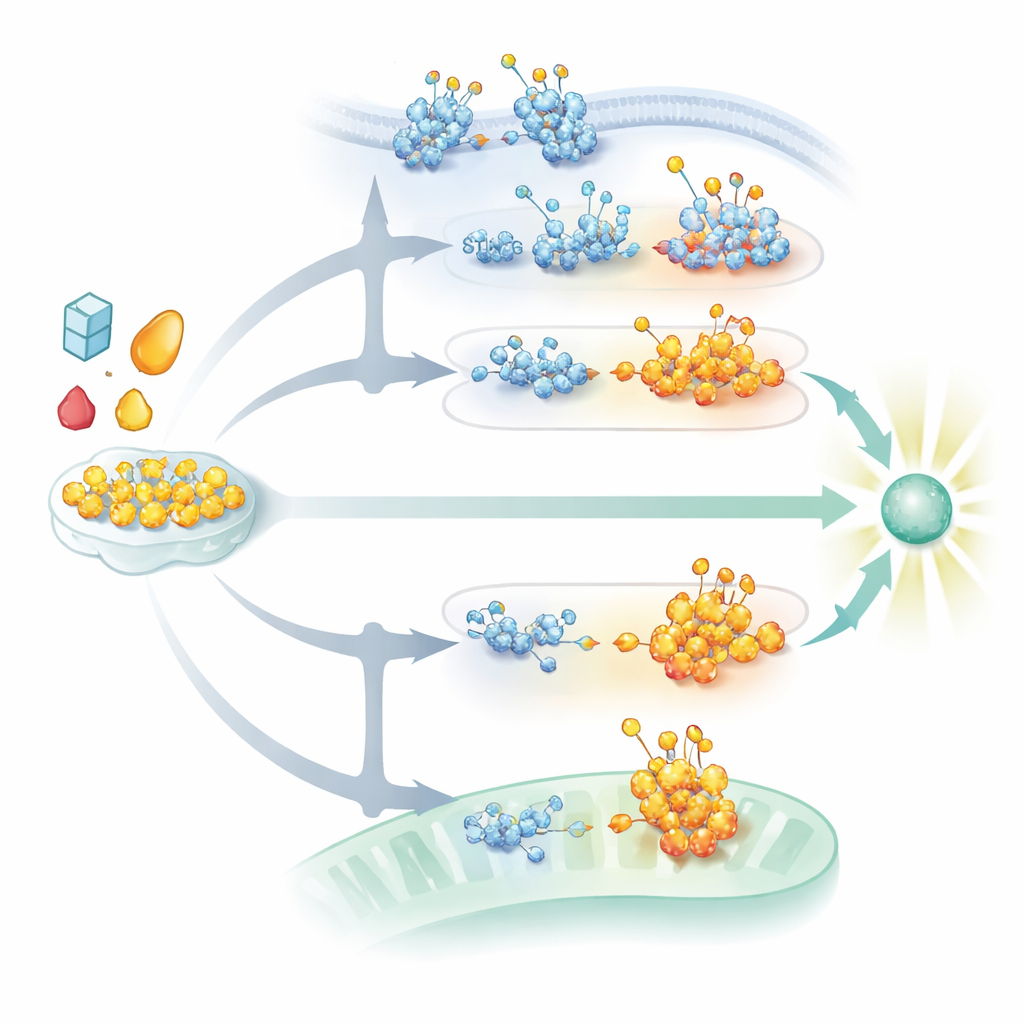
Metabolizm, choroby i przyszłe terapie
Ponieważ główny donor cukru dla O-GlcNAcylacji powstaje w szlaku metabolicznym zwanym drogą biosyntezy heksozaminowej, zmiany w wykorzystaniu składników odżywczych bezpośrednio kształtują sygnalizację przeciwwirusową. Wiele wirusów napędza ten szlak na swoją korzyść, podczas gdy eksperymentalne zwiększanie lub blokowanie przepływu heksozamin może w modelach zwierzęcych wzmacniać lub osłabiać odpowiedzi przeciwwirusowe. Przegląd łączy te mechanizmy z chorobami człowieka: guzy często przebudowują glikozylację, by tłumić sygnalizację interferonową i unikać ataku immunologicznego, podczas gdy przewlekły stres metaboliczny lub wrodzone defekty w przetwarzaniu glikanów mogą przechylić równowagę w stronę szkodliwej autoimmunizacji. Autorzy argumentują, że enzymy kontrolujące glikozylację — zwłaszcza te dodające lub usuwające O-GlcNAc oraz budujące kluczowe struktury N-glikanów — są obiecującymi, lecz trudnymi celami terapeutycznymi. Przyszłe terapie prawdopodobnie będą musiały działać w sposób specyficzny dla miejsca i świadomy kontekstu, delikatnie korygując „glyko-kod” w stronę lepszej ochrony przed infekcjami, rakiem i zaburzeniami zapalnymi, bez wywoływania nowych form zaburzeń odporności.
Ogólne znaczenie dla codziennego zdrowia
Mówiąc prościej, artykuł pokazuje, że przednie alarmy przeciwwirusowe organizmu nie działają w izolacji — są powiązane z użytkowaniem energii i chemia cukrów w komórce. Drobne cukrowe znaczniki na kilku krytycznych białkach decydują, czy obce genom wirusowy wywoła umiarkowane ostrzeżenie, pełną obronę, czy niebezpieczną nadreakcję. Odszyfrowanie i w efekcie nauczenie się modulowania tego cukrowego systemu kontrolnego może pozwolić badaczom zaprojektować terapie poprawiające skuteczność szczepionek, pomagające usuwać uporczywe infekcje, odkrywać nowotwory przed układem odpornościowym oraz łagodzić niekontrolowane zapalenie w chorobach autoimmunologicznych.
Cytowanie: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Słowa kluczowe: odporność wrodzona, glikozylacja, szlak RLR, cGAS-STING, O-GlcNAcylacja