Clear Sky Science · pl
Modelowanie napędzane tempem wzrostu sugeruje, że adaptacja fenotypowa napędza oporność na leki w raku melanocytowym z mutacją BRAFV600E
Komórki nowotworowe, które uczą się żyć z lekami
Leki celowane zrewolucjonizowały leczenie wielu osób z czerniakiem, poważnym nowotworem skóry. Jednak te leki niemal zawsze przestają działać: guzy, które kiedyś się kurczyły, zaczynają znowu rosnąć. W badaniu zadano proste, ale doniosłe pytanie: czy zamiast polegać wyłącznie na mutacjach genetycznych, komórki czerniaka mogą „nauczyć się” przetrwać terapię przez zmianę zachowania — i czy to uczenie się może wyjaśniać, dlaczego niektóre schematy podawania leków działają lepiej niż inne?
Od wrażliwych komórek do ocalałych
Naukowcy skupili się na komórkach czerniaka z powszechną zmianą w genie BRAF, która czyni je szczególnie wrażliwymi na inhibitory BRAF. W doświadczeniach laboratoryjnych z wcześniejszych badań komórki te wystawiano na działanie leku encorafenibu w różnych dawkach i przez różne okresy. Poprzez dokładne mierzenie, jak szybko komórki rosły lub umierały w każdym warunku, autorzy podzielili populację na dwie szerokie kategorie: komórki nigdy wcześniej nieeksponowane na lek (drug-naive) oraz komórki zaadaptowane do leku, które żyły w obecności leku przynajmniej przez tydzień. Komórki nieeksponowane dobrze rosły bez leczenia, ale były silnie hamowane lub zabijane przez lek. Komórki zaadaptowane rosły lepiej w obecności leku, lecz traciły tę przewagę po usunięciu leku — co sugeruje, że ich przetrwanie wiązało się z elastyczną, odwracalną zmianą stanu, a nie trwałym uszkodzeniem genetycznym.
Mapa ukrytych zachowań komórek
Aby zrozumieć te zmiany, zespół zbudował model matematyczny, w którym każdej komórce przypisano „stan fenotypowy” — abstrakcyjne położenie na skali od bardzo wrażliwego na lek do bardzo opornego. Zamiast zakładać tylko dwa typy komórek, dopuszczono wiele stanów pośrednich, odzwierciedlających stopniowe przesunięcia zachowania widoczne w biologicznych markerach oporności. Dla każdej kombinacji stanu i dawki leku oszacowano netto tempo wzrostu, które mogło być dodatnie (więcej podziałów niż zgonów) lub ujemne (więcej zgonów niż podziałów). Wszystkie te tempo ułożono w siatkę, czyli „macierz fitness”, działającą jak krajobraz: w niektórych stanach przy określonych dawkach komórki dobrze sobie radzą, w innych są skazane na zagładę. W modelu komórki mogą przesuwać się krok po kroku po tym krajobrazie w miarę włączania lub wyłączania leczenia.
Czy komórki dryfują, czy wspinają się ku przewadze?
Kluczową nieznaną była natura przemieszczania się komórek po tym krajobrazie. Autorzy przetestowali cztery możliwe strategie. W jednej komórki nigdy nie zmieniają stanu, więc wszelka oporność musi być obecna od początku. W innej komórki wędrują losowo między sąsiednimi stanami, niczym pijany wędrowiec, niezależnie od tego, czy ich sytuacja się poprawia. W dwóch pozostałych strategiach komórki mają tendencję do przechodzenia w kierunku stanów o wyższym tempie wzrostu — albo z pewnym hałasem i potknięciami, albo silnie, zawsze wspinając się ku lepszym warunkom przetrwania. Kiedy zespół uruchomił symulacje komputerowe i porównał je z rzeczywistymi danymi laboratoryjnymi, zwłaszcza eksperymentami, w których lek podawano ciągle lub w trybie włącz/wyłącz (tydzień włączony, tydzień wyłączony), tylko strategie zakładające wspinanie się ku wyższej fitnesie potrafiły odtworzyć obserwacje: leczenie przerywane przy wysokiej dawce lepiej tłumiło liczbę komórek niż leczenie ciągłe przy tym samym czasie łącznym i większej łącznej ilości leku.
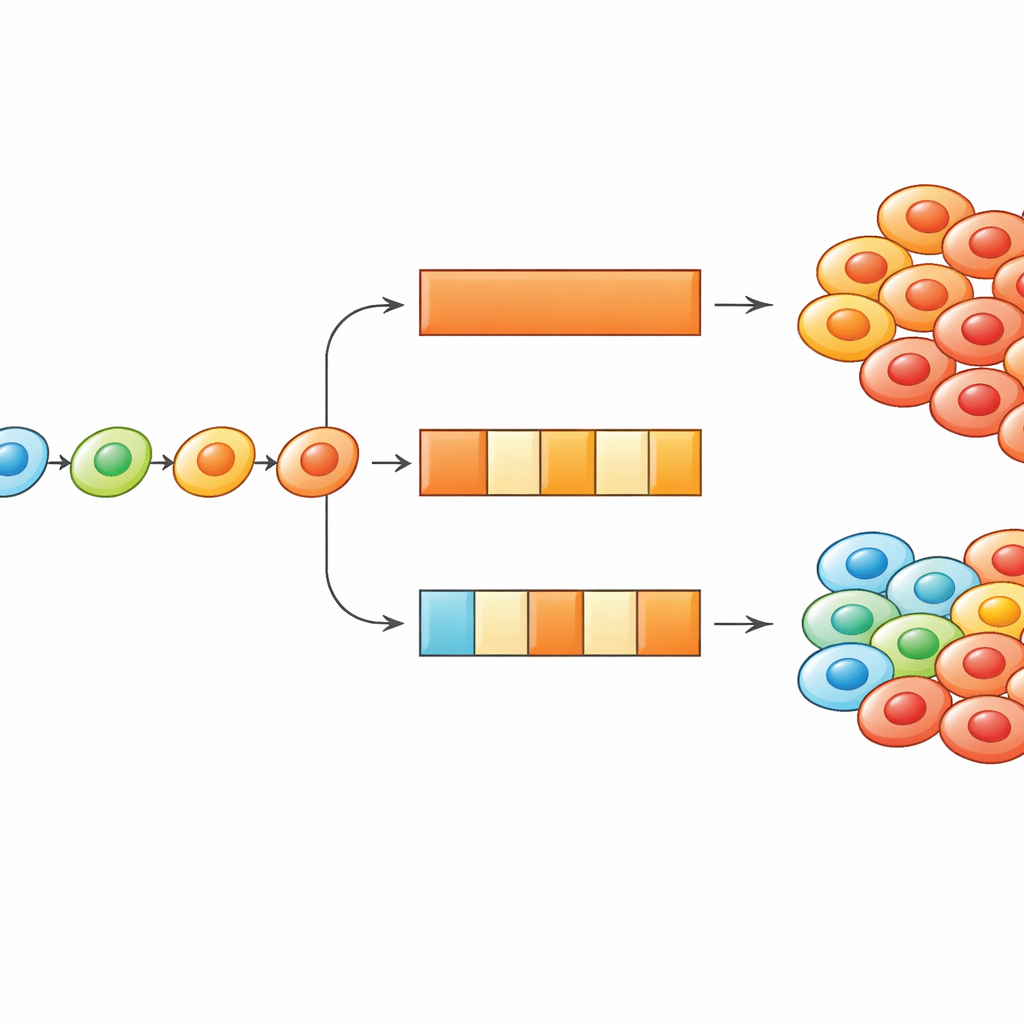
Wykorzystanie dawkowania w trybie włącz/wyłącz, by obrócić adaptację przeciwko rakowi
Zagłębiając się dalej, badacze użyli zarówno symulacji, jak i prostszych równań, by zbadać, jak często komórkom pozwala się zmieniać stan oraz jak długie są okresy leku włączonego i wyłączonego. Stwierdzili, że gdy komórki adaptują się ukierunkowanie, harmonogramy leczenia można dostroić, by albo spowalniać, albo wykorzystywać tę adaptację. Skrócenie częstości, z jaką komórki mogą aktualizować swój stan — konceptualnie: spowolnienie mechanizmów biologicznych umożliwiających zmianę fenotypową — zwykle zwiększa skuteczność leczeń przerywanych, ponieważ komórki nie są w stanie tak szybko wspiąć się do wysoce opornych stanów. Z drugiej strony, jeśli komórki zaczynają w silnie opornym stanie, przerwy w leczeniu mogą dać im czas, by zsunęły się z powrotem ku stanom bardziej wrażliwym, tak że ponowne wprowadzenie leku wywołuje falę śmierci komórek. Badanie pokazuje, jak czas dawkowania i tempo adaptacji komórek razem decydują, który schemat działa najlepiej.
Co to oznacza dla przyszłej opieki onkologicznej
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że komórki nowotworowe nie są tylko stałymi wrogami; są zmiennokształtne. W tym układzie czerniakowym komórki wydają się aktywnie zmierzać ku zachowaniom, które pomagają im rosnąć w danych warunkach. Model autorów sugeruje, że ta ukierunkowana adaptacja sama w sobie — bez odwoływania się do różnych trwałych klonów — może wyjaśniać, dlaczego harmonogramy włącz/wyłącz czasami przewyższają ciągłe dawkowanie, nawet gdy używają ogólnie mniej leku. Choć wyniki pochodzą z hodowanych w laboratorium komórek i wymagają dalszych badań zanim będą mogły kierować leczeniem pacjentów, podejście to oferuje praktyczne ramy: mierząc, jak szybko i w jakim kierunku komórki nowotworowe się adaptują, lekarze mogą w przyszłości zaprojektować schematy terapii, które nie tylko atakują guzy, ale też skierują ich fenotypowe „uczenie się” w ślepe zaułki zamiast dróg ucieczki.
Cytowanie: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Słowa kluczowe: czerniak, oporność na leki, plastyczność komórkowa, terapia przerywana, modelowanie matematyczne