Clear Sky Science · pl
Strukturalne podstawy aktywacji zależnej od dimeryzacji reduktazy tlenku azotu zależnej od chinolu u Neisseria meningitidis
Jak bakterie przechytrzają naszą odporność
Gdy szkodliwe bakterie najeżdżają organizm, nasze komórki odpornościowe uwalniają toksyczne związki, takie jak tlenek azotu, aby je zabić. Niektóre patogeny wyewoluowały jednak molekularne sztuczki pozwalające zneutralizować ten atak i przetrwać. Badanie to ujawnia w niemal atomowych szczegółach, jak kluczowy enzym bakteryjny rekonfiguruje się w pary, by znacznie lepiej detoksykować tlenek azotu, oraz dlaczego zrozumienie tego przeobrażenia może otworzyć nowe drogi projektowania antybiotyków.
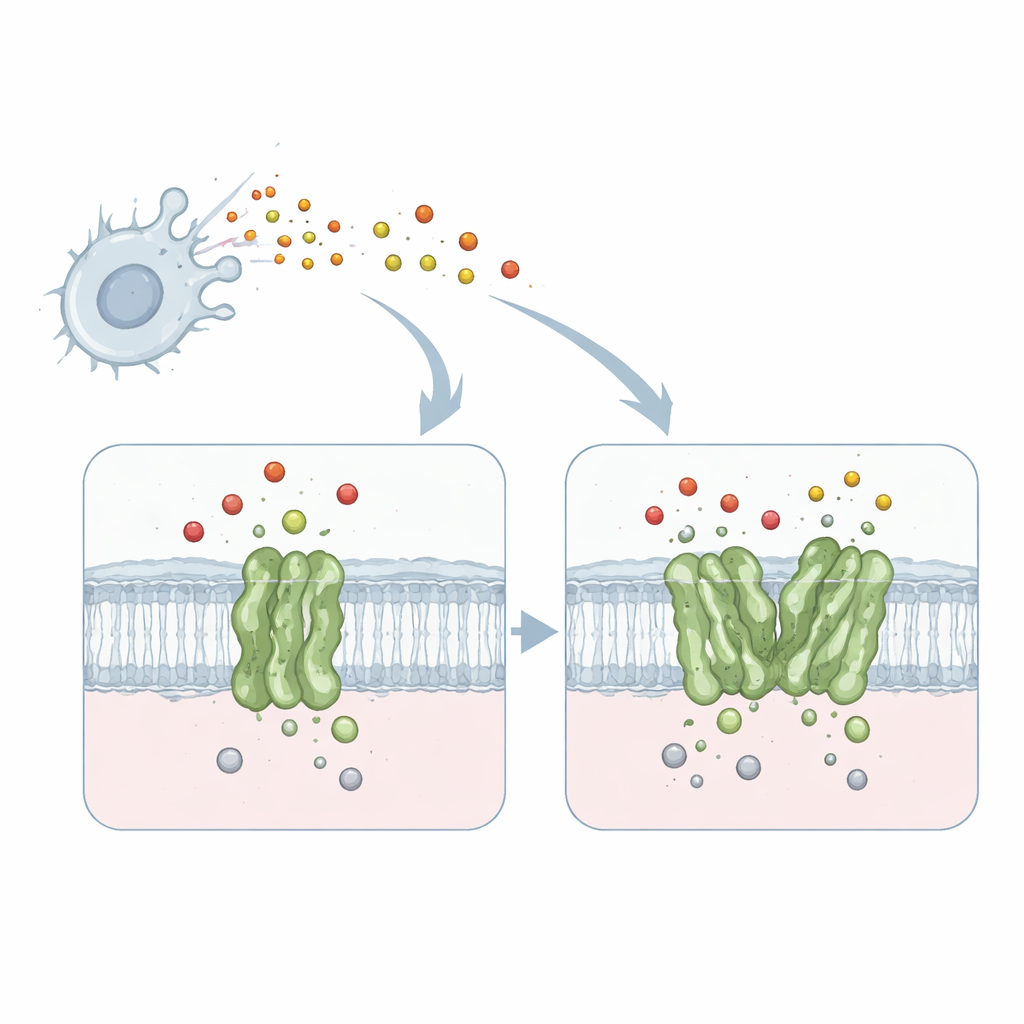
Mała maszyna unieszkodliwiająca toksyczny gaz
Praca koncentruje się na białku błonowym zwanym reduktazą tlenku azotu zależną od chinolu, w skrócie qNOR, pochodzącym od powodującego zapalenie opon mózgowo-rdzeniowych Neisseria meningitidis. qNOR osadza się w błonie komórkowej bakterii i przekształca tlenek azotu — toksyczny gaz produkowany przez nasz układ odpornościowy — w mniej szkodliwe produkty. Ta detoksykacja pozwala mikroorganizmowi nadal oddychać i rosnąć nawet w wrogich środowiskach, takich jak makrofagi człowieka. Ponieważ oddychanie i usuwanie tlenku azotu są kluczowe dla przeżycia patogenu, qNOR stanowi atrakcyjny cel dla nowych leków przeciwmikrobowych.
Gdy jeden jest dobry, a dwa lepsze
Poprzednie badania biochemiczne wykazały, że qNOR może występować jako pojedyncza jednostka (monomer) lub para (dimer) i że dimer neutralizuje tlenek azotu dwa do czterech razy szybciej. Do tej pory nie było jasne, dlaczego samo sparowanie dwóch kopii tego samego enzymu tak dramatycznie poprawia wydajność. Aby to wyjaśnić, badacze zastosowali wysokorozdzielczą pojedynczą cząsteczkową kriomikroskopię elektronową (single-particle cryo-EM), aby uchwycić szczegółowe struktury trójwymiarowe zarówno monomerycznego, jak i dimerycznego qNOR z tego samego szczepu bakterii. Otrzymali prawie atomowe rozdzielczości — 1,89 Å dla dimeru i 2,25 Å dla monomeru — wystarczająco ostre, by zlokalizować poszczególne łańcuchy boczne aminokwasów, jony metali i wiele cząsteczek wody.
Elastyczna helisa staje się usztywniającym wzmocnieniem
Niespodziewanie katalityczne jądro enzymu — centrum metaliczne, w którym zachodzi przekształcenie tlenku azotu — wyglądało niemal identycznie w obu formach. Kluczowe różnice pojawiły się jednak w pewnej odległości, w helisie przezbłonowej zwanej TM10 oraz w tym, jak styka się ona z inną helisą (TM2), gdy dwie cząsteczki qNOR łączą się w parę. W monomerze TM10 jest słabo osadzona i może znacznie się kołysać i wyginać, co ujawniła analiza obliczeniowa danych cryo-EM. W dimerze TM10 z każdego partnera blokuje się przy sąsiedzie, tworząc pakiet złożony z czterech helis, co znacznie ogranicza jego ruchomość. To usztywnienie subtelnie przesuwa krytyczny aminokwas — glutaminian o nazwie Glu563 — zbliżając go do innego glutaminianu (Glu494) w pobliżu miejsca aktywnego i kształtując bardziej skoncentrowaną trasę dla nadchodzących protonów niezbędnych do reakcji.
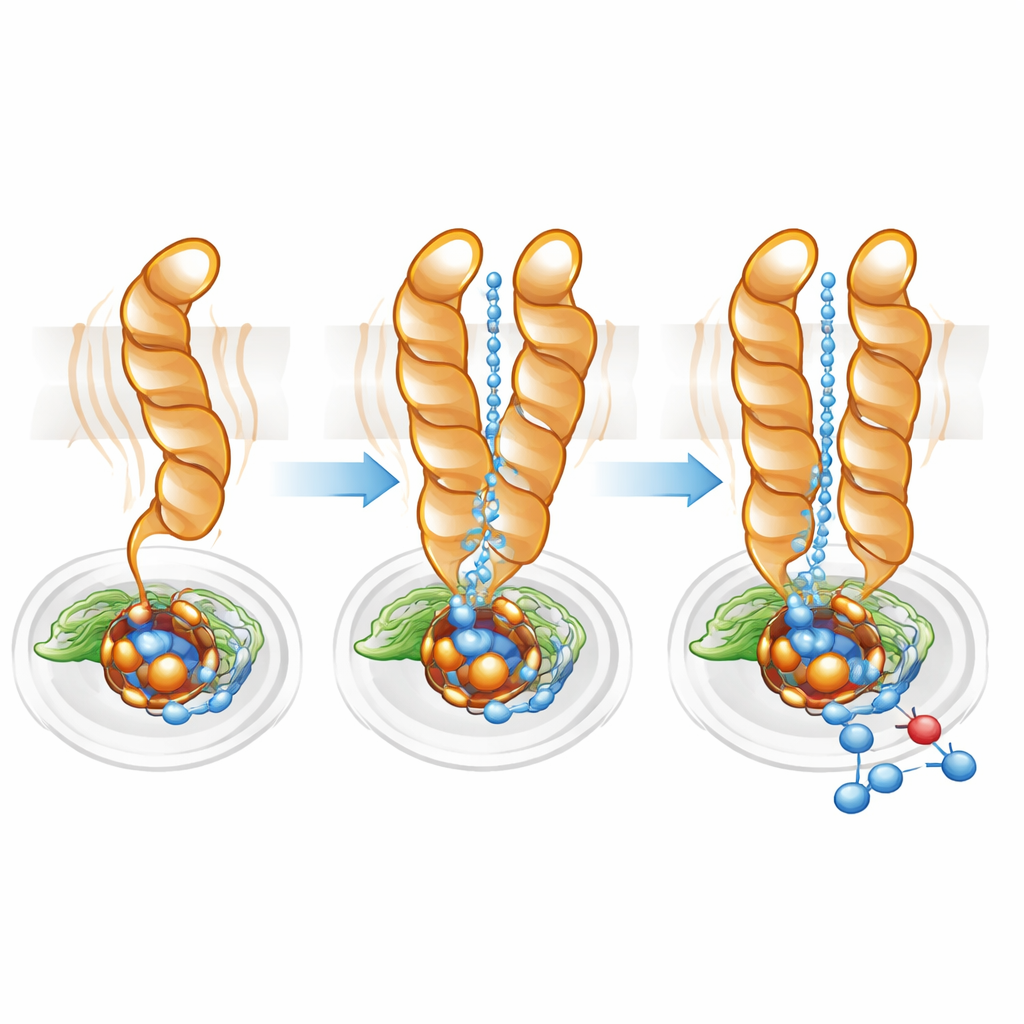
Dostrajanie autostrady protonowej
Protony — dodatnio naładowane jony wodoru — muszą być dostarczone wydajnie z wnętrza komórki do ukrytego miejsca aktywnego, aby redukcja tlenku azotu mogła zajść. Korzystając z oprogramowania do mapowania ścieżek, zespół zidentyfikował hydrofilową wnękę łączącą cytoplazmę z miejscem aktywnym zarówno w monomerze, jak i w dimerze. Jednak w monomerze kanał ten był szerszy i bardziej rozproszony, co zgadza się z większą ruchomością TM10. W dimerze zablokowane położenie TM10 i korzystna orientacja Glu563 pomogły wyznaczyć bardziej bezpośrednią, lepiej zorganizowaną ścieżkę. Mutacje Glu563 na aminokwasy niezdolne do tworzenia tych samych oddziaływań obniżyły aktywność enzymu do poniżej 10% normy i również destabilizowały dimer, podczas gdy mutacje w powiązanych pozycjach zmniejszały ilość niehemowego żelaza niezbędnego w miejscu aktywnym. Razem wyniki te pokazują, że tworzenie dimeru oraz precyzyjne ustawienie Glu563 i Glu494 są ściśle powiązane zarówno ze stabilnością strukturalną, jak i wydajnością katalityczną.
Od wglądu strukturalnego do nowych terapii
Wyniki ukazują wyraźny związek między parowaniem białek na powierzchni błony a drobnymi korektami głęboko we wnętrzu miejsca aktywnego, które kontrolują, jak skutecznie qNOR usuwa tlenek azotu. Mówiąc prościej: gdy dwie kopie enzymu obejmują się, prostują i usztywniają elastyczny fragment, który pomaga kierować protony do centrum reakcji, zwiększając wydajność enzymu. Dla rozwoju leków sugeruje to niekonwencjonalną strategię: zamiast blokować miejsce aktywne bezpośrednio, można zaprojektować molekuły rozdzierające dimer lub zakłócające interakcję Glu563–Glu494, zmuszając enzym do wolniejszego stanu monomerycznego. Ponieważ qNOR i powiązane enzymy są kluczowe dla przeżycia kilku groźnych, opornych na leki patogenów, takie podejścia oparte na strukturze mogą przyczynić się do następnej generacji ukierunkowanych środków przeciwmikrobowych.
Cytowanie: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Słowa kluczowe: detoksykacja tlenku azotu, oddychanie bakteryjne, enzymy błonowe, kriomikroskopia elektronowa, cele leków przeciwmikrobowych