Clear Sky Science · pl
Przestrzenne multiomiki ujawniają immunometaboliczne cechy zapalnej granicy wywołane przez nieodwracalną elektooporację w raku wątroby
Dlaczego nowe leczenie raka wątroby wymaga uważniejszego przyjrzenia się
Nieodwracalna elektroporacja (IRE) to nowsza metoda niszczenia guzów wątroby, która używa krótkich, wysokonapięciowych impulsów elektrycznych zamiast ciepła. Ponieważ oszczędza pobliskie naczynia krwionośne i przewody żółciowe, jest szczególnie przydatna w przypadku nowotworów położonych w delikatnych miejscach. Mimo to u nawet jednej trzeciej pacjentów guz nawraca tuż obok obszaru poddanego zabiegowi. W tym badaniu pytano, co dzieje się w tej wąskiej strefie granicznej po IRE — i czy ukryte zmiany w komórkach odpornościowych i metabolizmie komórek tam mogą po cichu stworzyć warunki sprzyjające odrostowi nowotworu.
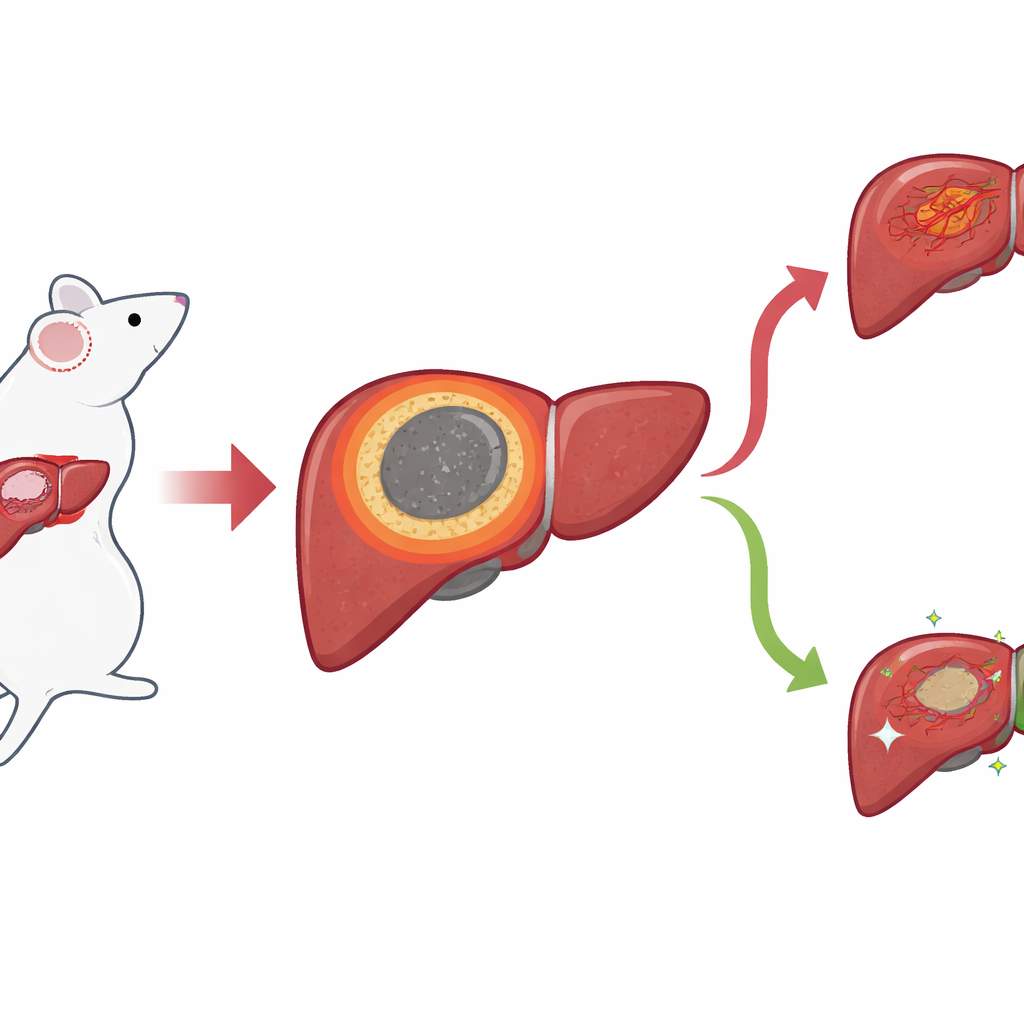
Wąska granica o dużych konsekwencjach
Wykorzystując model myszy z rakiem wątroby, badacze skupili się na cienkim pierścieniu tkanki, który powstaje między martwiczym, zniszczonym jądrem a otaczającą zdrową wątrobą po IRE. Nazywają go zapalną granicą (inflammatory margin, IM). Standardowe obrazy mikroskopowe pokazały, że ta strefa znajduje się dokładnie tam, gdzie zwykle pojawiają się miejscowe nawroty, ale jej granice trudno było wyznaczyć gołym okiem. Aby uzyskać wyraźniejszy obraz, zespół zastosował metody „przestrzenne”, które odczytują, jakie geny i małe cząsteczki są obecne, zachowując jednocześnie ich lokalizację w tkance. Dzięki przestrzennej transkryptomice odwzorowali aktywność genów punkt po punkcie i odkryli odrębną grupę punktów, która precyzyjnie pokrywała się z IM, oddzielając martwicze centrum od zdrowej wątroby i obszarów guza.
Komórki odpornościowe napływają — ale wiele z nich hamuje atak
Naukowcy następnie wykorzystali pojedynczo-komórkowe i pojedynczo-jądrowe sekwencjonowanie RNA oraz potężną metodę profilowania CyTOF, aby skatalogować poszczególne typy komórek w wątrobie. Stwierdzili, że IM dominuje typ komórek odpornościowych zwany makrofagami. W szczególności do IM w ciągu kilku dni po IRE napłynęła podgrupa przypominająca „makrofagi związane z lipidami” (lipid-associated macrophages, LAMs). Komórki te noszą markery powierzchniowe i sygnatury genowe związane z immunosupresją, w tym wysokie poziomy PD-L1, cząsteczki znanej z tłumienia reakcji limfocytów T. Analizy ekspresji genów sugerowały, że te makrofagi są biegłe w fagocytozie, reagowaniu na chemoatraktanty i wysyłaniu sygnałów, które mogą powstrzymywać właśnie te limfocyty T, potrzebne do zabijania komórek nowotworowych. Obrazowanie potwierdziło, że makrofagi pozytywne pod względem PD-L1 były znacznie liczniejsze w IM niż w pobliskiej zdrowej tkance.
Ognisko zmienionej chemii lipidów
Następnie zespół nałożył ten obraz immunologiczny na przestrzenną metabolomikę, metodę obrazowania za pomocą spektrometrii mas, która mapuje rozkład setek małych cząsteczek. Pokazali, że IM ma odcisk metaboliczny różny od zarówno martwiczego jądra, jak i otaczającej wątroby. W tym wąskim pasie wiele szlaków lipidowych (związanych z tłuszczami) było silnie wzmocnionych, w tym produkcja nienasyconych kwasów tłuszczowych, pochodnych kwasu arachidonowego oraz sphingolipidów. Kluczowe lipidy sygnałowe, takie jak prostaglandyny i leukotrieny pochodzące z kwasu arachidonowego, były wzbogacone w IM, podczas gdy inne ścieżki enzymatyczne przetwarzające ten sam związek były stosunkowo słabe. Inna rodzina lipidów, sphingolipidy — w tym ceramidy i sfingomieliny — również się kumulowała, wspierana przez zwiększoną ekspresję enzymów, które je wytwarzają i remodelują.
Krokowy przesunięcie od uszkodzenia do niszy bogatej w paliwo
Dzieląc zapalną granicę na trzy cienkie warstwy od martwicznego jądra na zewnątrz, badacze zaobserwowali stopniowe przesunięcie w chemii. Najbliżej martwej strefy najwyższe były złożone lipidy i związane z cholesterolem cząsteczki, podczas gdy dalej na zewnątrz rosły małe cząsteczki związane z energią, takie jak glukoza i niektóre aminokwasy. Ten wzorzec sugeruje, że w krótkim dystansie tkanka przechodzi od środowiska naładowanego lipidami i bogatego w sygnały do środowiska ukierunkowanego na zasilanie przetrwania i wzrostu komórek. Autorzy proponują, że to stopniowe przeprogramowanie pomaga podtrzymywać łakome na lipidy, immunosupresyjne makrofagi dominujące w IM i może po cichu przygotowywać grunt pod ponowne zasiedlenie przez komórki nowotworowe.
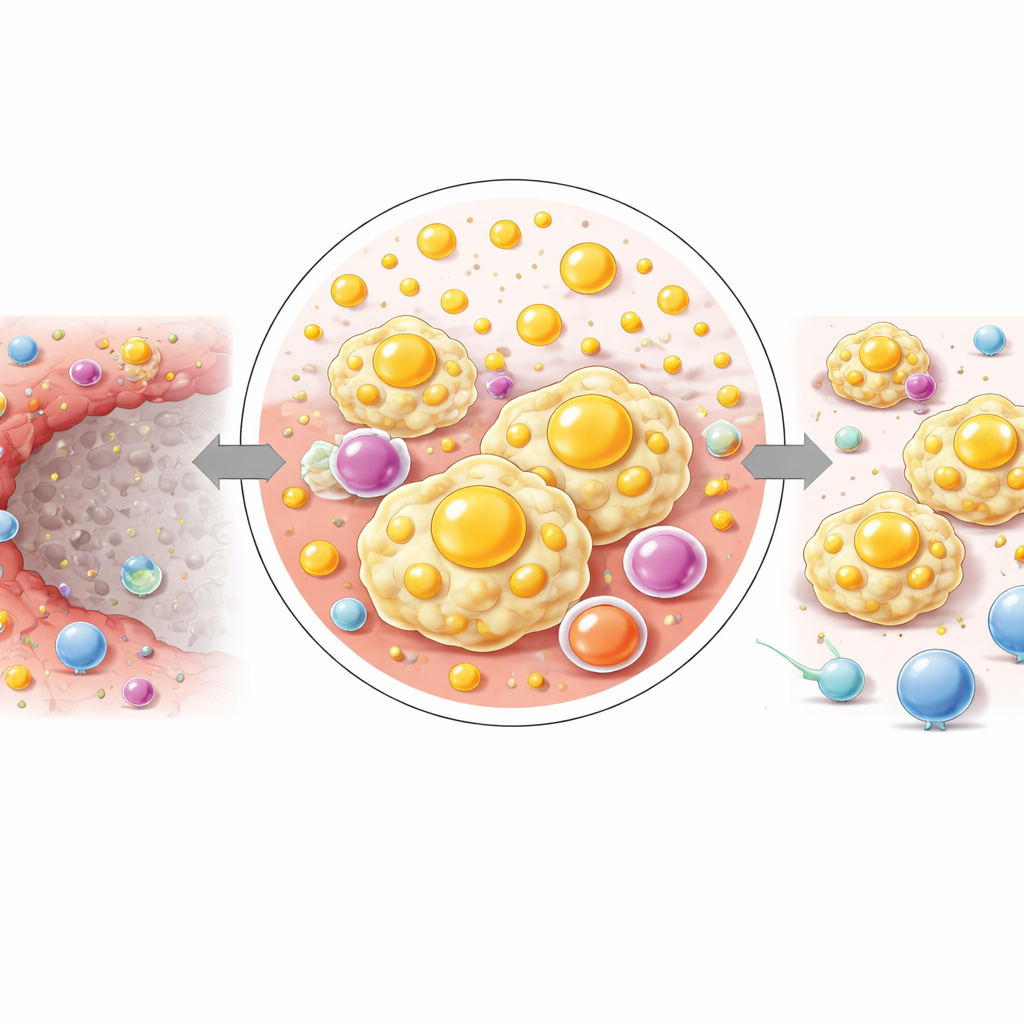
Co to oznacza dla przyszłej opieki nad rakiem wątroby
Mówiąc prosto, praca ta pokazuje, że IRE robi więcej niż tylko zabija komórki guza: tworzy również wąski pierścień tkanki, w którym komórki odpornościowe i chemia lipidów wspólnie budują osłoniętą, sprzyjającą guzowi „dzielnicę”. Makrofagi w tej strefie są liczne, naładowane lipidami i nastawione na wyłączanie limfocytów T zamiast im pomagać. Ponieważ te zmiany ściśle wiążą się ze specyficznymi szlakami metabolicznymi, sugerują nowe kierunki terapii. Połączenie IRE z lekami celującymi w metabolizm lipidów lub blokującymi PD-L1 w tej granicy mogłoby w zasadzie przekształcić granicę podatną na nawroty w strefę, która naprawdę kończy zadanie w walce z rakiem wątroby.
Cytowanie: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Słowa kluczowe: rak wątroby, ablacja guza, mikrośrodowisko immunologiczne, makrofagi, metabolizm lipidów