Clear Sky Science · pl
Ozdabianie powierzchni bakterii tworzy odporne żywe leki do lepszego leczenia wrzodziejącego zapalenia jelita grubego
Przekształcanie przyjaznych zarazków w małych obrońców
Wrzodziejące zapalenie jelita grubego to bolesna choroba jelit, w której własne jelito pacjenta ulega przewlekłemu zapaleniu, prowadząc do naglącej biegunki, krwawień i znacznego pogorszenia jakości życia. Lekarze i pacjenci mają nadzieję na «dobre bakterie» w pigułkach, które mogłyby łagodzić to zapalenie od środka, ale większość tych mikroorganizmów ginie w trudnej podróży przez żołądek i jelito cienkie, zanim dotrze do okrężnicy, gdzie są potrzebne. W tym badaniu opisano nowy sposób „ubrania” probiotycznych bakterii w ochronną zbroję, dzięki czemu mogą bezpiecznie przejść przez przewód pokarmowy, osiedlić się w okrężnicy i pomóc naprawić uszkodzone jelito.
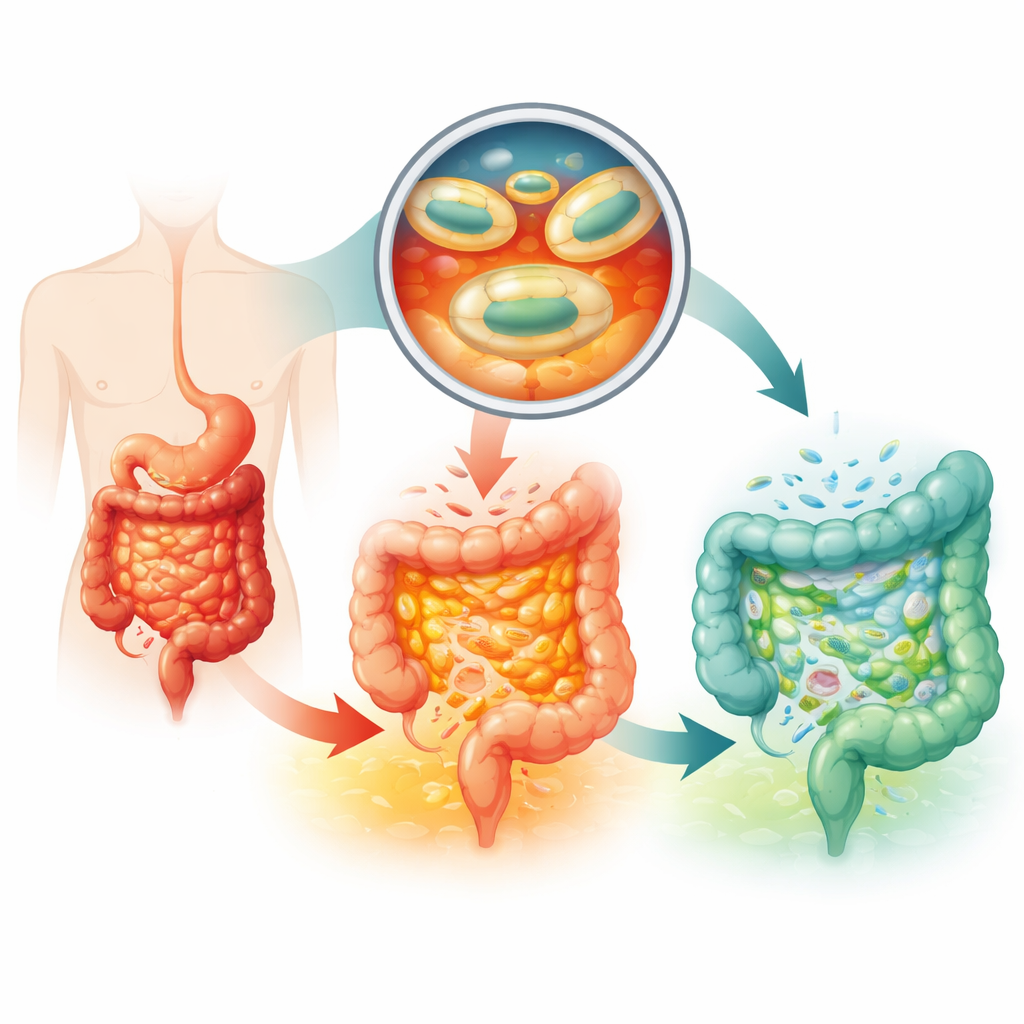
Dlaczego obecne pigułki z probiotykami często zawodzą
Standardowe metody leczenia wrzodziejącego zapalenia jelita grubego opierają się na lekach przeciwzapalnych i immunosupresyjnych, które mogą powodować poważne skutki uboczne i nie działają u wszystkich. Probiotyki oferują łagodniejsze podejście, pomagając przywrócić równowagę społeczności mikrobiologicznej jelita. Specjalny szczep Escherichia coli o nazwie Nissle 1917 jest już zatwierdzony jako lek na tę chorobę, ale pacjenci muszą przyjmować niezwykle duże dawki codziennie, a mimo to korzyści są umiarkowane. Kluczowym problemem jest przetrwanie i dostarczenie: kwas żołądkowy, enzymy trawienne oraz szybki pasaż przez górne odcinki jelit zabijają lub wypłukują większość bakterii, zanim zdążą się przyczepić i namnożyć w okrężnicy, gdzie normalnie znajduje się ponad 99% mikroorganizmów jelitowych.
Budowanie ochronnej powłoki wokół pomocnych bakterii
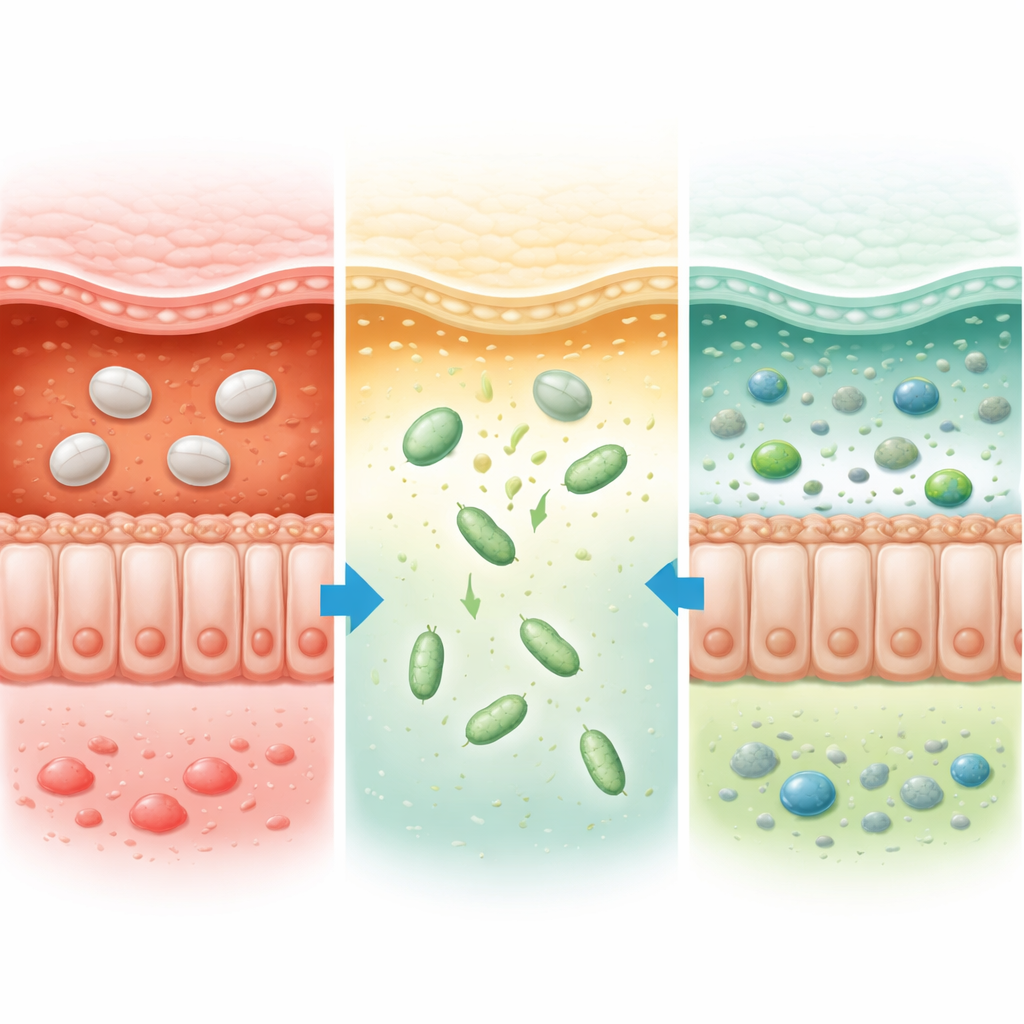
Aby to rozwiązać, badacze stworzyli cienką, inteligentną powłokę wokół każdej komórki probiotycznej, używając pochodzącego z roślin materiału o nazwie lignina. Chemicznie zmodyfikowali ligninę, aby uczynić ją bardziej rozpuszczalną i wrażliwą na zmiany kwasowości, otrzymując substancję stabilną w silnym kwasie, która rozpada się w mniej kwaśnym środowisku okrężnicy. Przy użyciu delikatnego procesu warstwa po warstwie najpierw dodali jony wapnia na powierzchnię probiotyku, a następnie owinęli go zmodyfikowaną ligniną, tworząc gładką „zbroję” o grubości około jednej dziesięciotysięcznej milimetra. Mikroskopia i pomiary rozmiaru cząstek wykazały, że tarcza ta chroni bakterie bez ich zabijania, a ta sama metoda zadziałała na kilku bardzo różniących się gatunkach bakterii, co sugeruje, że może posłużyć jako ogólna platforma dla wielu terapii probiotycznych.
Ukierunkowanie na okrężnicę i wspomaganie jej gojenia
W testach w symulowanych płynach trawiennych niechronione bakterie były szybko niszczone przez kwas żołądkowy, podczas gdy „opancerzone” bakterie pozostawały żywe przez godziny i uwalniały swój ładunek efektywnie dopiero przy pH przypominającym okrężnicę. U myszy z chemicznie wywołanym wrzodziejącym zapaleniem jelita grubego pokryte bakterie gromadziły się silnie w okrężnicy, podczas gdy bakterie bez powłoki lub proste mieszaniny z materiałem powłokowym w dużej mierze zawodziły. Zespół wykorzystał obrazowanie fluorescencyjne, testy genetyczne i modelowanie matematyczne, aby pokazać, że chronione bakterie nie tylko dotarły do okrężnicy w nienaruszonym stanie, lecz także się tam rozmnożyły, osiągając około jednej na tysiąc wszystkich mikroorganizmów jelitowych. Leczone myszy traciły mniej na wadze, miały dłuższe okrężnice i znacznie zdrowsze tkanki jelitowe w badaniu mikroskopowym, z silniejszymi połączeniami międzykomórkowymi i przywróconą warstwą śluzu, które razem tworzą istotną barierę między organizmem a zawartością jelit.
Uspokajanie układu odpornościowego i przywracanie równowagi mikrobiomu
Ponad fizyczną naprawą, opancerzone probiotyki przekształciły krajobraz immunologiczny i mikrobiologiczny w chorym jelicie. We krwi i w okrężnicy chorych myszy poziomy cząsteczek zapalnych były wysokie, a poziomy kluczowego sygnału przeciwzapalnego niskie; nowe leczenie odwróciło te tendencje, przesuwając układ odpornościowy w kierunku stanu bardziej wyciszonego. Szczegółowe analizy komórek wykazały zmiany w składzie komórek odpornościowych zarówno w okrężnicy, jak i w śledzionie. Równocześnie sekwencjonowanie DNA mikrobioty jelitowej wykazało, że terapia zwiększyła ogólną różnorodność mikroorganizmów i wzmocniła obecność kilku grup bakterii powiązanych ze zdrowiem jelit, w tym Akkermansia i Muribaculum. Profilowanie metabolitów dodatkowo pokazało szerokie zmiany w małych cząsteczkach związanych z metabolizmem witamin, kwasów tłuszczowych i aminokwasów, co sugeruje, że zrównoważony mikrobiom wytwarza środowisko chemiczne bardziej sprzyjające gojeniu.
Od badań na myszach do przyszłych żywych leków
Podsumowując, praca wykazuje, że nadanie probiotykom pH-czułej zbroi może niezawodnie przetransportować je przez trudy przewodu pokarmowego i zdeponować tam, gdzie wrzodziejące zapalenie jelita grubego wyrządza najwięcej szkód. U myszy ta strategia pozwoliła na kolonizację okrężnicy przy znacznie niższych dawkach bakterii, naprawę bariery jelitowej, zmniejszenie szkodliwego stanu zapalnego oraz przywrócenie zdrowszej społeczności mikrobiologicznej i profilu metabolicznego. Ponieważ powłoka roślinna w dużej mierze przechodzi przez organizm niezmieniona, a metoda może być zastosowana do wielu typów bakterii, autorzy argumentują, że ich podejście stanowi szeroko użyteczny plan projektowania kolejnej generacji «żywych» leków na wrzodziejące zapalenie jelita grubego i inne choroby okrężnicy.
Cytowanie: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
Słowa kluczowe: wrzodziejące zapalenie jelita grubego, probiotyki, mikrobiom jelitowy, dostarczanie leków, bariera jelitowa