Clear Sky Science · pl
Sekwencjonowanie RNA pojedynczych jąder i badania funkcjonalne ostrego upośledzenia poznawczego wywołanego metamfetaminą
Dlaczego to ma znaczenie dla zdrowia mózgu
Metamfetamina często przedstawiana jest jako substancja „wypalająca” mózg, ale jak rzeczywiście wygląda to uszkodzenie w komórkach? To badanie zagląda do centrum pamięci mysiego mózgu — hipokampa — komórka po komórce, aby zobaczyć, jak krótka fala intensywnego użycia metamfetaminy miesza mechanizmy wspierające uczenie się i pamięć. Mapując te zmiany z bezprecedensową szczegółowością, praca wskazuje nowe biologiczne słabe punkty, które pewnego dnia mogłyby być celem interwencji chroniących lub przywracających funkcję mózgu u osób narażonych na ten narkotyk.
Jak dawka „binge” metamfetaminy wpływa na pamięć
Naukowcy zadali najpierw proste pytanie: czy intensywna, krótkotrwała dawka metamfetaminy szkodzi pamięci u myszy? Zwierzęta otrzymały cztery zastrzyki metamfetaminy w ciągu jednego dnia, naśladując wzorzec binge. W testach te myszy miały trudności z rozpoznawaniem nowych obiektów i potrzebowały więcej czasu, by odnaleźć ukrytą platformę w labiryncie wodnym — klasyczne objawy zaburzeń uczenia się i pamięci przestrzennej. Nawet po usunięciu platformy mniej przeszukiwały właściwe miejsce, co sugeruje, że coś w hipokampie — ośrodku nawigacji i pamięci w mózgu — przestało działać prawidłowo.
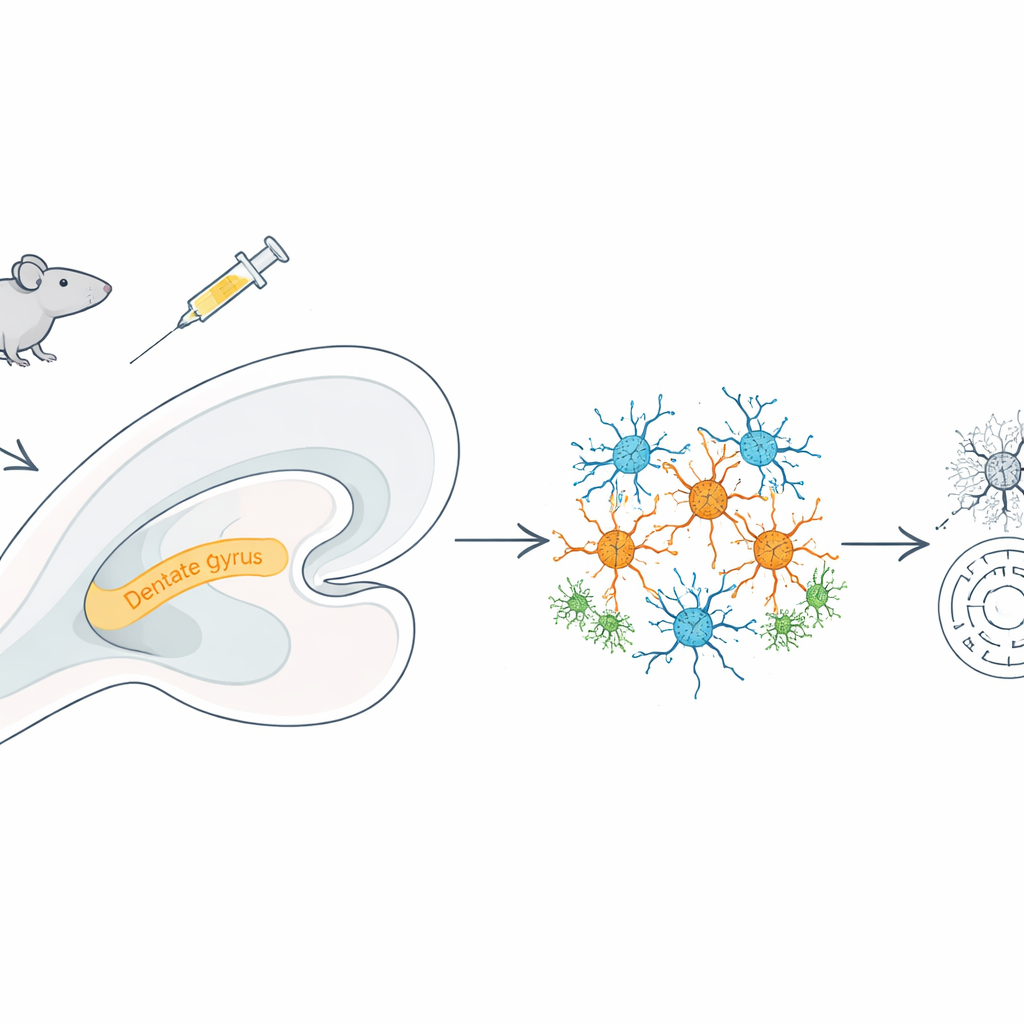
Przyglądanie się każdemu jądru z osobna
Aby zrozumieć, co szwankuje, zespół zastosował sekwencjonowanie RNA pojedynczych jąder, technikę odczytującą, które geny są aktywne w tysiącach indywidualnych jąder komórkowych jednocześnie. Z ponad 36 000 jąder hipokampa zidentyfikowali dziesięć głównych typów komórek, w tym neurony pobudzające i hamujące, astrocyty, mikroglej, oligodendrocyty oraz komórki naczyń krwionośnych. Ekspozycja na metamfetaminę przesunęła ten krajobraz komórkowy: było więcej neuronów pobudzających, mikrogleju, oligodendrocytów i komórek śródbłonka, ale mniej neuronów hamujących. To przechyliło równowagę w stronę pobudzenia, stanu, który może uczynić obwody nerwowe bardziej podatnymi na stres i uszkodzenie.
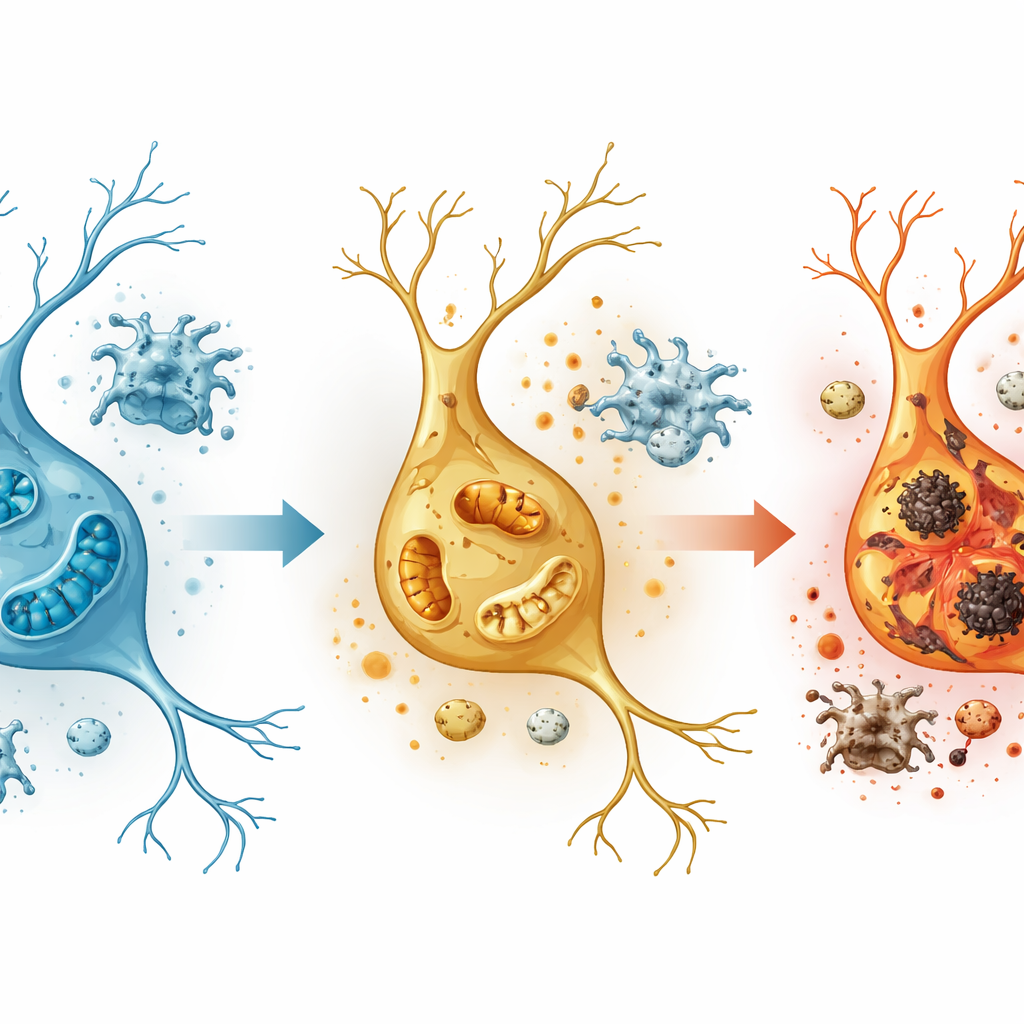
Fabryki energii pod stresem i osłabione mechanizmy obronne
Najbardziej dramatyczne zmiany w aktywności genów pojawiły się w neuronach pobudzających, zwłaszcza w regionie hipokampa zwanym zakrętem zębatym, który jest kluczowy dla formowania odrębnych wspomnień. Tam geny związane z fosforylacją oksydacyjną — procesem, w którym mitochondria wytwarzają energię komórkową — zostały silnie zmienione, a obrazy z mikroskopu elektronowego ukazały mitochondria pofragmentowane, z uszkodzonymi wewnętrznymi strukturami. Jednocześnie aktywowane były szlaki związane z reaktywnymi formami tlenu i sygnałami zapalnymi, a organelle zwane peroksysomami, które pomagają kontrolować szkodliwe produkty uboczne metabolizmu, wykazywały oznaki niewydolności. Kluczowe geny związane z peroksysomami, w tym PEX5, zmniejszyły aktywność, podczas gdy geny napędzające zapalenie i stres oksydacyjny wzrosły, co sugeruje, że metamfetamina popycha neurony w kierunku kryzysu energetycznego przy jednoczesnym osłabieniu ich naturalnych systemów detoksykacji.
Wrażliwe grupy komórek i zaburzone rozmowy międzykomórkowe
Zagłębiając się dalej, badacze odkryli, że neurony pobudzające można podzielić na pięć podtypów regionalnych, przy czym komórki zakrętu zębatego wykazywały najsilniejsze sygnały stresu: nasilone zapalenie, większe obciążenie oksydacyjne i rodzaj zapalnej śmierci komórkowej znany jako piroptoza. W tym regionie zidentyfikowali podgrupę neuronów pobudzających silnie wzbogaconą u zwierząt traktowanych metamfetaminą, która niosła najsilniejsze sygnatury uszkodzenia, wskazując na prawdopodobne ofiary ekspozycji. W całym hipokampie komunikacja między neuronami pobudzającymi a innymi typami komórek nasiliła się, podczas gdy połączenia neuronów hamujących osłabły. Mikroglej, strażnik immunologiczny mózgu, przeszedł w wysoce zapalny stan. Jednocześnie zespół wyodrębnił klastry genów, których aktywność ściśle korelowała z wydajnością pamięci, wskazując sieci w neuronach pobudzających, neuronach hamujących, astrocytach i oligodendrocytach, które mogą pogarszać lub łagodzić spadek funkcji poznawczych.
Nowe molekularne wskazówki i możliwe drogi ochronne dla mózgu
Badanie wyróżniło też konkretne molekuły, które mogą być centralnymi węzłami w urazie wywołanym metamfetaminą. Jedną z nich jest białko przetwarzające RNA o nazwie Ddx5, które było silnie podwyższone w wielu typach komórek, szczególnie w zakręcie zębatym, sugerując szeroką odpowiedź na stres, której ochronna lub szkodliwa rola wymaga dalszego wyjaśnienia. W przeciwieństwie do tego PEX5 i regulator lipidowy PPARα, oba ważne dla równowagi peroksysom–mitochondria, były osłabione w neuronach pobudzających. Razem te zmiany sugerują, że przywrócenie metabolizmu energetycznego, wzmocnienie funkcji peroksysomów i uspokojenie nadmiernie aktywnych odpowiedzi immunologicznych mogą być obiecującymi strategiami ograniczania uszkodzeń mózgu po ostrym narażeniu na metamfetaminę.
Co to oznacza prostymi słowami
Mówiąc prosto, praca pokazuje, że nawet krótkotrwały epizod binge metamfetaminy może pozostawić głębokie piętno w centrum pamięci mózgu. Wprowadza kluczowe neurony w zakręcie zębatym w niedobór energii, zalewa je toksycznymi produktami ubocznymi, osłabia ich systemy oczyszczania i pobudza pobliskie komórki odpornościowe, które dodatkowo wywołują stan zapalny tkanek. Mapując dokładnie, które typy komórek, regiony i sieci genów są najbardziej dotknięte, badanie wychodzi poza niejasne pojęcie „uszkodzenia mózgu” i wskazuje konkretne procesy biologiczne — takie jak wadliwa produkcja energii i zaburzone ścieżki detoksykacji — które mogłyby być celem działań chroniących lub naprawczych u osób dotkniętych działaniem metamfetaminy.
Cytowanie: An, D., Lu, F., Wang, Y. et al. Single-nucleus RNA sequencing and functional studies of acute methamphetamine-induced cognitive impairment. Commun Biol 9, 440 (2026). https://doi.org/10.1038/s42003-026-09728-2
Słowa kluczowe: metamfetamina, hipokamp, sekwencjonowanie RNA pojedynczych jąder, dysfunkcja mitochondriów, neurozapalenie